Задача:
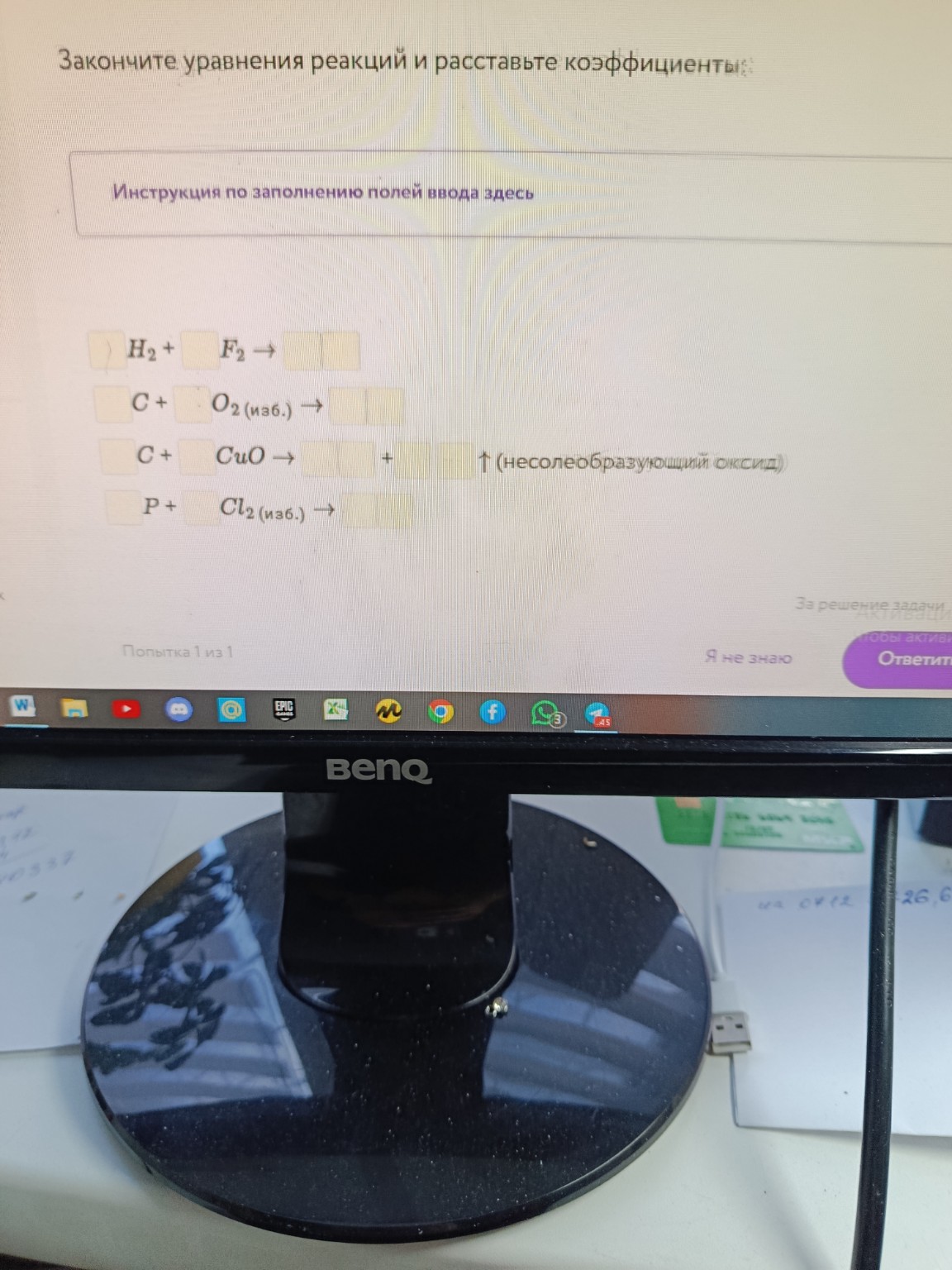
Закончите уравнения реакций и расставьте коэффициенты:
1. \( \mathrm{H_2} + \mathrm{F_2} \rightarrow \)
2. \( \mathrm{C} + \mathrm{O_2} \text{(изб.)} \rightarrow \)
3. \( \mathrm{C} + \mathrm{CuO} \rightarrow \uparrow \text{(несолеобразующий оксид)} \)
4. \( \mathrm{P} + \mathrm{Cl_2} \text{(изб.)} \rightarrow \)
Решение:
1. Реакция водорода с фтором:
- Водород (H2) реагирует с фтором (F2) с образованием фтороводорода (HF). Это очень бурная реакция, протекающая даже в темноте и при низких температурах.
- Уравнение реакции: \( \mathrm{H_2} + \mathrm{F_2} \rightarrow \mathrm{HF} \)
- Расставляем коэффициенты:
- Слева: 2 атома H, 2 атома F.
- Справа: 1 атом H, 1 атом F.
- Чтобы уравнять, ставим коэффициент 2 перед HF.
- Завершенное и уравненное уравнение: \[ \mathrm{H_2} + \mathrm{F_2} \rightarrow \mathrm{2HF} \]
2. Реакция углерода с избытком кислорода:
- Углерод (C) при горении в избытке кислорода (O2) образует углекислый газ (CO2).
- Уравнение реакции: \( \mathrm{C} + \mathrm{O_2} \rightarrow \mathrm{CO_2} \)
- Расставляем коэффициенты:
- Слева: 1 атом C, 2 атома O.
- Справа: 1 атом C, 2 атома O.
- Уравнение уже уравнено.
- Завершенное и уравненное уравнение: \[ \mathrm{C} + \mathrm{O_2} \text{(изб.)} \rightarrow \mathrm{CO_2} \]
3. Реакция углерода с оксидом меди(II) с образованием несолеобразующего оксида:
- Углерод (C) является восстановителем и может восстанавливать металлы из их оксидов при нагревании. В данном случае, углерод восстанавливает медь из оксида меди(II) (CuO).
- При этом углерод окисляется. Если образуется несолеобразующий оксид, то это угарный газ (CO).
- Уравнение реакции: \( \mathrm{C} + \mathrm{CuO} \rightarrow \mathrm{Cu} + \mathrm{CO} \)
- Расставляем коэффициенты:
- Слева: 1 атом C, 1 атом Cu, 1 атом O.
- Справа: 1 атом C, 1 атом Cu, 1 атом O.
- Уравнение уже уравнено.
- Завершенное и уравненное уравнение: \[ \mathrm{C} + \mathrm{CuO} \rightarrow \mathrm{Cu} + \mathrm{CO} \uparrow \]
4. Реакция фосфора с избытком хлора:
- Фосфор (P) реагирует с хлором (Cl2). В зависимости от соотношения реагентов могут образовываться хлорид фосфора(III) (PCl3) или хлорид фосфора(V) (PCl5).
- Поскольку указан избыток хлора, образуется хлорид фосфора(V).
- Уравнение реакции: \( \mathrm{P} + \mathrm{Cl_2} \rightarrow \mathrm{PCl_5} \)
- Расставляем коэффициенты:
- Слева: 1 атом P, 2 атома Cl.
- Справа: 1 атом P, 5 атомов Cl.
- Чтобы уравнять атомы хлора, найдем наименьшее общее кратное для 2 и 5, это 10.
- Ставим коэффициент 5 перед Cl2: \( \mathrm{P} + \mathrm{5Cl_2} \rightarrow \mathrm{PCl_5} \) (теперь 10 атомов Cl слева).
- Чтобы получить 10 атомов Cl справа, нужно 2 молекулы PCl5: \( \mathrm{P} + \mathrm{5Cl_2} \rightarrow \mathrm{2PCl_5} \) (теперь 2 атома P справа).
- Чтобы уравнять атомы фосфора, ставим коэффициент 2 перед P: \( \mathrm{2P} + \mathrm{5Cl_2} \rightarrow \mathrm{2PCl_5} \)
- Завершенное и уравненное уравнение: \[ \mathrm{2P} + \mathrm{5Cl_2} \text{(изб.)} \rightarrow \mathrm{2PCl_5} \]
Итоговые уравнения:
1. \( \mathrm{H_2} + \mathrm{F_2} \rightarrow \mathrm{2HF} \)
2. \( \mathrm{C} + \mathrm{O_2} \text{(изб.)} \rightarrow \mathrm{CO_2} \)
3. \( \mathrm{C} + \mathrm{CuO} \rightarrow \mathrm{Cu} + \mathrm{CO} \uparrow \)
4. \( \mathrm{2P} + \mathrm{5Cl_2} \text{(изб.)} \rightarrow \mathrm{2PCl_5} \)