schoolМатематика
verifiedРешено AI
Решение: Хлорсеребряный электрод - тип электрода
help_outlineУсловие задачи
Индикаторная титрование неверный ответ Реши задачу: Индикаторная титрование ответ неверный Реши задачу: Ответ на третий вопрос неверен Реши задачу: Ответ на третий вопрос неверен
lightbulbКраткий ответ
Хлорсеребряный электрод является ионообменным (электродом второго рода), а не электронообменным. В нем происходит обмен ионами между твердой фазой (AgCl) и раствором.
Подробное решение
Давайте разберем третий вопрос еще раз более внимательно.
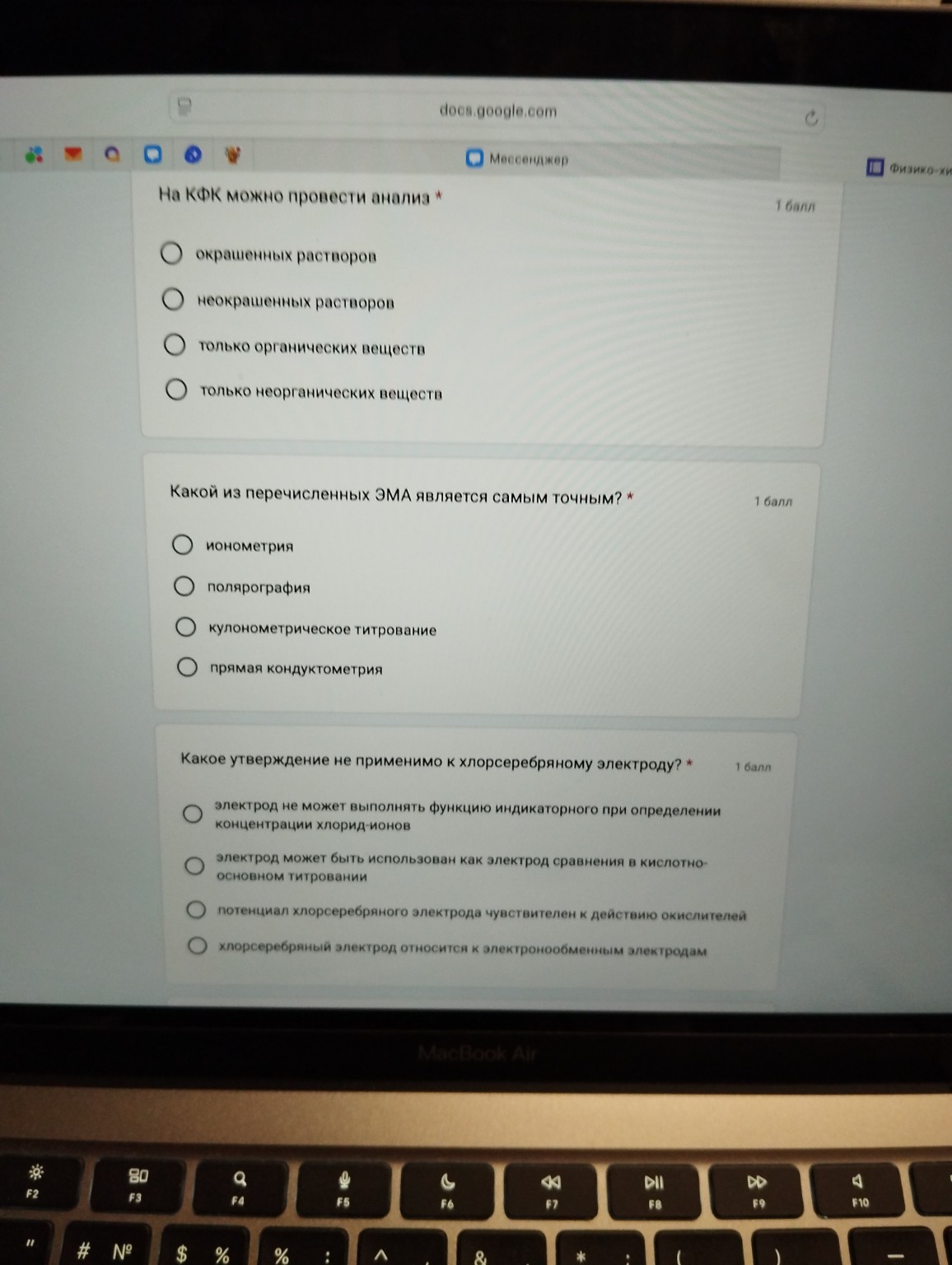
Вопрос: Какое утверждение не применимо к хлорсеребряному электроду?
Правильный ответ: хлорсеребряный электрод относится к электронообменным электродам.
Пояснение:
Это утверждение неверно (не применимо), потому что хлорсеребряный электрод является ионообменным электродом (электродом второго рода). В электронообменных электродах (например, платиновом в системе \( Fe^{3+}/Fe^{2+} \)) электрод лишь передает электроны, не участвуя в химических превращениях своего материала. В хлорсеребряном же электроде происходит обмен ионами между твердой фазой (\( AgCl \)) и раствором.
Разбор остальных вариантов (почему они применимы):
1. Электрод может выполнять функцию индикаторного при определении хлорид-ионов — это верно, так как его потенциал зависит от концентрации \( Cl^- \).
2. Электрод может быть использован как электрод сравнения — это его основная роль в аналитической химии.
3. Потенциал чувствителен к действию окислителей — это утверждение может считаться применимым в определенных условиях (окислители могут разрушать поверхность серебра или влиять на систему), но ключевым "неприменимым" термином здесь является классификация электрода.
Запись в тетрадь:
Утверждение "хлорсеребряный электрод относится к электронообменным электродам" является неверным, так как данный электрод относится к электродам второго рода (ионообменным).
Уравнение реакции на электроде:
\[ AgCl + e^- \rightleftharpoons Ag^0 + Cl^- \]