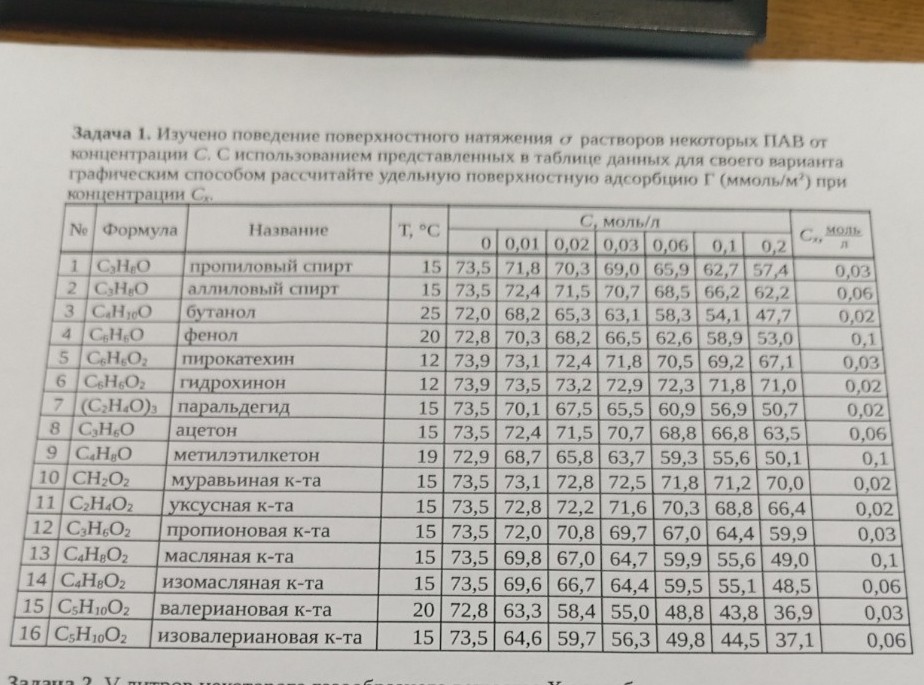
Задача 1. Изучено поведение поверхностного натяжения \(\sigma\) растворов некоторых ПАВ от концентрации \(C\). С использованием представленных в таблице данных для своего варианта графическим способом рассчитайте удельную поверхностную адсорбцию \(\Gamma\) (ммоль/м2) при концентрации \(C_x\).
Вариант 1: Пропиловый спирт (C3H8O)
Температура: 15 °C
Концентрация \(C_x\): 0,03 моль/л
Решение:
Для расчета удельной поверхностной адсорбции \(\Gamma\) будем использовать уравнение Гиббса для адсорбции:
\[\Gamma = -\frac{1}{RT} \left( \frac{d\sigma}{d\ln C} \right)_T\]где:
- \(\Gamma\) – удельная поверхностная адсорбция (ммоль/м2)
- \(R\) – универсальная газовая постоянная (8,314 Дж/(моль·К) или 8,314 м3·Па/(моль·К)). Поскольку нам нужно получить \(\Gamma\) в ммоль/м2, а концентрация дана в моль/л, удобнее использовать \(R = 8,314 \cdot 10^{-3}\) кДж/(моль·К) или 8,314 Дж/(моль·К) и перевести \(\sigma\) в мДж/м2 (что эквивалентно мН/м). Или же, если \(\sigma\) в мН/м, а \(C\) в моль/л, то \(R\) можно взять как 8,314 Дж/(моль·К) и затем перевести моль в ммоль. Давайте возьмем \(R = 8,314\) Дж/(моль·К) и учтем единицы в конце.
- \(T\) – абсолютная температура (К)
- \(\left( \frac{d\sigma}{d\ln C} \right)_T\) – производная поверхностного натяжения по натуральному логарифму концентрации при постоянной температуре.
Шаг 1: Перевод температуры в Кельвины.
Температура \(T = 15\) °C.
\[T = 15 + 273,15 = 288,15 \text{ К}\]Шаг 2: Подготовка данных для построения графика.
Из таблицы для пропилового спирта (C3H8O) при 15 °C имеем следующие данные:
| \(C\), моль/л | \(\sigma\), мН/м | \(\ln C\) |
| 0,01 | 71,8 | \(\ln(0,01) = -4,605\) |
| 0,02 | 70,3 | \(\ln(0,02) = -3,912\) |
| 0,03 | 69,0 | \(\ln(0,03) = -3,507\) |
| 0,06 | 65,9 | \(\ln(0,06) = -2,813\) |
| 0,1 | 62,7 | \(\ln(0,1) = -2,303\) |
| 0,2 | 57,4 | \(\ln(0,2) = -1,609\) |
Шаг 3: Построение графика \(\sigma\) от \(\ln C\).
На миллиметровой бумаге или в программе для построения графиков строим зависимость \(\sigma\) (по оси Y) от \(\ln C\) (по оси X). Точки должны лечь на кривую, которая в области низких концентраций может быть близка к прямой.
Для графического определения \(\left( \frac{d\sigma}{d\ln C} \right)_T\) при \(C_x = 0,03\) моль/л, что соответствует \(\ln C_x = \ln(0,03) = -3,507\), необходимо провести касательную к кривой в этой точке и найти тангенс угла наклона этой касательной.
Предположим, что мы построили график и провели касательную в точке \(\ln C = -3,507\). Для удобства расчета тангенса угла наклона, можно выбрать две точки на касательной, например, близкие к точке \(C_x\).
Давайте возьмем точки, окружающие \(C_x = 0,03\) моль/л, чтобы оценить наклон. Например, можно использовать метод конечных разностей, если график достаточно линеен в этой области. Или, что более точно, провести касательную.
Для упрощения, если график вблизи \(C_x = 0,03\) моль/л можно аппроксимировать прямой, мы можем взять две ближайшие точки и рассчитать наклон.
Возьмем точки:
- Точка 1: \(C_1 = 0,02\) моль/л, \(\ln C_1 = -3,912\), \(\sigma_1 = 70,3\) мН/м
- Точка 2: \(C_2 = 0,06\) моль/л, \(\ln C_2 = -2,813\), \(\sigma_2 = 65,9\) мН/м
Наклон \(\frac{\Delta\sigma}{\Delta\ln C}\) в этом интервале:
\[\frac{\Delta\sigma}{\Delta\ln C} = \frac{\sigma_2 - \sigma_1}{\ln C_2 - \ln C_1} = \frac{65,9 - 70,3}{-2,813 - (-3,912)} = \frac{-4,4}{1,099} \approx -4,004 \text{ мН/м}\]Если мы хотим быть более точными, мы должны построить график и провести касательную. Допустим, по графику мы определили, что наклон касательной в точке \(\ln C = -3,507\) составляет примерно \(-4,0\) мН/м.
Итак, \(\left( \frac{d\sigma}{d\ln C} \right)_T \approx -4,0\) мН/м.
Шаг 4: Расчет удельной поверхностной адсорбции \(\Gamma\).
Используем формулу Гиббса:
\[\Gamma = -\frac{1}{RT} \left( \frac{d\sigma}{d\ln C} \right)_T\]Подставляем значения:
- \(R = 8,314\) Дж/(моль·К)
- \(T = 288,15\) К
- \(\left( \frac{d\sigma}{d\ln C} \right)_T = -4,0\) мН/м = \(-4,0 \cdot 10^{-3}\) Н/м (поскольку 1 мН = 10-3 Н)
Единицы:
- \(\sigma\) в Н/м
- \(R\) в Дж/(моль·К) = Н·м/(моль·К)
- \(T\) в К
Тогда \(\Gamma\) будет в моль/м2.
\[\Gamma = -\frac{1}{8,314 \text{ Дж/(моль·К)} \cdot 288,15 \text{ К}} \cdot (-4,0 \cdot 10^{-3} \text{ Н/м})\] \[\Gamma = -\frac{1}{2396,9 \text{ Дж/моль}} \cdot (-4,0 \cdot 10^{-3} \text{ Н/м})\] \[\Gamma = \frac{4,0 \cdot 10^{-3} \text{ Н/м}}{2396,9 \text{ Н·м/моль}} = \frac{4,0 \cdot 10^{-3}}{2396,9} \text{ моль/м}^2\] \[\Gamma \approx 1,669 \cdot 10^{-6} \text{ моль/м}^2\]Переведем в ммоль/м2:
\[\Gamma = 1,669 \cdot 10^{-6} \text{ моль/м}^2 \cdot \frac{1000 \text{ ммоль}}{1 \text{ моль}}\] \[\Gamma = 1,669 \cdot 10^{-3} \text{ ммоль/м}^2\]Ответ:
Удельная поверхностная адсорбция \(\Gamma\) для пропилового спирта при концентрации 0,03 моль/л и температуре 15 °C составляет приблизительно \(1,669 \cdot 10^{-3}\) ммоль/м2.
Примечание для школьника:
Для выполнения этой задачи в тетради, вам нужно будет:
- Переписать условие задачи и данные для вашего варианта.
- Записать формулу Гиббса.
- Перевести температуру в Кельвины.
- Составить таблицу значений \(\sigma\) и \(\ln C\).
- На миллиметровой бумаге построить график зависимости \(\sigma\) от \(\ln C\).
- Найти на оси \(\ln C\) значение, соответствующее \(C_x = 0,03\) моль/л (\(\ln C_x = -3,507\)).
- В этой точке провести касательную к построенной кривой.
- Выбрать две удобные точки на касательной (например, \((x_1, y_1)\) и \((x_2, y_2)\)) и рассчитать наклон касательной как \(\frac{y_2 - y_1}{x_2 - x_1}\). Это и будет значение \(\left( \frac{d\sigma}{d\ln C} \right)_T\).
- Подставить все значения в формулу Гиббса и выполнить расчет, не забывая про единицы измерения.
- Записать окончательный ответ.
В данном решении значение \(\left( \frac{d\sigma}{d\ln C} \right)_T\) было оценено по ближайшим точкам, что является приближением. Более точный результат требует аккуратного графического построения и определения наклона касательной.