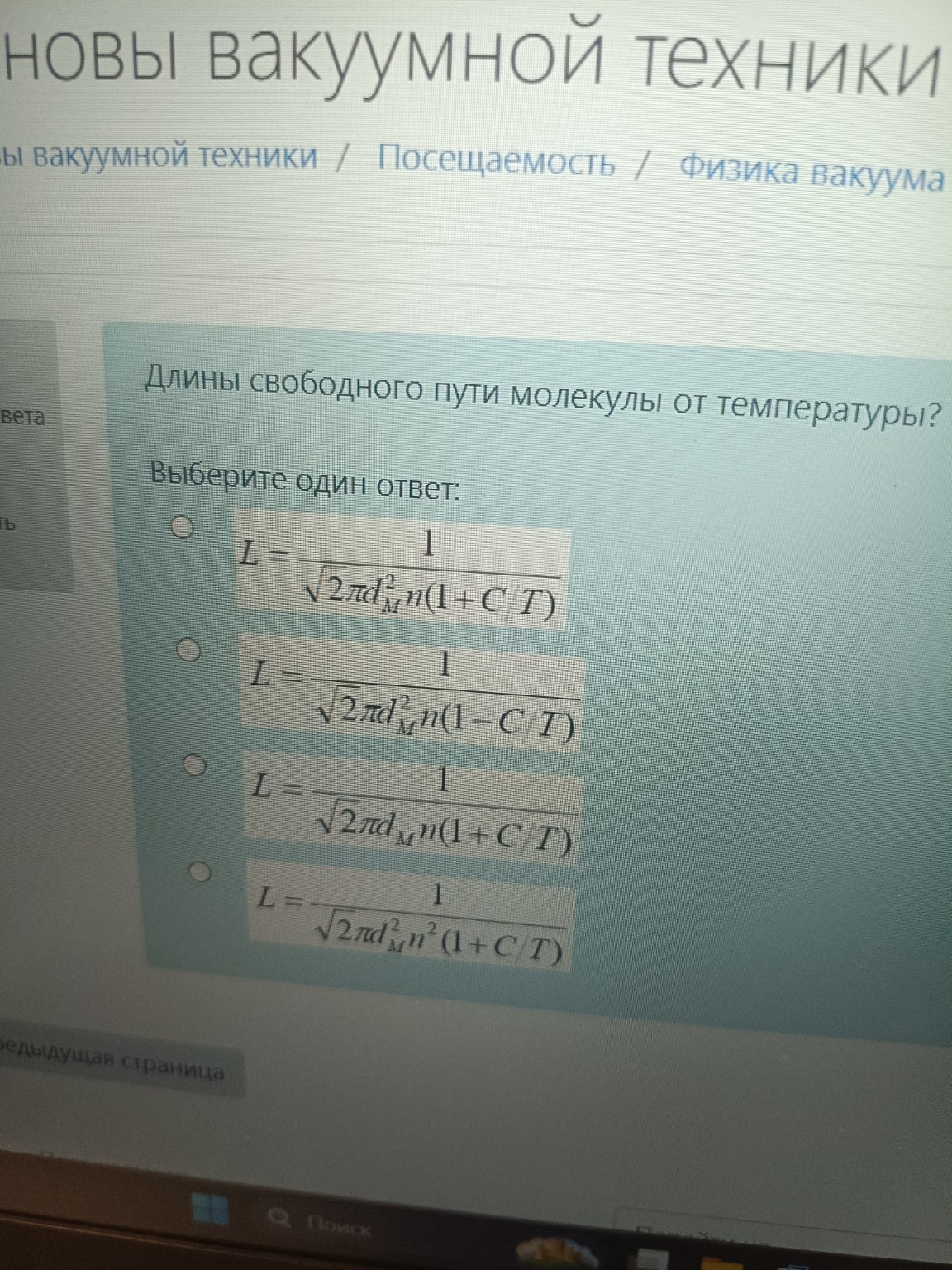
Вопрос: Длины свободного пути молекулы от температуры?
Выберите один ответ:
Правильный ответ:
\[L = \frac{1}{\sqrt{2}\pi d_M^2 n (1 + C/T)}\]
Пояснение:
Длина свободного пробега молекулы \(L\) — это среднее расстояние, которое молекула пролетает между двумя последовательными столкновениями с другими молекулами. Для идеального газа формула для длины свободного пробега обычно выглядит так:
\[L = \frac{1}{\sqrt{2}\pi d^2 n}\]где:
- \(d\) — эффективный диаметр молекулы;
- \(n\) — концентрация молекул (число молекул в единице объема).
Однако, в условиях, когда учитывается влияние температуры на эффективное сечение столкновения (например, для более точных моделей или при определенных условиях), может использоваться модифицированная формула, которая включает температурную зависимость. Один из таких подходов может быть связан с учетом сил притяжения между молекулами, которые становятся более значимыми при низких температурах. В этом случае эффективное сечение столкновения может зависеть от температуры.
Представленная в вариантах ответа формула с членом \((1 + C/T)\) в знаменателе является модификацией, которая учитывает температурную зависимость. Этот член \((1 + C/T)\) может быть связан с так называемым "фактором Сезерленда" или другими поправками, которые учитывают взаимодействие между молекулами, зависящее от температуры. Например, для вязкости газов часто используется формула Сезерленда, которая имеет похожую температурную зависимость.
В данном случае, из предложенных вариантов, наиболее полная и корректная формула, учитывающая температурную зависимость длины свободного пути, это:
\[L = \frac{1}{\sqrt{2}\pi d_M^2 n (1 + C/T)}\]где:
- \(L\) — длина свободного пробега;
- \(d_M\) — диаметр молекулы;
- \(n\) — концентрация молекул;
- \(C\) — некоторая постоянная, связанная с межмолекулярными взаимодействиями;
- \(T\) — абсолютная температура.
Эта формула показывает, что с ростом температуры (при прочих равных условиях) длина свободного пробега увеличивается, так как знаменатель уменьшается (член \(C/T\) становится меньше). Это может быть связано с тем, что при более высоких температурах молекулы движутся быстрее, и время взаимодействия между ними уменьшается, что может влиять на эффективное сечение столкновения.