schoolМатематика
verifiedРешено AI
Решение задачи: Закончите уравнения реакций горения (Al, Li, Ca)
help_outlineУсловие задачи
Реши задачу: Биология, 8 класс
lightbulbКраткий ответ
Решены уравнения реакций горения с алюминием, литием и кальцием с образованием оксидов. Также определены формулы оксидов хлора(VII), железа(III) и натрия.
Подробное решение
Хорошо, давайте решим эти задачи по химии.
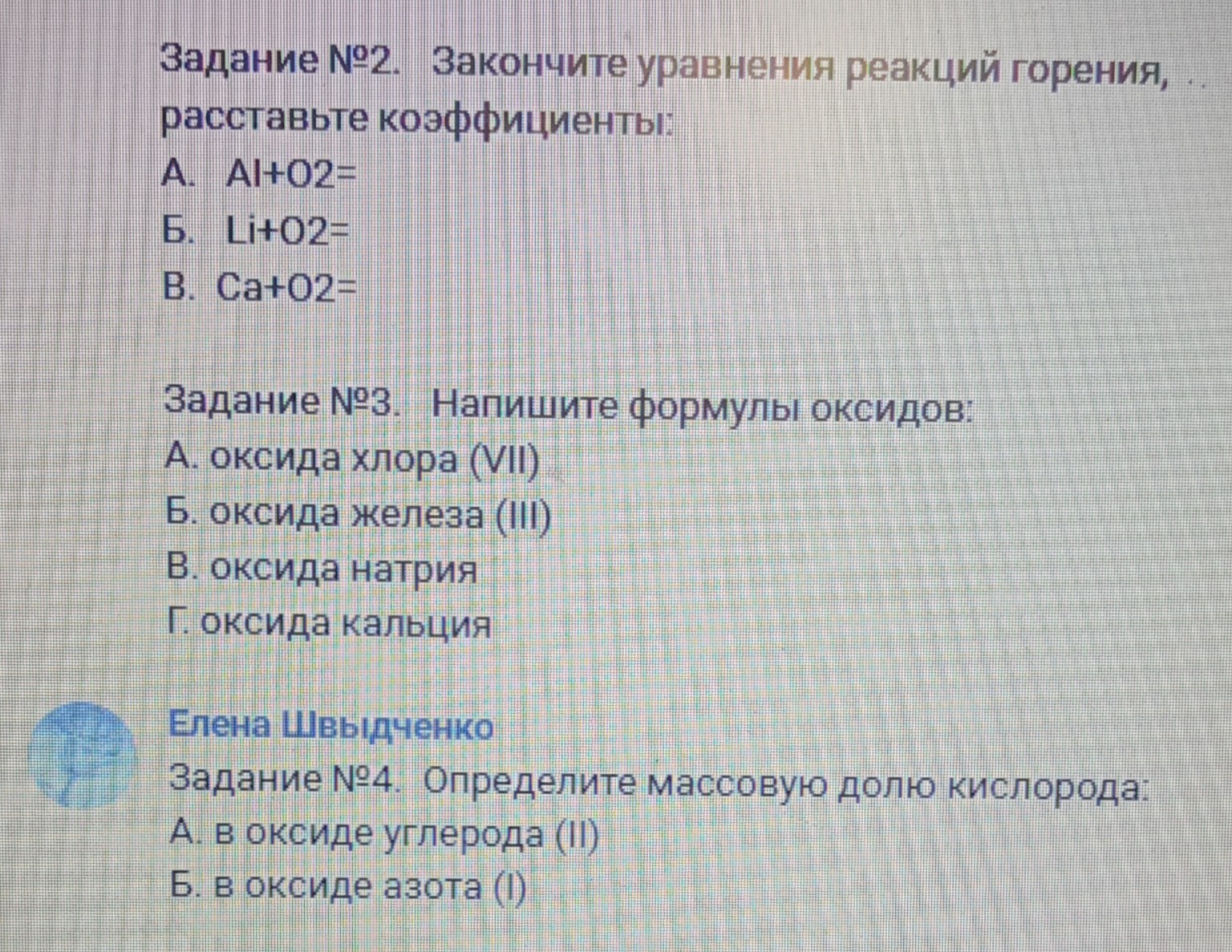
Задание №2. Закончите уравнения реакций горения, расставьте коэффициенты:
А. \( \text{Al} + \text{O}_2 = \)
Б. \( \text{Li} + \text{O}_2 = \)
В. \( \text{Ca} + \text{O}_2 = \)
Решение:
А. Алюминий реагирует с кислородом, образуя оксид алюминия \( \text{Al}_2\text{O}_3 \).
Уравнение реакции:
\( 4\text{Al} + 3\text{O}_2 = 2\text{Al}_2\text{O}_3 \)
Б. Литий реагирует с кислородом, образуя оксид лития \( \text{Li}_2\text{O} \).
Уравнение реакции:
\( 4\text{Li} + \text{O}_2 = 2\text{Li}_2\text{O} \)
В. Кальций реагирует с кислородом, образуя оксид кальция \( \text{CaO} \).
Уравнение реакции:
\( 2\text{Ca} + \text{O}_2 = 2\text{CaO} \)
Задание №3. Напишите формулы оксидов:
А. оксида хлора (VII)
Б. оксида железа (III)
В. оксида натрия
Г. оксида кальция
Решение:
А. Оксид хлора (VII). Хлор имеет степень окисления +7, кислород -2. Для составления формулы находим наименьшее общее кратное для модулей степеней окисления (7 и 2), это 14. Делим 14 на 7 (получаем 2 атома хлора) и 14 на 2 (получаем 7 атомов кислорода).
Формула: \( \text{Cl}_2\text{O}_7 \)
Б. Оксид железа (III). Железо имеет степень окисления +3, кислород -2. Наименьшее общее кратное для 3 и 2 - это 6. Делим 6 на 3 (получаем 2 атома железа) и 6 на 2 (получаем 3 атома кислорода).
Формула: \( \text{Fe}_2\text{O}_3 \)
В. Оксид натрия. Натрий - элемент первой группы, имеет степень окисления +1. Кислород -2. Наименьшее общее кратное для 1 и 2 - это 2. Делим 2 на 1 (получаем 2 атома натрия) и 2 на 2 (получаем 1 атом кислорода).
Формула: \( \text{Na}_2\text{O} \)
Г. Оксид кальция. Кальций - элемент второй группы, имеет степень окисления +2. Кислород -2. Наименьшее общее кратное для 2 и 2 - это 2. Делим 2 на 2 (получаем 1 атом кальция) и 2 на 2 (получаем 1 атом кислорода).
Формула: \( \text{CaO} \)
Задание №4. Определите массовую долю кислорода:
А. в оксиде углерода (II)
Б. в оксиде азота (I)
Решение:
Для определения массовой доли элемента в соединении используется формула:
\[ \omega(\text{элемента}) = \frac{n \cdot A_r(\text{элемента})}{M_r(\text{соединения})} \cdot 100\% \]
где \( n \) - число атомов элемента в формуле, \( A_r \) - относительная атомная масса элемента, \( M_r \) - относительная молекулярная масса соединения.
Относительные атомные массы (округляем до целых):
\( A_r(\text{C}) = 12 \)
\( A_r(\text{O}) = 16 \)
\( A_r(\text{N}) = 14 \)
А. В оксиде углерода (II).
Формула оксида углерода (II) - \( \text{CO} \).
Относительная молекулярная масса \( M_r(\text{CO}) = A_r(\text{C}) + A_r(\text{O}) = 12 + 16 = 28 \).
Массовая доля кислорода в \( \text{CO} \):
\[ \omega(\text{O}) = \frac{1 \cdot A_r(\text{O})}{M_r(\text{CO})} \cdot 100\% = \frac{1 \cdot 16}{28} \cdot 100\% \]
\[ \omega(\text{O}) = \frac{16}{28} \cdot 100\% \approx 0.5714 \cdot 100\% \approx 57.14\% \]
Ответ: Массовая доля кислорода в оксиде углерода (II) составляет примерно 57.14%.
Б. В оксиде азота (I).
Формула оксида азота (I) - \( \text{N}_2\text{O} \).
Относительная молекулярная масса \( M_r(\text{N}_2\text{O}) = 2 \cdot A_r(\text{N}) + A_r(\text{O}) = 2 \cdot 14 + 16 = 28 + 16 = 44 \).
Массовая доля кислорода в \( \text{N}_2\text{O} \):
\[ \omega(\text{O}) = \frac{1 \cdot A_r(\text{O})}{M_r(\text{N}_2\text{O})} \cdot 100\% = \frac{1 \cdot 16}{44} \cdot 100\% \]
\[ \omega(\text{O}) = \frac{16}{44} \cdot 100\% \approx 0.3636 \cdot 100\% \approx 36.36\% \]
Ответ: Массовая доля кислорода в оксиде азота (I) составляет примерно 36.36%.