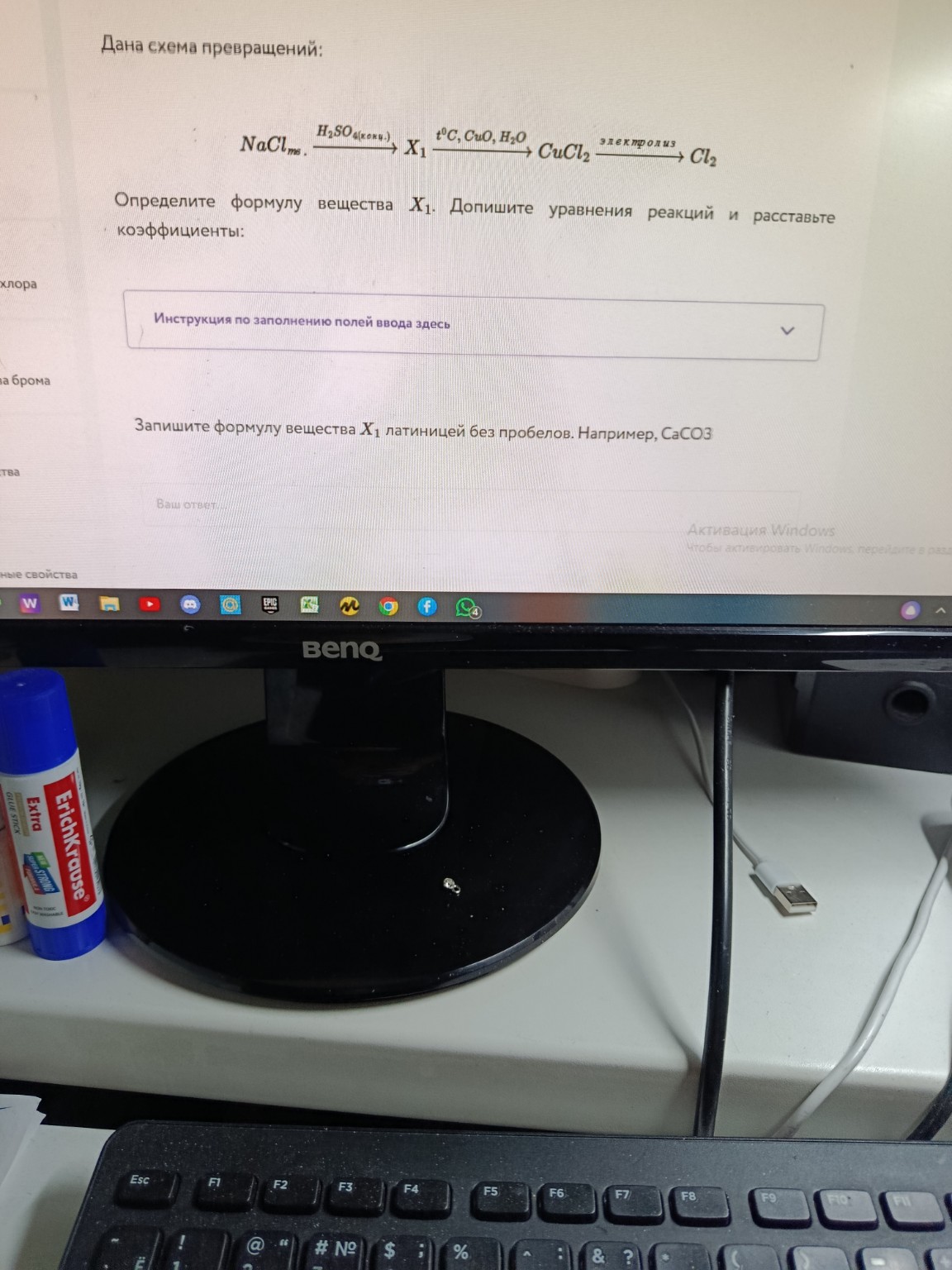
Задача: Дана схема превращений:
\[NaCl_{(тв.)} \xrightarrow{H_2SO_{4(конц.)}} X_1 \xrightarrow{t^\circ C, CuO, H_2O} CuCl_2 \xrightarrow{электролиз} Cl_2\]
Определите формулу вещества \(X_1\). Допишите уравнения реакций и расставьте коэффициенты:
Решение:
Рассмотрим каждое превращение по порядку, чтобы определить вещество \(X_1\) и дописать уравнения.
1. Превращение: \(NaCl_{(тв.)} \xrightarrow{H_2SO_{4(конц.)}} X_1\)
- Это реакция получения хлороводорода (\(HCl\)) из хлорида натрия (\(NaCl\)) и концентрированной серной кислоты (\(H_2SO_4\)).
- При нагревании твердого хлорида натрия с концентрированной серной кислотой образуется газообразный хлороводород и гидросульфат натрия (или сульфат натрия при более сильном нагревании).
- Уравнение реакции:
\[NaCl_{(тв.)} + H_2SO_{4(конц.)} \xrightarrow{t^\circ C} NaHSO_4 + HCl \uparrow\] - Таким образом, вещество \(X_1\) — это хлороводород (\(HCl\)).
Формула вещества \(X_1\): HCl
2. Превращение: \(X_1 \xrightarrow{t^\circ C, CuO, H_2O} CuCl_2\)
- Мы определили, что \(X_1\) — это \(HCl\).
- Для получения хлорида меди(II) (\(CuCl_2\)) из \(HCl\) с использованием оксида меди(II) (\(CuO\)) и воды (\(H_2O\)) при нагревании, происходит реакция между соляной кислотой (раствором \(HCl\) в воде) и оксидом меди(II).
- Уравнение реакции:
\[2HCl + CuO \xrightarrow{t^\circ C} CuCl_2 + H_2O\] - Здесь \(HCl\) реагирует как кислота с основным оксидом.
3. Превращение: \(CuCl_2 \xrightarrow{электролиз} Cl_2\)
- Это электролиз раствора хлорида меди(II) (\(CuCl_2\)).
- При электролизе водного раствора \(CuCl_2\) на аноде выделяется газообразный хлор (\(Cl_2\)), а на катоде — металлическая медь (\(Cu\)).
- Уравнение реакции:
\[CuCl_2 \xrightarrow{электролиз} Cu + Cl_2 \uparrow\]
Окончательные уравнения реакций с коэффициентами:
1. \[NaCl_{(тв.)} + H_2SO_{4(конц.)} \xrightarrow{t^\circ C} NaHSO_4 + HCl \uparrow\]
2. \[2HCl + CuO \xrightarrow{t^\circ C} CuCl_2 + H_2O\]
3. \[CuCl_2 \xrightarrow{электролиз} Cu + Cl_2 \uparrow\]
Ответ:
Формула вещества \(X_1\): HCl