schoolМатематика
verifiedРешено AI
Решение: Найти ΔH и ΔS методом Кайнора
help_outlineУсловие задачи
Реши задачу: Найди дельта H и дельта S через метод Кайнора, какая матрица получится?
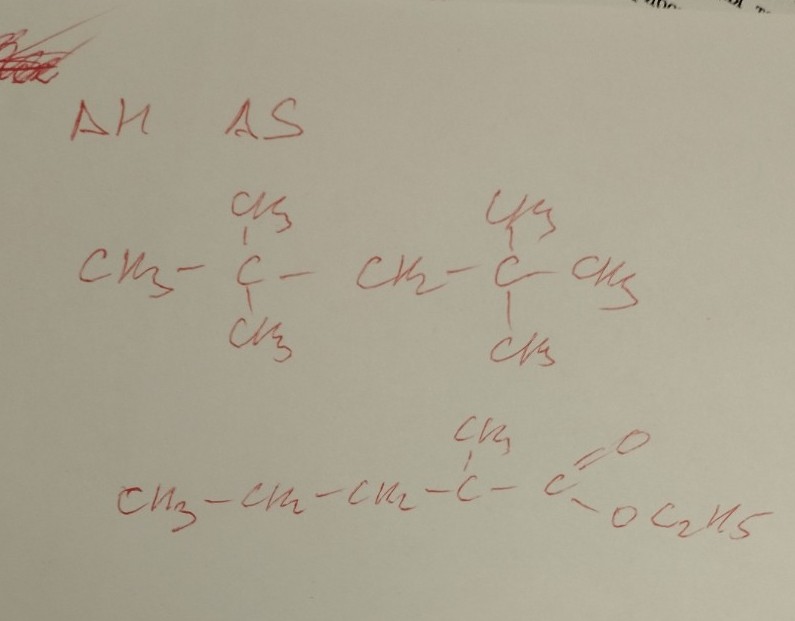
lightbulbКраткий ответ
Для расчета ΔH и ΔS методом Кайнора-Бенсона необходимо разбить молекулу на структурные группы и составить матрицу вкладов, учитывающую количество каждой группы. Пример для 2,2,4,4-тетраметилпентана представлен в решении.
Подробное решение
Для решения данной задачи по определению стандартной энтальпии образования \(\Delta H_{f}^{0}\) и стандартной энтропии \(S^{0}\) методом Бенсона (часто называемым методом групповых вкладов Кайнора-Бенсона), необходимо разбить молекулы на составляющие их структурные группы.
1. Анализ первого соединения (2,2,4,4-тетраметилпентан):
Структурная формула: \(CH_{3}-C(CH_{3})_{2}-CH_{2}-C(CH_{3})_{3}\)
Группы в молекуле:
- Шесть групп \(C-(C)(H)_{3}\) (концевые метильные группы).
- Две группы \(C-(C)_{4}\) (четвертичные атомы углерода).
- Одна группа \(C-(C)_{2}(H)_{2}\) (вторичный атом углерода в центре).
Матрица вкладов (количество групп):
\[
\begin{pmatrix}
Группа & Кол-во \\
C-(C)(H)_{3} & 6 \\
C-(C)_{4} & 2 \\
C-(C)_{2}(H)_{2} & 1
\end{pmatrix}
\]
Расчет \(\Delta H\) и \(S\) производится путем суммирования табличных значений для каждой группы:
\[ \Delta H_{total} = 6 \cdot \Delta H[C-(C)(H)_{3}] + 2 \cdot \Delta H[C-(C)_{4}] + 1 \cdot \Delta H[C-(C)_{2}(H)_{2}] \]
\[ S_{total} = 6 \cdot S[C-(C)(H)_{3}] + 2 \cdot S[C-(C)_{4}] + 1 \cdot S[C-(C)_{2}(H)_{2}] - R \ln(\sigma) \]
где \(\sigma\) — число симметрии молекулы.
2. Анализ второго соединения (этиловый эфир 2-метилпентановой кислоты):
Структурная формула: \(CH_{3}-CH_{2}-CH_{2}-CH(CH_{3})-CO-O-C_{2}H_{5}\)
Группы в молекуле:
- Три группы \(C-(C)(H)_{3}\) (метильные группы в цепи и радикале).
- Две группы \(C-(C)_{2}(H)_{2}\) (метиленовые группы в основной цепи).
- Одна группа \(C-(C)_{2}(H)(C=O)\) (третичный углерод, связанный с карбонилом).
- Одна группа \(C=O-(C)(O)\) (карбонильная группа сложного эфира).
- Одна группа \(O-(C=O)(C)\) (эфирный кислород).
- Одна группа \(C-(O)(C)(H)_{2}\) (метиленовая группа этильного радикала).
Матрица вкладов для второго соединения:
\[
\begin{pmatrix}
Группа & Кол-во \\
C-(C)(H)_{3} & 3 \\
C-(C)_{2}(H)_{2} & 2 \\
C-(C)_{2}(H)(C=O) & 1 \\
C=O-(C)(O) & 1 \\
O-(C=O)(C) & 1 \\
C-(O)(C)(H)_{2} & 1
\end{pmatrix}
\]
Итоговые значения \(\Delta H\) и \(\Delta S\) (изменение энтропии реакции образования) получаются подстановкой констант из справочника Бенсона в данные матрицы. Метод позволяет с высокой точностью предсказывать термодинамические свойства органических веществ, что крайне важно для развития отечественной химической промышленности и науки.