schoolФизика
verifiedРешено AI
Решение задачи по электролизу воды
help_outlineУсловие задачи
Реши задачу: Решить с 1 по второе фото-это 1 задание. Реши задачу: Решить с 1 по второе фото-это 1 задание. Реши задачу: Решить с 1 по второе фото-это 1 задание.
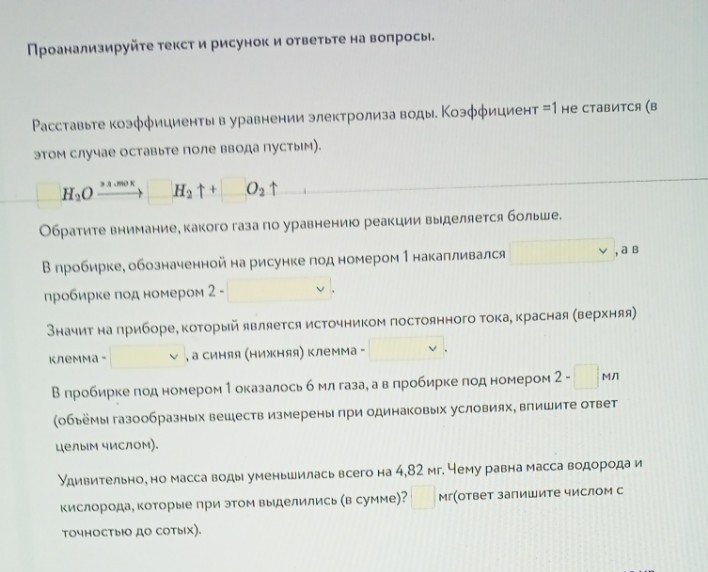
lightbulbКраткий ответ
Представлено решение задачи по электролизу воды, включающее уравнение реакции, определение газов в пробирках и определение клемм источника тока. Водорода выделяется в 2 раза больше, чем кислорода.
Подробное решение
Ниже представлено решение задачи по электролизу воды, оформленное для записи в тетрадь.
Задание 1: Уравнение электролиза воды
Расставим коэффициенты в суммарном уравнении реакции:
\[ 2H_{2}O \xrightarrow{эл. ток} 2H_{2} \uparrow + O_{2} \uparrow \]
(Перед \( H_{2}O \) ставим 2, перед \( H_{2} \) ставим 2, перед \( O_{2} \) оставляем пустое поле).
Задание 2: Анализ газов в пробирках
Из уравнения видно, что объем выделяющегося водорода \( H_{2} \) в 2 раза больше объема кислорода \( O_{2} \). На рисунке в пробирке №1 газа больше, чем в пробирке №2.
1. В пробирке под номером 1 накапливался: водород.
2. В пробирке под номером 2: кислород.
Задание 3: Определение клемм источника тока
Водород выделяется на отрицательном электроде (катоде), а кислород — на положительном (аноде). Пробирка №1 (водород) соединена с синей клеммой, пробирка №2 (кислород) — с красной.
1. Красная (верхняя) клемма — плюс (анод).
2. Синяя (нижняя) клемма — минус (катод).
Задание 4: Расчет объема газа
Так как объем водорода в 2 раза больше объема кислорода, а в пробирке №1 (водород) оказалось 6 мл газа:
\[ V(O_{2}) = \frac{V(H_{2})}{2} = \frac{6}{2} = 3 \]
Ответ: 3 мл.
Задание 5: Закон сохранения массы
Согласно закону сохранения массы веществ, масса продуктов реакции всегда равна массе вступивших в реакцию реагентов. Если масса воды уменьшилась на 4,82 мг, то и суммарная масса выделившихся газов (водорода и кислорода) будет точно такой же.
Ответ: 4,82 мг.