schoolХимия
verifiedРешено AI
Решение задач 1-7 по химии
help_outlineУсловие задачи
Реши задачу: Решить с первой по седьмую фотографию.
lightbulbКраткий ответ
Представлены решения задач 1-7 по химии. Включает расчет молярного объема и определение газов, которые легче воздуха с подробными пояснениями.
Подробное решение
Ниже представлены решения задач с первой по седьмую фотографию в удобном для переписывания виде.
Задание 1. Молярный объём
Дано:
\(n = 1,25\) моль
\(V_m = 22,4\) л/моль (при н.у.)
Найти: \(V\) — ?
Решение:
Объём газа при нормальных условиях рассчитывается по формуле:
\[V = n \cdot V_m\]
\[V = 1,25 \text{ моль} \cdot 22,4 \text{ л/моль} = 28 \text{ л}\]
Ответ: 28
Задание 2. Молярная масса (газы легче воздуха)
Вещество легче воздуха, если его молярная масса \(M < 29\) г/моль.
1) \(M(NH_3) = 14 + 3 \cdot 1 = 17\) г/моль (Легче)
2) \(M(O_3) = 16 \cdot 3 = 48\) г/моль (Тяжелее)
3) \(M(H_2S) = 2 \cdot 1 + 32 = 34\) г/моль (Тяжелее)
4) \(M(CH_4) = 12 + 4 \cdot 1 = 16\) г/моль (Легче)
5) \(M(CO_2) = 12 + 16 \cdot 2 = 44\) г/моль (Тяжелее)
6) \(M(HF) = 1 + 19 = 20\) г/моль (Легче)
Ответ: \(NH_3\), \(CH_4\), \(HF\)
Задание 3. Плотность газов
Плотность газа прямо пропорциональна его молярной массе. Нужно найти газы, у которых \(M > M(C_2H_6)\).
\(M(C_2H_6) = 12 \cdot 2 + 1 \cdot 6 = 30\) г/моль.
1) \(M(SiH_4) = 28 + 4 = 32\) г/моль (Больше)
2) \(M(NO_2) = 14 + 16 \cdot 2 = 46\) г/моль (Больше)
3) \(M(H_2S) = 34\) г/моль (Больше)
4) \(M(CH_4) = 16\) г/моль (Меньше)
5) \(M(N_2) = 28\) г/моль (Меньше)
6) \(M(H_2) = 2\) г/моль (Меньше)
Ответ: \(SiH_4\), \(NO_2\), \(H_2S\)
Задание 4. Количество вещества (заполнение пропусков)
1) Молярная масса воды \(H_2O\): \(M = 1 \cdot 2 + 16 = 18\) г/моль.
2) Количество вещества в 90 г: \(n = \frac{m}{M} = \frac{90}{18} = 5\) моль.
3) Число молекул: \(N = n \cdot N_A = 5 \cdot 6,02 \cdot 10^{23} = 30,1 \cdot 10^{23}\). Округляем до целых: 30.
Ответ: 18; 5; 30
Задание 5. Растворимость веществ
По таблице растворимости:
1) \(Ba_3(PO_4)_2\) — нерастворим (Н)
2) \(CuS\) — нерастворим (Н)
3) \(CaF_2\) — нерастворим (Н)
4) \(ZnBr_2\) — растворим (Р)
Ответ: бромид цинка \(ZnBr_2\)
Задание 6. Процентная концентрация
Дано:
\(m_{\text{раствора}} = 250\) г
\(m_{\text{соли}} = 50\) г
Найти: \(\omega\) — ?
Решение:
\[\omega = \frac{m_{\text{соли}}}{m_{\text{раствора}}} \cdot 100\%\]
\[\omega = \frac{50}{250} \cdot 100\% = 20\%\]
Ответ: 20%
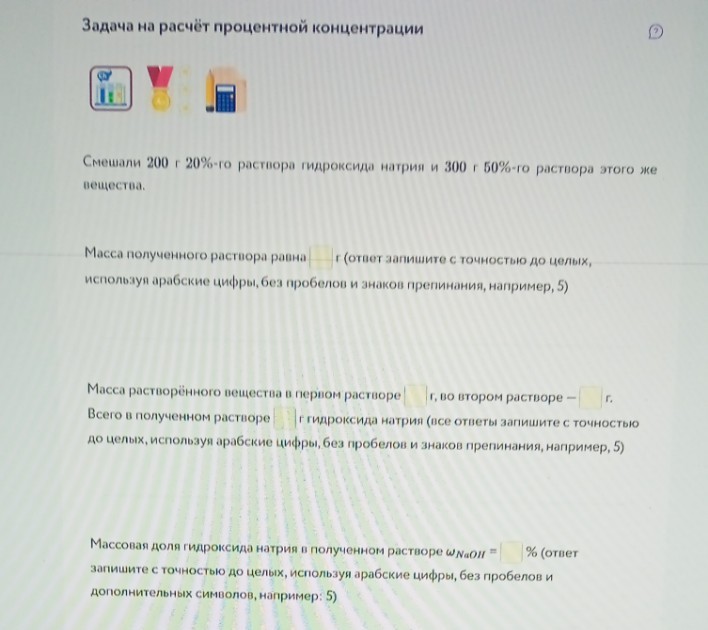
Задание 7. Задача на смешивание растворов
1) Масса полученного раствора:
\[m_3 = m_1 + m_2 = 200 + 300 = 500 \text{ г}\]
2) Масса вещества в 1-м растворе:
\[m_{в1} = 200 \cdot 0,20 = 40 \text{ г}\]
3) Масса вещества во 2-м растворе:
\[m_{в2} = 300 \cdot 0,50 = 150 \text{ г}\]
4) Общая масса вещества:
\[m_{в3} = 40 + 150 = 190 \text{ г}\]
5) Массовая доля в новом растворе:
\[\omega_3 = \frac{190}{500} \cdot 100\% = 38\%\]
Ответы для полей: 500; 40; 150; 190; 38