school
Общие знания
verified
Решено AI
Решение задачи Вариант 10 по химии
help_outline
Условие задачи
Вариант 10 Вариант 10 Вариант 10
lightbulb
Краткий ответ
Для решения задачи необходимо определить продукт реакции H2S и Cu(NO3)2, рассчитать заряд частиц золя и, исходя из этого, определить электролит с наименьшим порогом коагуляции, основываясь на правиле Шульце-Гарди.
Подробное решение
Хорошо, давайте решим задачу для варианта 10.
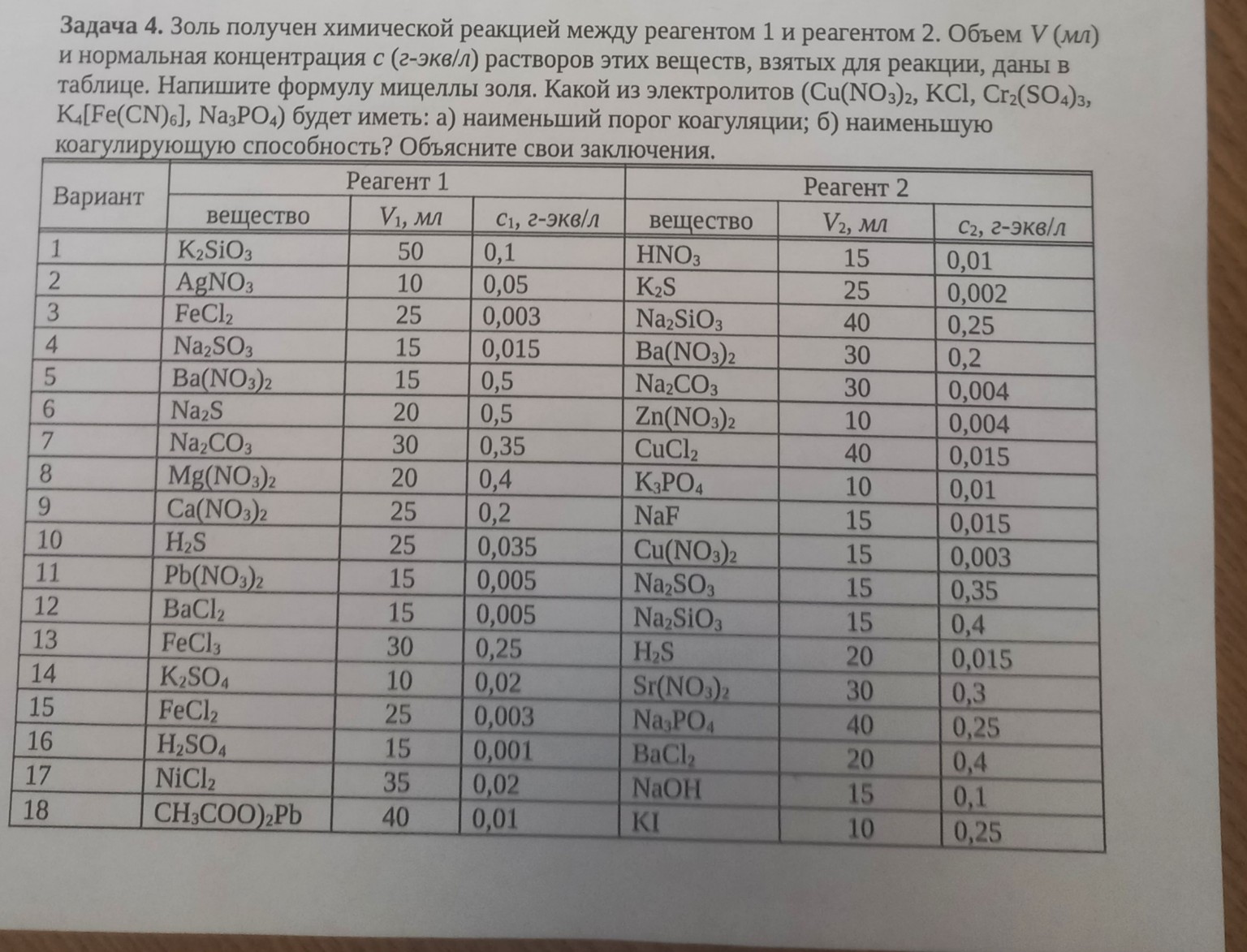
Задача 4. Золь получен химической реакцией между реагентом 1 и реагентом 2. Объем V (мл) и нормальная концентрация c (г-экв/л) растворов этих веществ, взятых для реакции, даны в таблице. Напишите формулу мицеллы золя. Какой из электролитов (\(\text{Cu(NO}_3)_2\), \(\text{KCl}\), \(\text{Cr}_2(\text{SO}_4)_3\), \(\text{K}_4[\text{Fe(CN)}_6]\), \(\text{Na}_3\text{PO}_4\)) будет иметь: а) наименьший порог коагуляции; б) наименьшую коагулирующую способность? Объясните свои заключения.
Таблица данных для варианта 10:
Реагент 1:
вещество: \(\text{H}_2\text{S}\)
\(V_1\), мл: 25
\(c_1\), г-экв/л: 0,035
Реагент 2:
вещество: \(\text{Cu(NO}_3)_2\)
\(V_2\), мл: 15
\(c_2\), г-экв/л: 0,003
Электролиты для сравнения: \(\text{Cu(NO}_3)_2\), \(\text{KCl}\), \(\text{Cr}_2(\text{SO}_4)_3\), \(\text{K}_4[\text{Fe(CN)}_6]\), \(\text{Na}_3\text{PO}_4\).
Часть 1: Напишите формулу мицеллы золя.
1. Определим, какой реагент взят в избытке. Для этого рассчитаем количество эквивалентов каждого реагента.
Количество эквивалентов \(N = c \cdot V\), где \(c\) - нормальная концентрация (г-экв/л), \(V\) - объем (л).
Переведем объемы из мл в л:
\(V_1 = 25 \text{ мл} = 0,025 \text{ л}\)
\(V_2 = 15 \text{ мл} = 0,015 \text{ л}\)
Количество эквивалентов \(\text{H}_2\text{S}\):
\(N_1 = 0,035 \text{ г-экв/л} \cdot 0,025 \text{ л} = 0,000875 \text{ г-экв}\)
Количество эквивалентов \(\text{Cu(NO}_3)_2\):
\(N_2 = 0,003 \text{ г-экв/л} \cdot 0,015 \text{ л} = 0,000045 \text{ г-экв}\)
Сравним количества эквивалентов: \(N_1 > N_2\).
Значит, \(\text{H}_2\text{S}\) взят в избытке.
2. Напишем уравнение реакции образования золя:
\(\text{Cu(NO}_3)_2 + \text{H}_2\text{S} \rightarrow \text{CuS} \downarrow + 2\text{HNO}_3\)
Продукт реакции, образующий ядро золя, - это \(\text{CuS}\) (сульфид меди(II)), который является нерастворимым осадком.
3. Определим потенциалопределяющие ионы.
Поскольку \(\text{H}_2\text{S}\) взят в избытке, в растворе после реакции останутся ионы, образующиеся при диссоциации \(\text{H}_2\text{S}\).
\(\text{H}_2\text{S} \rightleftharpoons \text{H}^+ + \text{HS}^-\)
\(\text{HS}^- \rightleftharpoons \text{H}^+ + \text{S}^{2-}\)
Ионы \(\text{S}^{2-}\) (или \(\text{HS}^-\)) являются общими с осадком \(\text{CuS}\) и будут адсорбироваться на его поверхности, образуя потенциалопределяющий слой. Таким образом, ядро золя будет заряжено отрицательно.
4. Определим противоионы.
Противоионами будут ионы, оставшиеся в растворе из реагента, который был в недостатке, и избыточного реагента, но с противоположным зарядом.
Из \(\text{Cu(NO}_3)_2\) в растворе остаются ионы \(\text{NO}_3^-\) (они не участвуют в образовании ядра и потенциалопределяющего слоя).
Из \(\text{H}_2\text{S}\) в растворе остаются ионы \(\text{H}^+\).
Так как потенциалопределяющий слой отрицательный (\(\text{S}^{2-}\)), противоионами будут положительно заряженные ионы. В данном случае это \(\text{H}^+\) из избытка \(\text{H}_2\text{S}\) и \(\text{Cu}^{2+}\) из \(\text{Cu(NO}_3)_2\) (но \(\text{Cu}^{2+}\) почти полностью прореагировали, поэтому их мало). Основными противоионами будут \(\text{H}^+\).
5. Напишем формулу мицеллы золя:
Ядро: \((\text{CuS})_n\)
Потенциалопределяющий слой: \(m\text{S}^{2-}\) (или \(m\text{HS}^-\))
Адсорбционный слой: \(m\text{S}^{2-} \cdot x\text{H}^+\)
Диффузный слой: \((m-x)\text{H}^+\)
Полная формула мицеллы:
\[ \{ (\text{CuS})_n \cdot m\text{S}^{2-} \cdot x\text{H}^+ \} ^{(2m-x)-} \cdot (m-x)\text{H}^+ \]
Или, более упрощенно, с указанием заряда ядра и противоионов:
\[ \{ (\text{CuS})_n \cdot m\text{S}^{2-} \} ^{2m-} \cdot 2m\text{H}^+ \]
(где \(x\) - количество ионов \(\text{H}^+\) в адсорбционном слое, а \((m-x)\) - в диффузном слое).
Таким образом, золь \(\text{CuS}\) будет отрицательно заряженным.
Часть 2: Какой из электролитов будет иметь: а) наименьший порог коагуляции; б) наименьшую коагулирующую способность? Объясните свои заключения.
Золь \(\text{CuS}\) отрицательно заряжен. Для коагуляции отрицательно заряженного золя необходимы положительно заряженные ионы (катионы). Чем выше заряд коагулирующего иона, тем сильнее его коагулирующая способность и тем меньше его порог коагуляции (правило Шульце-Гарди).
Рассмотрим предложенные электролиты и их катионы:
1. \(\text{Cu(NO}_3)_2\): Катион \(\text{Cu}^{2+}\) (заряд +2)
2. \(\text{KCl}\): Катион \(\text{K}^+\) (заряд +1)
3. \(\text{Cr}_2(\text{SO}_4)_3\): Катион \(\text{Cr}^{3+}\) (заряд +3)
4. \(\text{K}_4[\text{Fe(CN)}_6]\): Катион \(\text{K}^+\) (заряд +1)
5. \(\text{Na}_3\text{PO}_4\): Катион \(\text{Na}^+\) (заряд +1)
Сравним заряды катионов:
\(\text{K}^+\) (из \(\text{KCl}\) и \(\text{K}_4[\text{Fe(CN)}_6]\)): +1
\(\text{Na}^+\) (из \(\text{Na}_3\text{PO}_4\)): +1
\(\text{Cu}^{2+}\) (из \(\text{Cu(NO}_3)_2\)): +2
\(\text{Cr}^{3+}\) (из \(\text{Cr}_2(\text{SO}_4)_3\)): +3
а) Наименьший порог коагуляции:
Наименьший порог коагуляции будет у электролита, который имеет наибольшую коагулирующую способность. Согласно правилу Шульце-Гарди, это электролит с катионом, имеющим наибольший заряд.
В нашем случае это \(\text{Cr}^{3+}\) из \(\text{Cr}_2(\text{SO}_4)_3\).
Следовательно, \(\text{Cr}_2(\text{SO}_4)_3\) будет иметь наименьший порог коагуляции.
б) Наименьшая коагулирующая способность:
Наименьшая коагулирующая способность будет у электролита, который имеет наименьший заряд катиона.
В нашем случае это \(\text{K}^+\) (из \(\text{KCl}\) и \(\text{K}_4[\text{Fe(CN)}_6]\)) и \(\text{Na}^+\) (из \(\text{Na}_3\text{PO}_4\)), все они имеют заряд +1.
Следовательно, \(\text{KCl}\), \(\text{K}_4[\text{Fe(CN)}_6]\) и \(\text{Na}_3\text{PO}_4\) будут иметь наименьшую коагулирующую способность. Среди них нет различий по заряду катиона, поэтому их коагулирующая способность будет примерно одинаковой и наименьшей.
Объяснение:
Правило Шульце-Гарди гласит, что коагулирующая способность иона-коагулянта тем выше, чем больше его заряд. Соответственно, чем выше коагулирующая способность, тем меньшая концентрация этого иона (т.е. меньший порог коагуляции) требуется для осаждения золя. Для отрицательно заряженного золя коагулянтами являются катионы.
Запишем решение в тетрадь:
Решение задачи для варианта 10.
Дано:
Реагент 1: \(\text{H}_2\text{S}\), \(V_1 = 25 \text{ мл}\), \(c_1 = 0,035 \text{ г-экв/л}\)
Реагент 2: \(\text{Cu(NO}_3)_2\), \(V_2 = 15 \text{ мл}\), \(c_2 = 0,003 \text{ г-экв/л}\)
Электролиты для сравнения: \(\text{Cu(NO}_3)_2\), \(\text{KCl}\), \(\text{Cr}_2(\text{SO}_4)_3\), \(\text{K}_4[\text{Fe(CN)}_6]\), \(\text{Na}_3\text{PO}_4\).
Часть 1: Формула мицеллы золя.
1. Определим, какой реагент взят в избытке.
Переведем объемы в литры: \(V_1 = 0,025 \text{ л}\), \(V_2 = 0,015 \text{ л}\).
Количество эквивалентов \(\text{H}_2\text{S}\): \(N_1 = c_1 \cdot V_1 = 0,035 \cdot 0,025 = 0,000875 \text{ г-экв}\).
Количество эквивалентов \(\text{Cu(NO}_3)_2\): \(N_2 = c_2 \cdot V_2 = 0,003 \cdot 0,015 = 0,000045 \text{ г-экв}\).
Так как \(N_1 > N_2\), \(\text{H}_2\text{S}\) взят в избытке.
2. Уравнение реакции:
\(\text{Cu(NO}_3)_2 + \text{H}_2\text{S} \rightarrow \text{CuS} \downarrow + 2\text{HNO}_3\)
Ядро золя образует нерастворимый осадок \(\text{CuS}\).
3. Определим потенциалопределяющие ионы.
Избыточный реагент \(\text{H}_2\text{S}\) диссоциирует, образуя ионы \(\text{S}^{2-}\) (или \(\text{HS}^-\)). Эти ионы являются общими с веществом ядра \(\text{CuS}\) и адсорбируются на его поверхности, придавая ядру отрицательный заряд.
Следовательно, золь \(\text{CuS}\) является отрицательно заряженным.
4. Определим противоионы.
Противоионами будут положительно заряженные ионы, оставшиеся в растворе. В данном случае это ионы \(\text{H}^+\) из избытка \(\text{H}_2\text{S}\).
5. Формула мицеллы золя:
\[ \{ (\text{CuS})_n \cdot m\text{S}^{2-} \cdot x\text{H}^+ \} ^{(2m-x)-} \cdot (m-x)\text{H}^+ \]
где \(n\) - число молекул \(\text{CuS}\) в ядре, \(m\) - число адсорбированных ионов \(\text{S}^{2-}\), \(x\) - число ионов \(\text{H}^+\) в адсорбционном слое.
Часть 2: Сравнение коагулирующей способности электролитов.
1. Определим заряд золя: Золь \(\text{CuS}\) отрицательно заряжен.
2. Согласно правилу Шульце-Гарди, для коагуляции отрицательно заряженного золя необходимы катионы. Чем выше заряд катиона, тем сильнее его коагулирующая способность и тем меньше его порог коагуляции.
3. Рассмотрим катионы и их заряды для предложенных электролитов:
* \(\text{Cu(NO}_3)_2\): катион \(\text{Cu}^{2+}\) (заряд +2)
* \(\text{KCl}\): катион \(\text{K}^+\) (заряд +1)
* \(\text{Cr}_2(\text{SO}_4)_3\): катион \(\text{Cr}^{3+}\) (заряд +3)
* \(\text{K}_4[\text{Fe(CN)}_6]\): катион \(\text{K}^+\) (заряд +1)
* \(\text{Na}_3\text{PO}_4\): катион \(\text{Na}^+\) (заряд +1)
а) Наименьший порог коагуляции:
Наименьший порог коагуляции будет у электролита с катионом, имеющим наибольший заряд. Это \(\text{Cr}^{3+}\) (заряд +3) из \(\text{Cr}_2(\text{SO}_4)_3\).
Заключение: \(\text{Cr}_2(\text{SO}_4)_3\) будет иметь наименьший порог коагуляции.
б) Наименьшая коагулирующая способность:
Наименьшая коагулирующая способность будет у электролитов с катионами, имеющими наименьший заряд. Это \(\text{K}^+\) (заряд +1) из \(\text{KCl}\) и \(\text{K}_4[\text{Fe(CN)}_6]\), а также \(\text{Na}^+\) (заряд +1) из \(\text{Na}_3\text{PO}_4\).
Заключение: \(\text{KCl}\), \(\text{K}_4[\text{Fe(CN)}_6]\) и \(\text{Na}_3\text{PO}_4\) будут иметь наименьшую коагулирующую способность.
Объяснение: Правило Шульце-Гарди утверждает, что коагулирующая способность иона-коагулянта прямо пропорциональна его заряду. Чем выше заряд иона, тем эффективнее он нейтрализует заряд коллоидной частицы и вызывает ее коагуляцию, что приводит к снижению необходимой концентрации коагулянта (порога коагуляции).