schoolФизика
verifiedРешено AI
Решение задачи: Моляльная концентрация раствора MgSO4
help_outlineУсловие задачи
lightbulbКраткий ответ
Для приготовления раствора необходимо рассчитать массу воды, используя молярные массы компонентов и заданную моляльную концентрацию раствора MgSO4. Правильный ответ будет найден после расчета.
Подробное решение
Решим задачу по химии.
Задача:
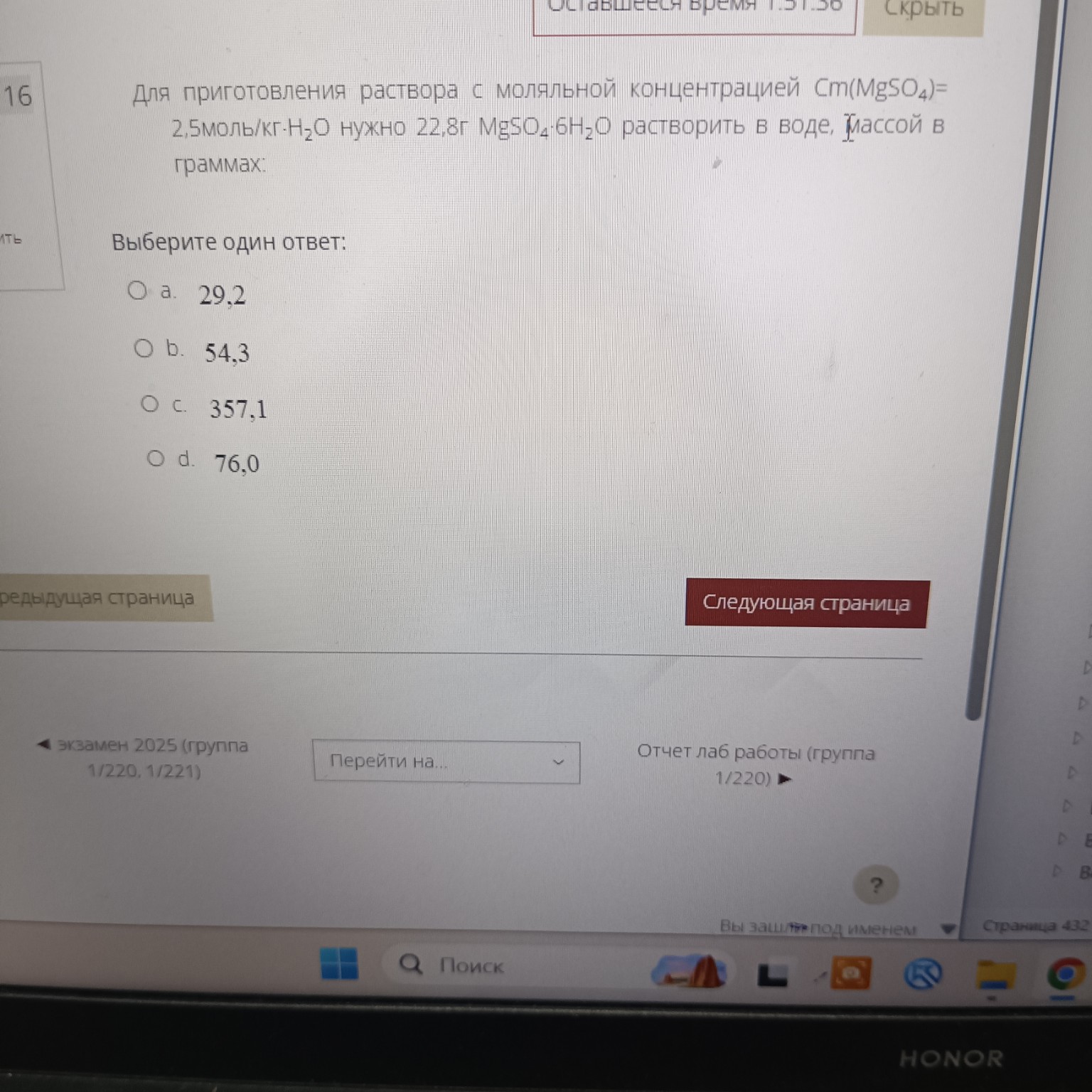
Для приготовления раствора с моляльной концентрацией \(C_m(\text{MgSO}_4) = 2,5 \text{ моль/кг}\cdot\text{H}_2\text{O}\) нужно 22,8 г \(\text{MgSO}_4 \cdot 6\text{H}_2\text{O}\) растворить в воде. Масса воды в граммах:
Варианты ответов:
а. 29,2
б. 54,3
в. 357,1
г. 76,0
Решение:
1. Определим молярную массу гидрата сульфата магния \(\text{MgSO}_4 \cdot 6\text{H}_2\text{O}\).
Молярная масса \(\text{Mg}\) = 24,3 г/моль
Молярная масса \(\text{S}\) = 32,1 г/моль
Молярная масса \(\text{O}\) = 16,0 г/моль
Молярная масса \(\text{H}\) = 1,0 г/моль
Молярная масса \(\text{MgSO}_4 = 24,3 + 32,1 + 4 \cdot 16,0 = 24,3 + 32,1 + 64,0 = 120,4 \text{ г/моль}\).
Молярная масса \(\text{H}_2\text{O} = 2 \cdot 1,0 + 16,0 = 18,0 \text{ г/моль}\).
Молярная масса \(\text{MgSO}_4 \cdot 6\text{H}_2\text{O} = 120,4 + 6 \cdot 18,0 = 120,4 + 108,0 = 228,4 \text{ г/моль}\).
Для удобства расчетов, округлим до 228 г/моль, так как в условии дано 22,8 г, что является 0,1 моль.
2. Найдем количество вещества \(\text{MgSO}_4 \cdot 6\text{H}_2\text{O}\).
Масса гидрата \(m(\text{MgSO}_4 \cdot 6\text{H}_2\text{O}) = 22,8 \text{ г}\).
Количество вещества \(n = \frac{m}{M}\).
\[n(\text{MgSO}_4 \cdot 6\text{H}_2\text{O}) = \frac{22,8 \text{ г}}{228,4 \text{ г/моль}} \approx 0,1 \text{ моль}\]
(Если использовать округленную молярную массу 228 г/моль, то \(n = \frac{22,8}{228} = 0,1 \text{ моль}\)).
3. При растворении гидрата \(\text{MgSO}_4 \cdot 6\text{H}_2\text{O}\) в воде, в раствор переходит 0,1 моль \(\text{MgSO}_4\).
Также, 6 моль воды из гидрата становятся частью растворителя.
Масса воды, которая содержится в 0,1 моль гидрата:
\[m(\text{H}_2\text{O} \text{ из гидрата}) = n(\text{MgSO}_4 \cdot 6\text{H}_2\text{O}) \cdot 6 \cdot M(\text{H}_2\text{O}) = 0,1 \text{ моль} \cdot 6 \cdot 18,0 \text{ г/моль} = 10,8 \text{ г}\]
4. Моляльная концентрация \(C_m\) определяется как количество вещества растворенного вещества на массу растворителя (воды) в килограммах.
\[C_m = \frac{n(\text{растворенного вещества})}{m(\text{растворителя, кг})}\]
Нам дана моляльная концентрация \(C_m(\text{MgSO}_4) = 2,5 \text{ моль/кг}\).
Количество вещества \(\text{MgSO}_4\) в растворе равно 0,1 моль.
Значит, масса растворителя (воды), которая должна быть в растворе, чтобы получить такую концентрацию:
\[m(\text{растворителя, кг}) = \frac{n(\text{MgSO}_4)}{C_m(\text{MgSO}_4)} = \frac{0,1 \text{ моль}}{2,5 \text{ моль/кг}} = 0,04 \text{ кг}\]
Переведем в граммы:
\[m(\text{растворителя}) = 0,04 \text{ кг} \cdot 1000 \text{ г/кг} = 40 \text{ г}\]
5. Эта масса (40 г) - это общая масса воды, которая должна быть в растворе. Однако, часть этой воды уже содержится в гидрате (10,8 г).
Следовательно, нужно добавить дополнительную массу воды:
\[m(\text{дополнительной воды}) = m(\text{общей воды}) - m(\text{воды из гидрата})\]
\[m(\text{дополнительной воды}) = 40 \text{ г} - 10,8 \text{ г} = 29,2 \text{ г}\]
Таким образом, нужно добавить 29,2 г воды.
Сравним с вариантами ответов:
а. 29,2
б. 54,3
в. 357,1
г. 76,0
Правильный ответ: а. 29,2
Ответ:
а. 29,2