schoolХимия
verifiedРешено AI
Решение задачи по химии: окислительно-восстановительная реакция KCrO2 и Br2
help_outlineУсловие задачи
lightbulbКраткий ответ
В данной задаче KCrO2 выступает восстановителем, а Br2 - окислителем. В результате реакции цвет раствора изменяется с зеленого на желтый из-за образования хромата.
Подробное решение
Хорошо, давайте решим эту задачу по химии.
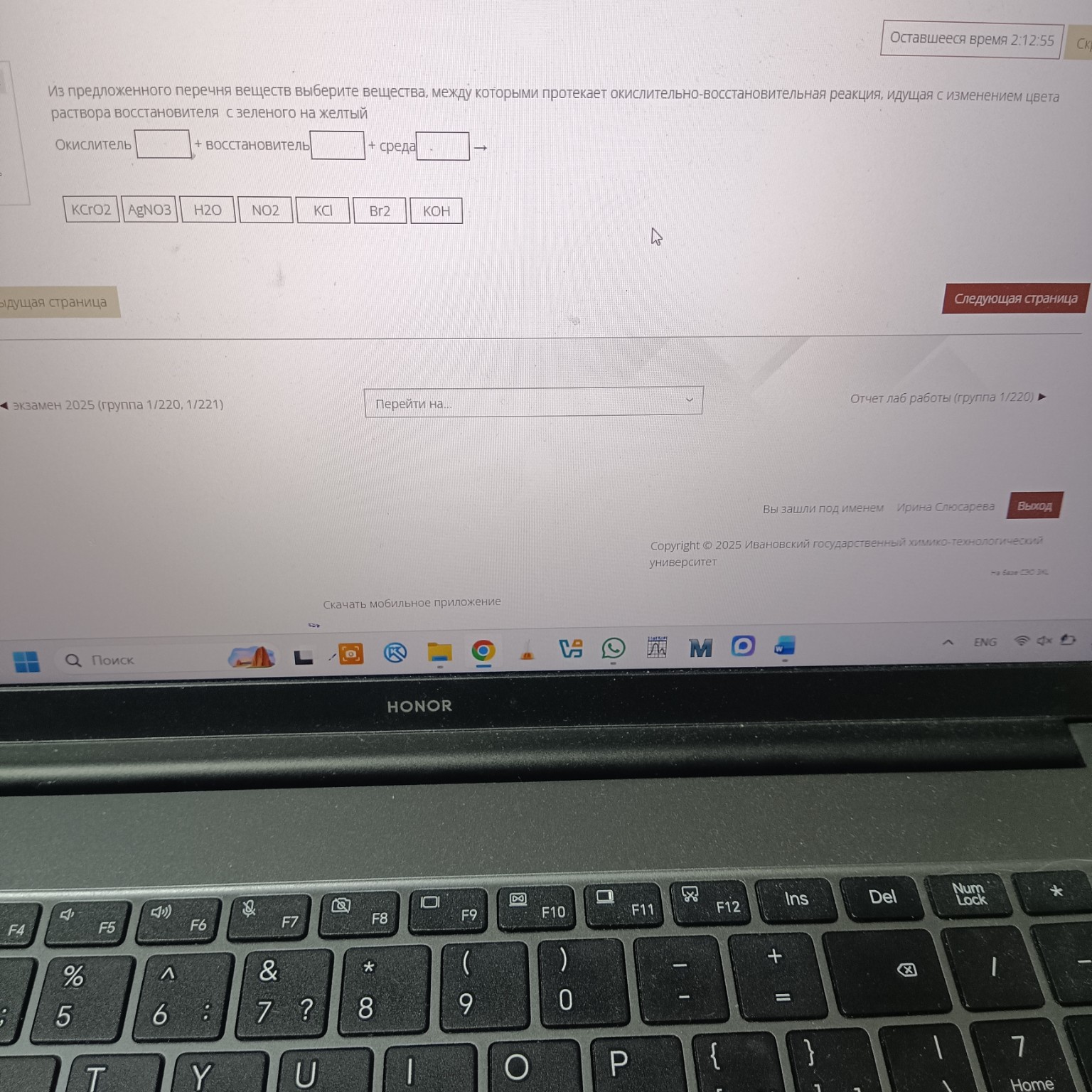
Задача: Из предложенного перечня веществ выберите вещества, между которыми протекает окислительно-восстановительная реакция, идущая с изменением цвета раствора восстановителя с зеленого на желтый.
Предложенные вещества: KCrO2, AgNO3, H2O, NO2, KCl, Br2, KOH.
Нам нужно найти окислитель, восстановитель и среду, чтобы цвет раствора восстановителя изменился с зеленого на желтый.
Раствор зеленого цвета, который может быть восстановителем и менять цвет на желтый, указывает на соединения хрома(III). Хром(III) имеет зеленый цвет, а хром(VI) (например, хроматы) имеет желтый цвет. Значит, восстановитель должен содержать хром(III) и окисляться до хрома(VI).
Из предложенных веществ соединение хрома(III) - это KCrO2 (хромит калия). В этом соединении хром имеет степень окисления +3.
Теперь нам нужно найти окислитель, который сможет окислить хром из +3 до +6.
Рассмотрим предложенные вещества:
* AgNO3 (нитрат серебра) - серебро в степени окисления +1, может быть окислителем.
* H2O (вода) - обычно не является сильным окислителем в таких реакциях.
* NO2 (диоксид азота) - азот в степени окисления +4, может быть как окислителем, так и восстановителем.
* KCl (хлорид калия) - хлор в степени окисления -1, калий в +1, не является окислителем.
* Br2 (бром) - бром в степени окисления 0, является сильным окислителем.
* KOH (гидроксид калия) - сильное основание, создает щелочную среду.
Для окисления хрома(III) до хрома(VI) обычно требуется сильный окислитель и щелочная среда.
Из предложенных окислителей, бром (Br2) является достаточно сильным.
Щелочную среду обеспечит KOH.
Итак, предполагаемая реакция:
Окислитель: Br2
Восстановитель: KCrO2
Среда: KOH
Запишем уравнение реакции в щелочной среде:
KCrO2 + Br2 + KOH → K2CrO4 + KBr + H2O
Теперь уравняем реакцию методом электронного баланса.
1. Определим степени окисления элементов, которые меняются:
В KCrO2: K (+1), O (-2), Cr (+3)
В Br2: Br (0)
В K2CrO4: K (+1), O (-2), Cr (+6)
В KBr: K (+1), Br (-1)
2. Составим полуреакции окисления и восстановления:
Окисление: Cr+3 - 3e- → Cr+6
Восстановление: Br20 + 2e- → 2Br-1
3. Найдем наименьшее общее кратное для числа отданных и принятых электронов (3 и 2), это 6.
Для окисления: (Cr+3 - 3e- → Cr+6) * 2
Для восстановления: (Br20 + 2e- → 2Br-1) * 3
Получаем:
2Cr+3 - 6e- → 2Cr+6
3Br20 + 6e- → 6Br-1
4. Суммируем полуреакции и добавим ионы среды (OH-) и воду (H2O) для баланса атомов кислорода и водорода.
В щелочной среде:
2CrO2- + 8OH- - 6e- → 2CrO42- + 4H2O
3Br2 + 6e- → 6Br-
Суммируем:
2CrO2- + 3Br2 + 8OH- → 2CrO42- + 6Br- + 4H2O
5. Добавим ионы калия (K+) для получения молекулярного уравнения:
2KCrO2 + 3Br2 + 8KOH → 2K2CrO4 + 6KBr + 4H2O
Проверим баланс атомов:
K: 2 + 8 = 10 (слева); 2*2 + 6 = 10 (справа) - сбалансировано
Cr: 2 (слева); 2 (справа) - сбалансировано
O: 2*2 + 8 = 12 (слева); 2*4 + 4 = 12 (справа) - сбалансировано
Br: 3*2 = 6 (слева); 6 (справа) - сбалансировано
H: 8 (слева); 4*2 = 8 (справа) - сбалансировано
Все сбалансировано.
Таким образом, вещества, которые нужно выбрать:
Окислитель: Br2
Восстановитель: KCrO2
Среда: KOH
Цвет раствора восстановителя (KCrO2) изменится с зеленого (Cr+3) на желтый (K2CrO4, Cr+6).
Ответы для записи в тетрадь:
1. Окислитель: Br2
2. Восстановитель: KCrO2
3. Среда: KOH
Уравнение реакции:
\[2KCrO_2 + 3Br_2 + 8KOH \rightarrow 2K_2CrO_4 + 6KBr + 4H_2O\]