schoolХимия
verifiedРешено AI
Решение задачи по химии: ОВР с выделением газа
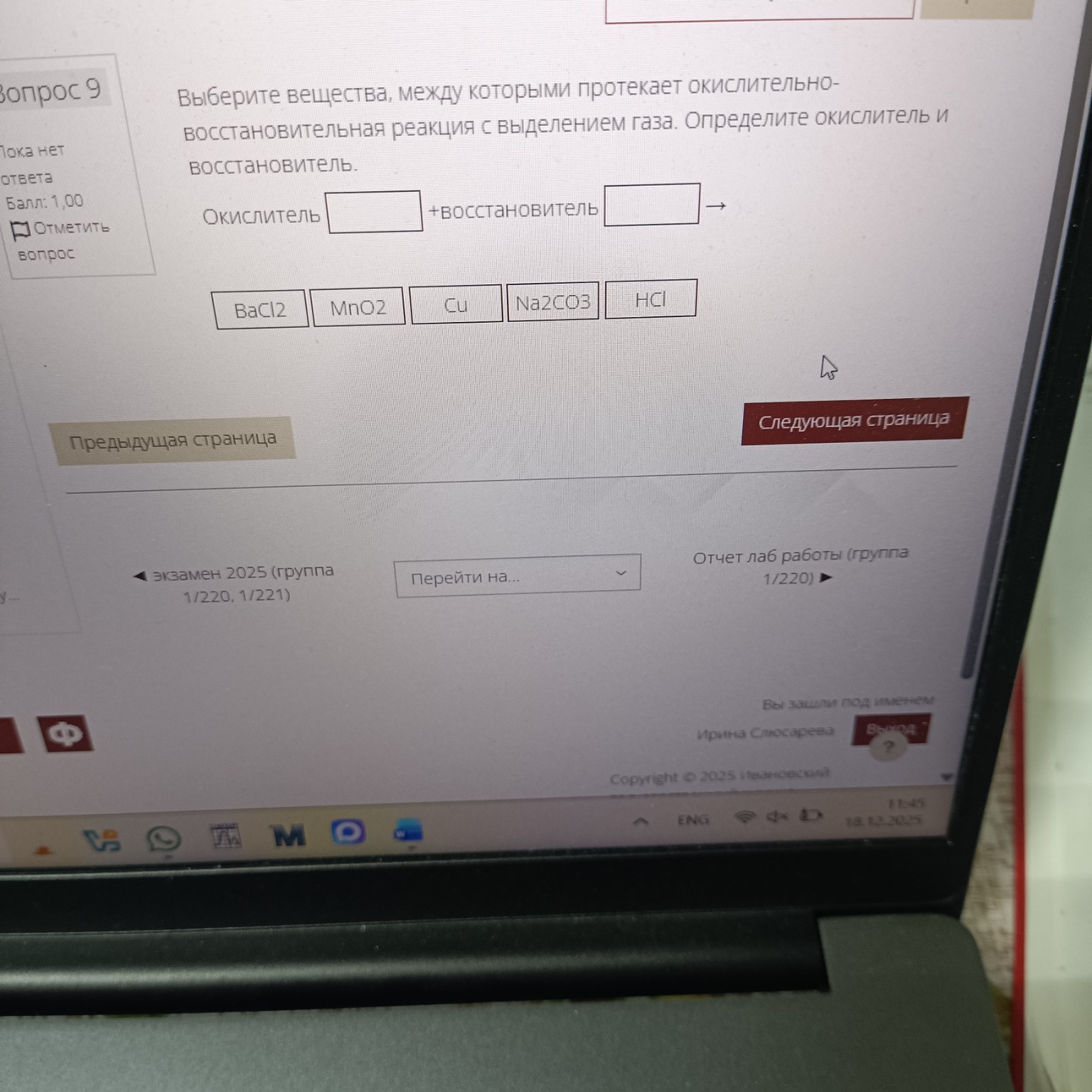
help_outlineУсловие задачи
lightbulbКраткий ответ
Для протекания ОВР с выделением газа необходимы MnO2 и HCl. MnO2 является окислителем, а HCl – восстановителем, в результате реакции выделяется хлор.
Подробное решение
Хорошо, давайте решим эту задачу по химии.
Задача: Выберите вещества, между которыми протекает окислительно-восстановительная реакция с выделением газа. Определите окислитель и восстановитель.
Предложенные вещества: BaCl2, MnO2, Cu, Na2CO3, HCl.
Нам нужно найти такую пару веществ, при взаимодействии которых произойдет окислительно-восстановительная реакция (ОВР) и выделится газ.
Рассмотрим предложенные вещества и их свойства:
* BaCl2 (хлорид бария) - соль, барий в степени окисления +2, хлор в -1. Не является ни сильным окислителем, ни сильным восстановителем.
* MnO2 (оксид марганца(IV)) - марганец в степени окисления +4. Может быть окислителем (например, в кислой среде).
* Cu (медь) - простое вещество, металл. Медь в степени окисления 0, является восстановителем.
* Na2CO3 (карбонат натрия) - соль, углерод в степени окисления +4. Не является ни сильным окислителем, ни сильным восстановителем в ОВР. При взаимодействии с кислотами может выделять CO2, но это не ОВР.
* HCl (соляная кислота) - водород в степени окисления +1, хлор в -1. Может быть восстановителем (за счет Cl-) или кислотой.
Ищем ОВР с выделением газа.
Рассмотрим возможные комбинации:
1. **MnO2 + HCl**:
Оксид марганца(IV) (MnO2) является сильным окислителем в кислой среде. Соляная кислота (HCl) может выступать в роли восстановителя за счет ионов Cl-.
При взаимодействии MnO2 с концентрированной HCl при нагревании выделяется газообразный хлор (Cl2). Это классическая реакция получения хлора в лаборатории.
Степени окисления:
В MnO2: Mn (+4)
В HCl: Cl (-1)
В продуктах: Cl2 (0), MnCl2 (Mn +2)
Марганец понижает степень окисления с +4 до +2 (восстанавливается).
Хлор повышает степень окисления с -1 до 0 (окисляется).
Это окислительно-восстановительная реакция с выделением газа (Cl2).
Уравнение реакции:
MnO2 + 4HCl → MnCl2 + Cl2↑ + 2H2O
В этой реакции:
* Окислитель: MnO2 (марганец в MnO2 принимает электроны)
* Восстановитель: HCl (хлор в HCl отдает электроны)
2. **Cu + HCl**:
Медь (Cu) - малоактивный металл, не реагирует с соляной кислотой с выделением водорода. Для реакции с HCl требуется окислитель, например, кислород воздуха, но тогда не будет выделения газа из самой реакции Cu + HCl.
3. **Na2CO3 + HCl**:
Это реакция обмена, не ОВР. Выделяется газ CO2, но степени окисления элементов не меняются.
Na2CO3 + 2HCl → 2NaCl + H2O + CO2↑
4. Другие комбинации не дадут ОВР с выделением газа из предложенного списка.
Таким образом, подходящая реакция - это взаимодействие MnO2 и HCl.
Определим окислитель и восстановитель:
* Окислитель - вещество, которое принимает электроны и понижает свою степень окисления. В данной реакции это MnO2, так как марганец понижает степень окисления с +4 до +2.
* Восстановитель - вещество, которое отдает электроны и повышает свою степень окисления. В данной реакции это HCl (точнее, ионы Cl-), так как хлор повышает степень окисления с -1 до 0.
Ответы для записи в тетрадь:
1. Окислитель: MnO2
2. Восстановитель: HCl
Уравнение реакции:
\[MnO_2 + 4HCl \rightarrow MnCl_2 + Cl_2\uparrow + 2H_2O\]