schoolХимия
verifiedРешено AI
Практическая работа №3 по Химии: Получение Аммиака и его Свойства
help_outlineУсловие задачи
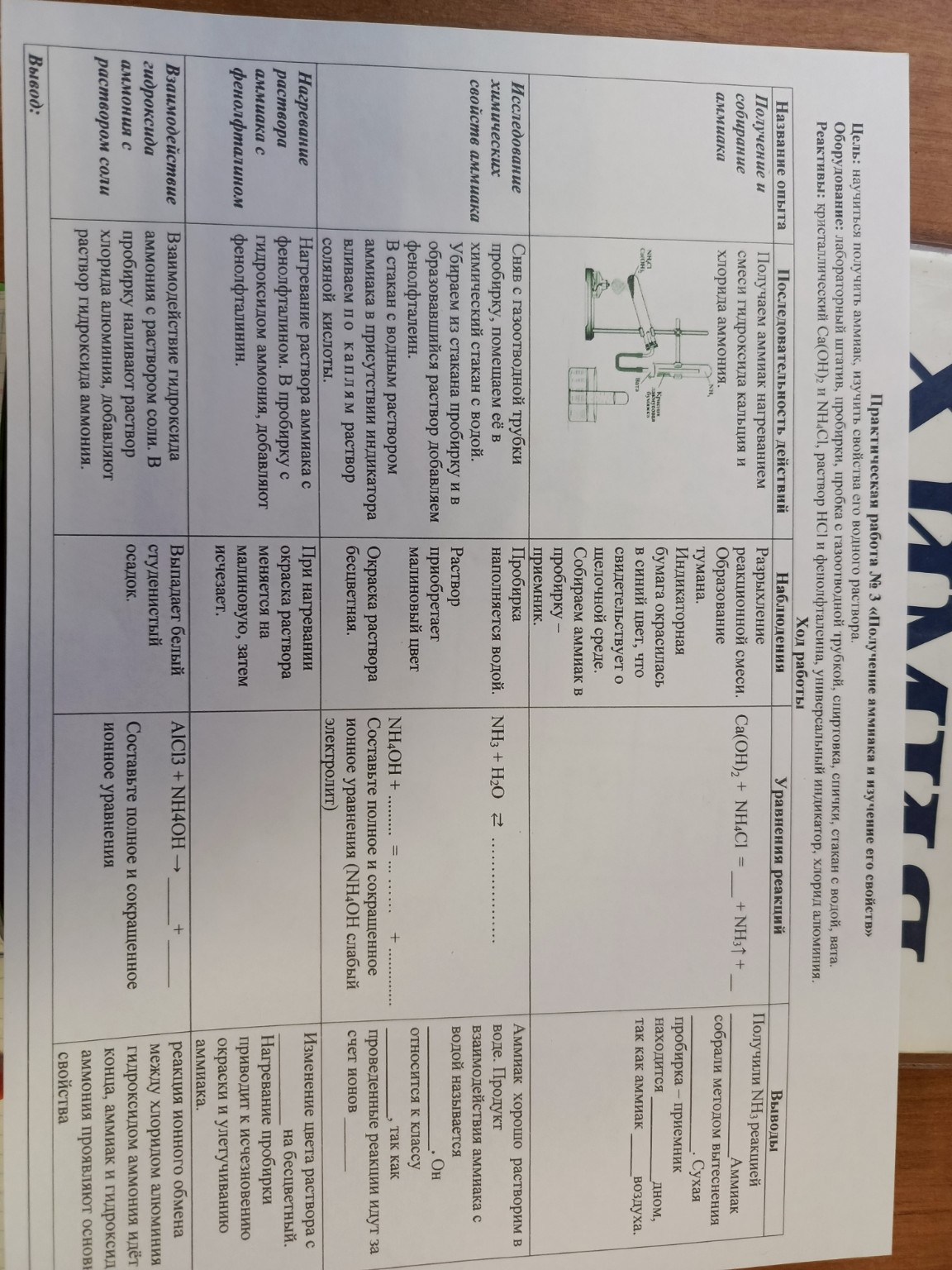
lightbulbКраткий ответ
Представлено готовое решение практической работы №3 по химии, включающее уравнения реакций получения аммиака и изучения его свойств, а также выводы по проделанной работе. Рассмотрено взаимодействие аммиака с водой и соляной кислотой.
Подробное решение
Ниже представлено оформление практической работы № 3 по химии, заполненное согласно вашему заданию для переписывания в тетрадь.
Практическая работа № 3
Тема: Получение аммиака и изучение его свойств.
1. Получение и собирание аммиака.
Уравнение реакции:
\[ 2NH_{4}Cl + Ca(OH)_{2} \xrightarrow{t} CaCl_{2} + 2NH_{3}\uparrow + 2H_{2}O \]
Выводы: Получили \( NH_{3} \) реакцией обмена. Аммиак собрали методом вытеснения воздуха. Сухая пробирка-приемник находится вверх дном, так как аммиак легче воздуха.
2. Исследование химических свойств аммиака.
Уравнение реакции взаимодействия с водой:
\[ NH_{3} + H_{2}O \rightleftarrows NH_{4}OH \rightleftarrows NH_{4}^{+} + OH^{-} \]
Уравнение реакции с соляной кислотой (в стакане):
\[ NH_{4}OH + HCl = NH_{4}Cl + H_{2}O \]
Полное ионное уравнение:
\[ NH_{4}OH + H^{+} + Cl^{-} = NH_{4}^{+} + Cl^{-} + H_{2}O \]
Сокращенное ионное уравнение:
\[ NH_{4}OH + H^{+} = NH_{4}^{+} + H_{2}O \]
Выводы: Аммиак хорошо растворим в воде. Продукт взаимодействия аммиака с водой называется гидрат аммиака. Он относится к классу оснований, так как проведенные реакции идут за счет ионов \( OH^{-} \).
3. Нагревание раствора аммиака с фенолфталеином.
Выводы: Изменение цвета раствора с малинового на бесцветный. Нагревание пробирки приводит к исчезновению окраски и улетучиванию аммиака.
4. Взаимодействие гидроксида аммония с раствором соли.
Уравнение реакции:
\[ AlCl_{3} + 3NH_{4}OH = Al(OH)_{3}\downarrow + 3NH_{4}Cl \]
Полное ионное уравнение:
\[ Al^{3+} + 3Cl^{-} + 3NH_{4}OH = Al(OH)_{3}\downarrow + 3NH_{4}^{+} + 3Cl^{-} \]
Сокращенное ионное уравнение:
\[ Al^{3+} + 3NH_{4}OH = Al(OH)_{3}\downarrow + 3NH_{4}^{+} \]
Выводы: Произошла реакция ионного обмена между хлоридом алюминия и гидроксидом аммония. Реакция идет до конца, так как образуется осадок. Аммиак и гидроксид аммония проявляют основные свойства.
Общий вывод: В ходе работы мы научились получать аммиак лабораторным способом, изучили его физические свойства (газ легче воздуха, хорошо растворим) и химические свойства (взаимодействие с водой, кислотами и солями), подтвердив его основные свойства.