schoolХимия
verifiedРешено AI
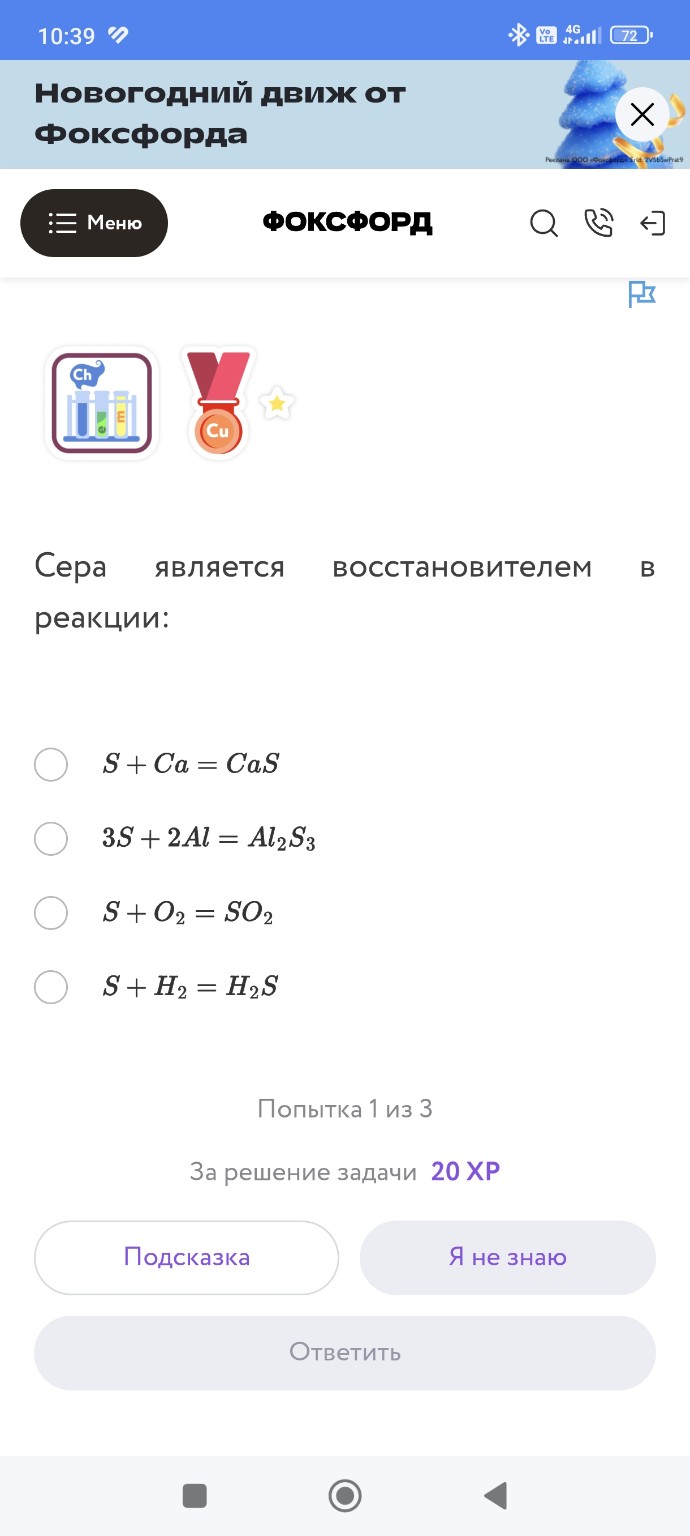
Сера - восстановитель в реакции: S + O2 = SO2
help_outlineУсловие задачи
lightbulbКраткий ответ
В реакции S + O2 = SO2 сера является восстановителем, так как отдает электроны и повышает свою степень окисления с 0 до +4. Кислород при этом является окислителем, принимая электроны и понижая свою степень окисления.
Подробное решение
Задание: Сера является восстановителем в реакции.
Правильный ответ: \(S + O_{2} = SO_{2}\).
Решение для записи в тетрадь:
Восстановитель — это вещество (атом), которое отдает электроны, при этом его степень окисления повышается.
Окислитель — это вещество (атом), которое принимает электроны, при этом его степень окисления понижается.
Проверим изменение степеней окисления серы в каждой реакции:
1) \(S^{0} + Ca^{0} = Ca^{+2}S^{-2}\)
Здесь сера понижает степень окисления с \(0\) до \(-2\). Значит, сера — окислитель.
2) \(3S^{0} + 2Al^{0} = Al_{2}^{+3}S_{3}^{-2}\)
Здесь сера понижает степень окисления с \(0\) до \(-2\). Значит, сера — окислитель.
3) \(S^{0} + O_{2}^{0} = S^{+4}O_{2}^{-2}\)
В этой реакции сера повышает степень окисления с \(0\) до \(+4\). Это происходит потому, что кислород является более электроотрицательным элементом и забирает электроны у серы. Так как степень окисления серы повысилась, она является восстановителем.
4) \(S^{0} + H_{2}^{0} = H_{2}^{+1}S^{-2}\)
Здесь сера понижает степень окисления с \(0\) до \(-2\). Значит, сера — окислитель.
Вывод: Сера проявляет свойства восстановителя только в реакции с кислородом.
Ответ: \(S + O_{2} = SO_{2}\).