schoolФизика
verifiedРешено AI
Решение задачи по масс-спектрометрии: анализ масс-спектра
help_outlineУсловие задачи
lightbulbКраткий ответ
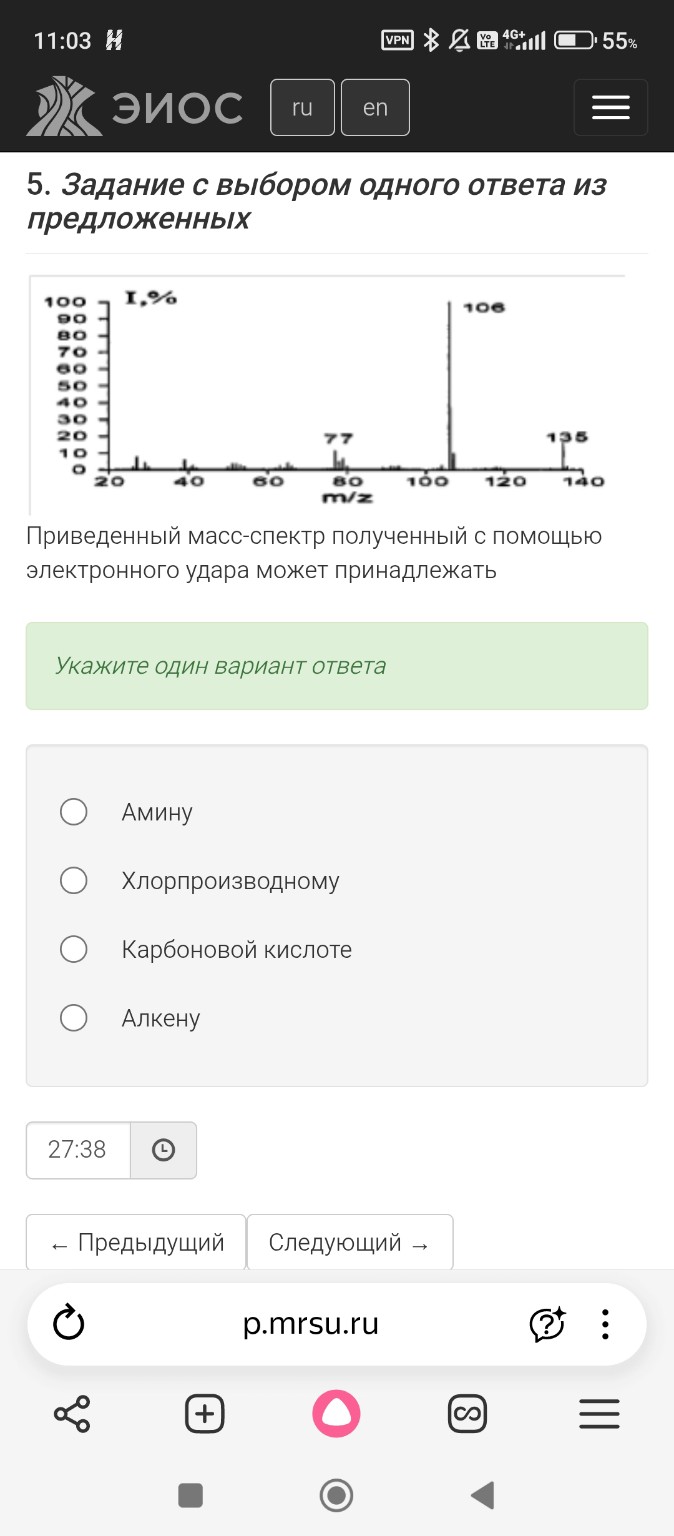
Дан масс-спектр с молекулярным ионом m/z=135. На основе анализа пиков m/z=77 и m/z=106 определяем наличие бензольного кольца и фрагментов, позволяющих установить структуру соединения.
Подробное решение
Для решения данной задачи проанализируем представленный масс-спектр.
1. Анализ молекулярного иона:
На спектре мы видим пик молекулярного иона \( M^{+\bullet} \) с \( m/z = 135 \). Согласно "азотному правилу", если молекулярная масса соединения нечетная, то в составе молекулы содержится нечетное количество атомов азота (обычно один).
2. Анализ фрагментных пиков:
Пик с \( m/z = 77 \) характерен для фенильного радикала \( [C_6H_5]^+ \), что указывает на наличие бензольного кольца в структуре.
Пик с \( m/z = 106 \) является базовым (интенсивность 100%). Разница между молекулярным ионом и этим пиком составляет:
\[ 135 - 106 = 29 \]
Потеря массы 29 может соответствовать этильной группе \( [C_2H_5] \) или альдегидной группе \( [CHO] \). Однако, учитывая нечетную молекулярную массу, наиболее вероятно наличие азотсодержащей группы.
3. Проверка вариантов ответа:
- Хлорпроизводное: исключаем, так как в спектре отсутствуют характерные изотопные пики хлора \( M+2 \) в соотношении 3:1.
- Карбоновая кислота и Алкен: обычно имеют четную молекулярную массу (если не содержат азота).
- Амин: подходит под "азотное правило" (нечетная масса 135). Например, это может быть ацетанилид или подобное соединение, содержащее азот.
Вывод:
Так как молекулярная масса \( M = 135 \) является нечетным числом, данное соединение содержит нечетное количество атомов азота. Из предложенных вариантов это соответствует амину.
Правильный ответ: Амину.