schoolХимия
verifiedРешено AI
Расчет pH раствора соляной кислоты HCl
help_outlineУсловие задачи
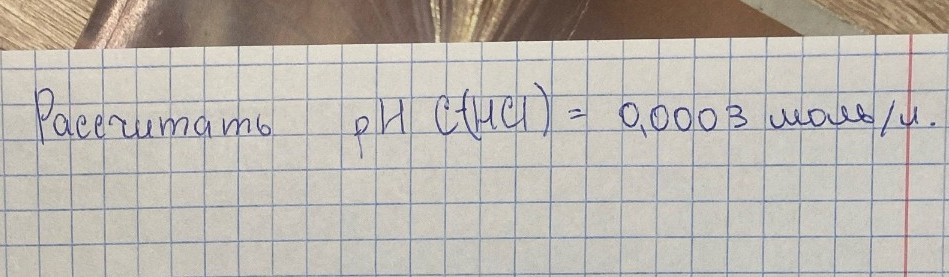
lightbulbКраткий ответ
pH раствора HCl с концентрацией 0,0003 моль/л рассчитывается по формуле pH = -lg[H+]. В данном случае pH ≈ 3.52.
Подробное решение
Задача: Рассчитать pH раствора соляной кислоты \( HCl \) с концентрацией \( C(HCl) = 0,0003 \) моль/л.
Дано:
\( C(HCl) = 0,0003 \) моль/л = \( 3 \cdot 10^{-4} \) моль/л
Найти:
\( pH \) — ?
Решение:
1. Соляная кислота \( HCl \) является сильным электролитом и в водном растворе диссоциирует полностью по уравнению:
\[ HCl \rightarrow H^{+} + Cl^{-} \]
2. Так как из 1 моль кислоты образуется 1 моль ионов водорода, то концентрация ионов водорода \( [H^{+}] \) равна концентрации кислоты:
\[ [H^{+}] = C(HCl) = 0,0003 \text{ моль/л} = 3 \cdot 10^{-4} \text{ моль/л} \]
3. Водородный показатель \( pH \) рассчитывается по формуле:
\[ pH = -\lg[H^{+}] \]
4. Подставим значение концентрации в формулу:
\[ pH = -\lg(3 \cdot 10^{-4}) \]
\[ pH = -(\lg 3 + \lg 10^{-4}) \]
\[ pH = -(0,477 - 4) \]
\[ pH = -(-3,523) \]
\[ pH \approx 3,52 \]
Ответ: \( pH \approx 3,52 \).