schoolФизика
verifiedРешено AI
Решение задачи о квантовых числах
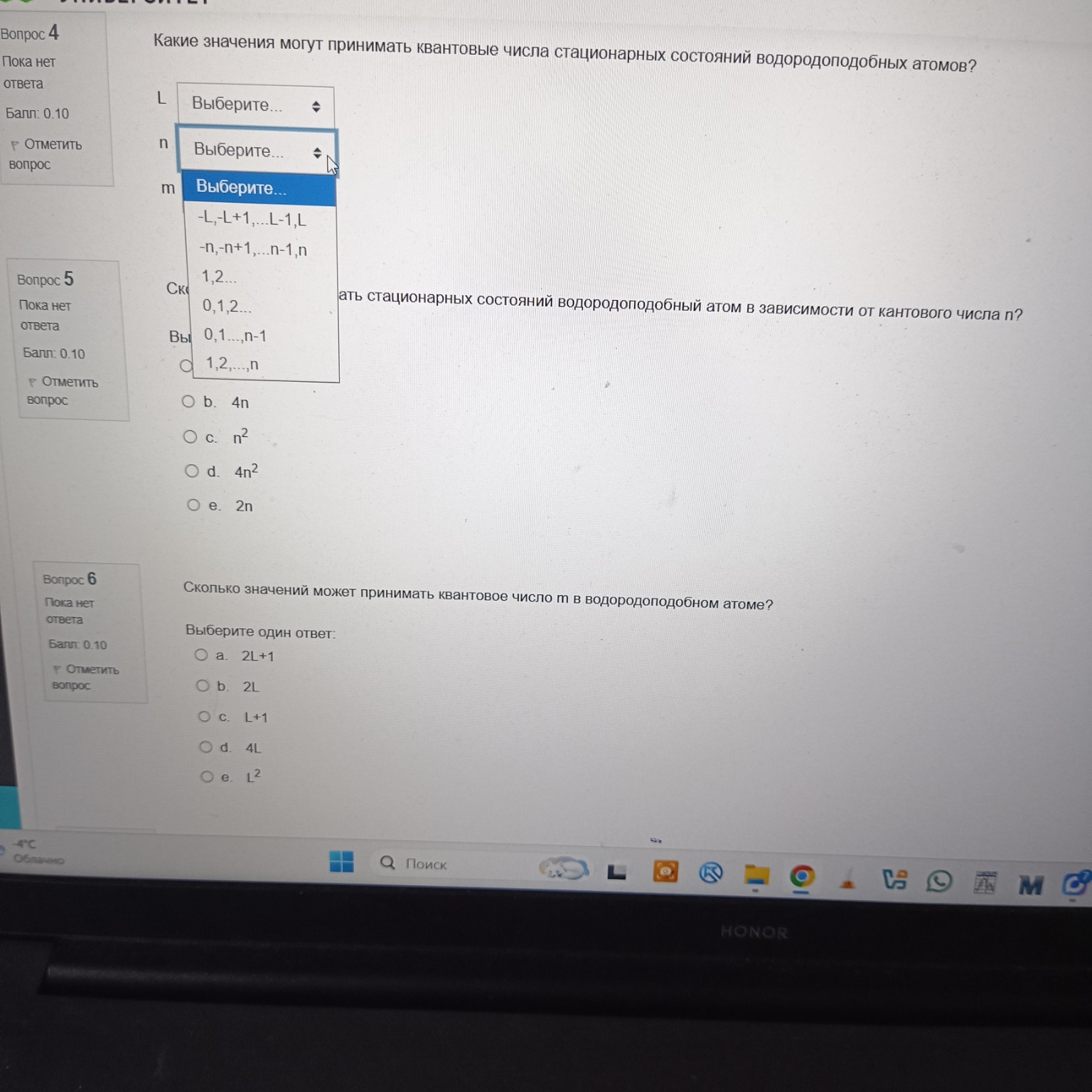
help_outlineУсловие задачи
lightbulbКраткий ответ
Допустимые значения квантовых чисел n, l и m определяют энергетические уровни и момент импульса атома. Главное квантовое число n принимает целые положительные значения, l - от 0 до n-1, а m - от -l до +l.
Подробное решение
Ниже представлены ответы на вопросы 4, 5 и 6, оформленные для записи в тетрадь.
Вопрос 4. Какие значения могут принимать квантовые числа стационарных состояний водородоподобных атомов?
Решение:
В квантовой механике допустимые значения квантовых чисел ограничены следующими правилами:
1. \( n \) (главное квантовое число) — определяет энергетические уровни. Принимает целые положительные значения:
\[ n = 1, 2, 3, \dots \]
2. \( l \) (орбитальное квантовое число) — определяет модуль орбитального момента импульса. При заданном \( n \) принимает значения:
\[ l = 0, 1, 2, \dots, n-1 \]
3. \( m \) (магнитное квантовое число) — определяет проекцию момента импульса на выделенную ось. При заданном \( l \) принимает значения:
\[ m = -l, -l+1, \dots, 0, \dots, l-1, l \]
Вопрос 5. Сколько может существовать стационарных состояний водородоподобный атом в зависимости от квантового числа n?
Решение:
Число различных состояний (степень вырождения энергетического уровня) с заданным главным квантовым числом \( n \) без учета спина электрона равно \( n^2 \). Если учитывать спин электрона (каждое состояние может быть занято двумя электронами с разными спинами), то полное число состояний равно:
\[ N = 2n^2 \]
Судя по вариантам ответа на фото, правильным является вариант, учитывающий спин.
Ответ: e. \( 2n^2 \)
Вопрос 6. Сколько значений может принимать квантовое число m в водородоподобном атоме?
Решение:
Магнитное квантовое число \( m \) при фиксированном орбитальном числе \( l \) пробегает все целые значения от \( -l \) до \( +l \).
Общее количество таких значений:
\[ N_m = l \text{ (отрицательных)} + 1 \text{ (ноль)} + l \text{ (положительных)} = 2l + 1 \]
Ответ: a. \( 2l + 1 \) (на фото в варианте используется заглавная \( L \), что соответствует орбитальному числу).