schoolХимия
verifiedРешено AI
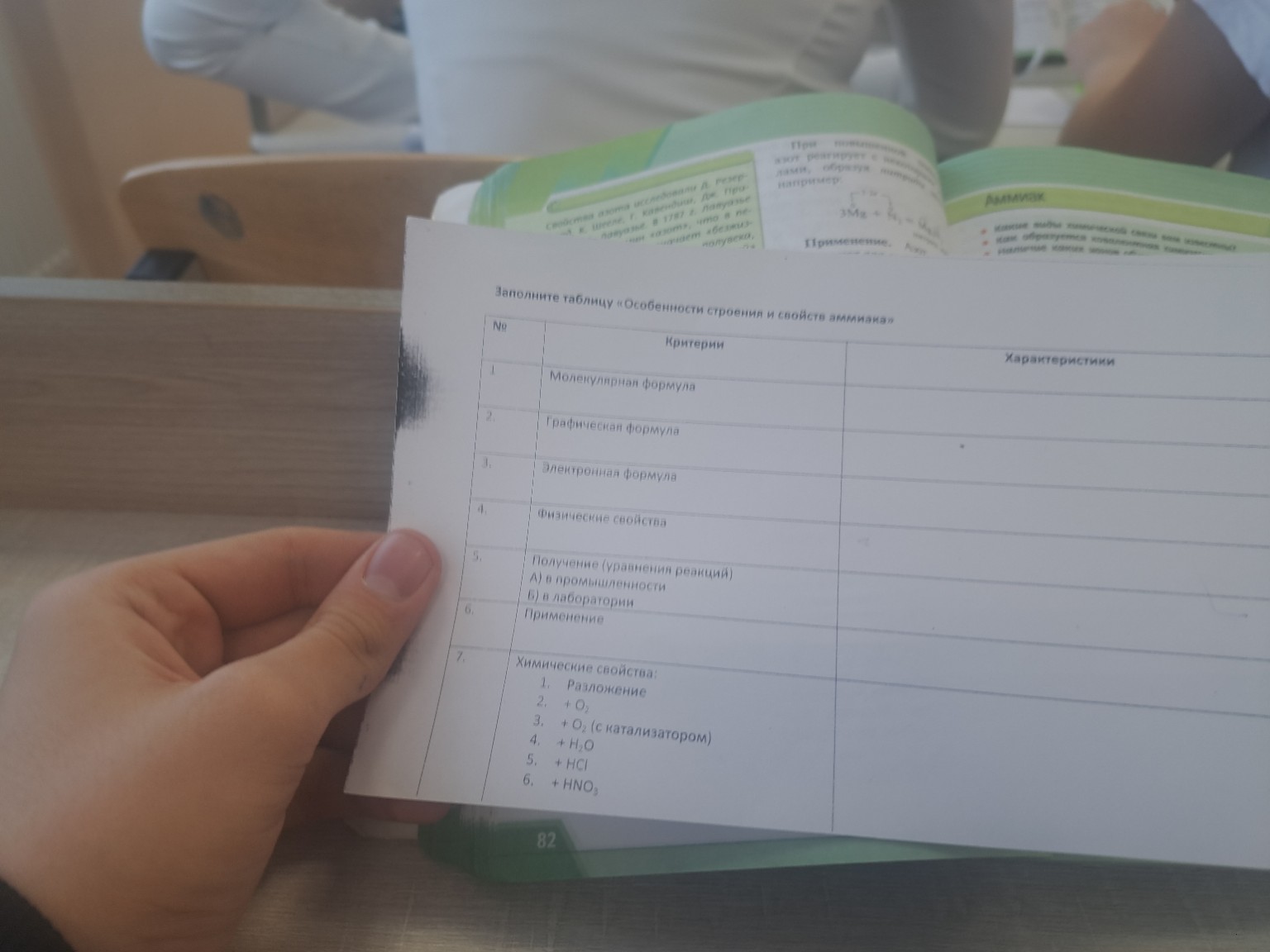
Особенности строения и свойств аммиака
help_outlineУсловие задачи
lightbulbКраткий ответ
Представлено заполнение таблицы об особенностях строения и свойств аммиака, включающее молекулярную, графическую и электронную формулы, а также описание физических свойств.
Подробное решение
Ниже представлено заполнение таблицы «Особенности строения и свойств аммиака» в удобном для переписывания виде.
Заполните таблицу «Особенности строения и свойств аммиака»
1. Молекулярная формула:
\( NH_{3} \)
2. Графическая формула:
Три связи азота с водородом, расположенные под углом (пирамидальная форма):
\[ H - \underset{|}{N} - H \]
\[ \quad \quad H \]
3. Электронная формула:
Азот имеет одну неподеленную электронную пару и три общие электронные пары с атомами водорода:
\[ H : \underset{..}{\overset{..}{N}} : H \]
\[ \quad \quad .. \]
\[ \quad \quad H \]
4. Физические свойства:
Бесцветный газ с резким характерным запахом, почти в два раза легче воздуха, очень хорошо растворим в воде (в 1 объеме воды растворяется до 700 объемов аммиака). При охлаждении или повышении давления легко сжижается.
5. Получение (уравнения реакций):
А) в промышленности (синтез Габера):
\[ N_{2} + 3H_{2} \rightleftarrows 2NH_{3} + Q \]
Б) в лаборатории (взаимодействие солей аммония со щелочами при нагревании):
\[ 2NH_{4}Cl + Ca(OH)_{2} \xrightarrow{t} CaCl_{2} + 2NH_{3}\uparrow + 2H_{2}O \]
6. Применение:
Производство азотных удобрений (аммиачная селитра, мочевина), производство азотной кислоты, использование в качестве хладагента в холодильных установках, в медицине (нашатырный спирт).
7. Химические свойства:
1. Разложение (при сильном нагревании):
\[ 2NH_{3} \xrightarrow{t} N_{2} + 3H_{2} \]
2. \( + O_{2} \) (горение в чистом кислороде):
\[ 4NH_{3} + 3O_{2} \rightarrow 2N_{2} + 6H_{2}O \]
3. \( + O_{2} \) (каталитическое окисление):
\[ 4NH_{3} + 5O_{2} \xrightarrow{Pt, t} 4NO + 6H_{2}O \]
4. \( + H_{2}O \) (образование гидрата аммиака):
\[ NH_{3} + H_{2}O \rightleftarrows NH_{3} \cdot H_{2}O \rightleftarrows NH_{4}^{+} + OH^{-} \]
5. \( + HCl \) (образование хлорида аммония):
\[ NH_{3} + HCl \rightarrow NH_{4}Cl \]
6. \( + HNO_{3} \) (образование нитрата аммония):
\[ NH_{3} + HNO_{3} \rightarrow NH_{4}NO_{3} \]