schoolХимия
verifiedРешено AI
Решение уравнения реакции горения C4H8 + O2 = CO2 + H2O
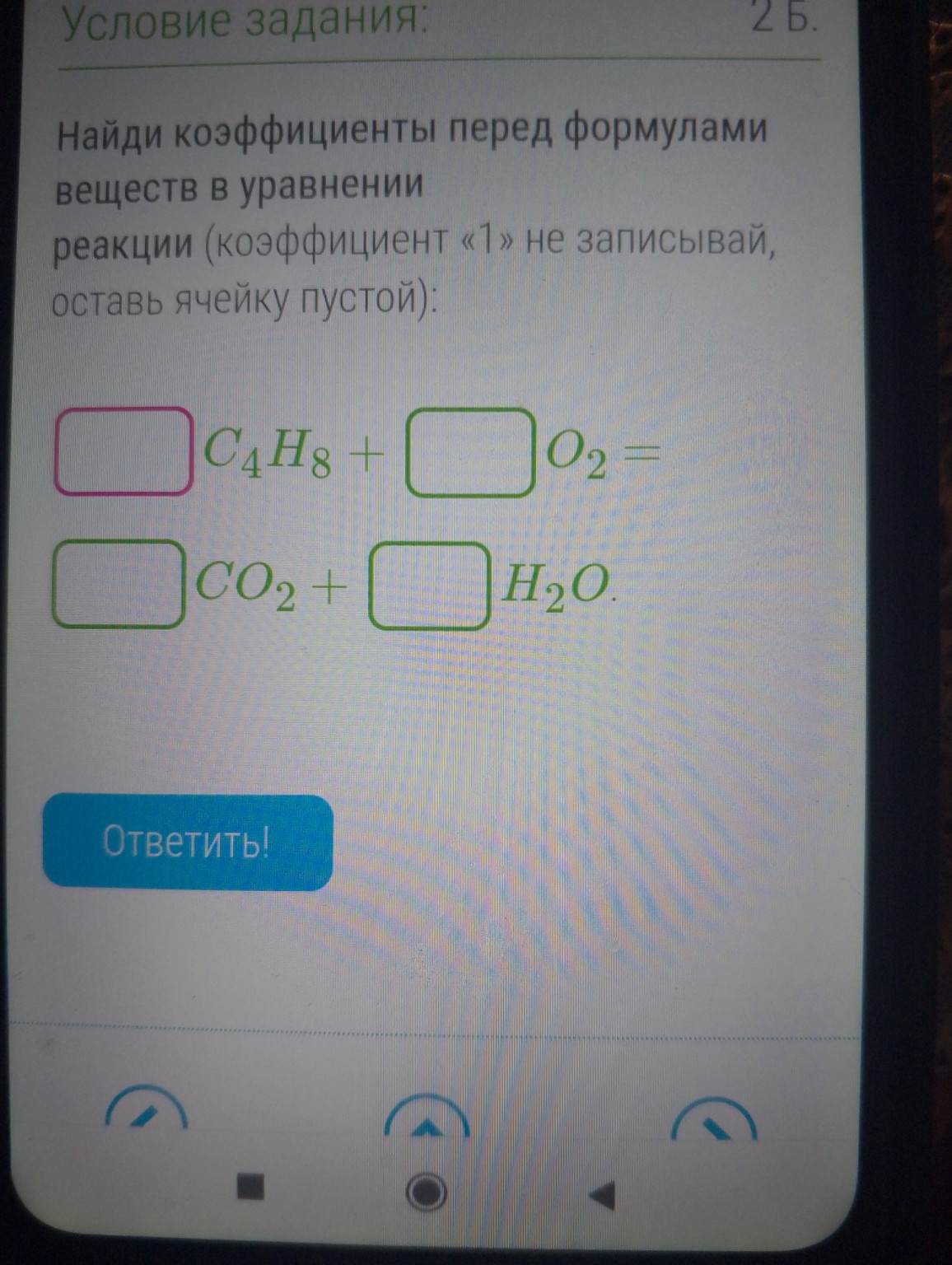
help_outlineУсловие задачи
lightbulbКраткий ответ
Для уравнения горения углеводорода C4H8 + O2 = CO2 + H2O необходимо расставить коэффициенты: C4H8 + 6O2 = 4CO2 + 4H2O. Уравнение балансируется путем уравнивания количества атомов каждого элемента в обеих частях.
Подробное решение
Для того чтобы расставить коэффициенты в уравнении реакции горения углеводорода, нужно уравнять количество атомов каждого элемента в левой и правой частях уравнения.
\[C_4H_8 + O_2 = CO_2 + H_2O\]
1. Уравниваем углерод (\(C\)). В левой части 4 атома углерода, значит, перед \(CO_2\) ставим коэффициент 4:
\[C_4H_8 + O_2 = 4CO_2 + H_2O\]
2. Уравниваем водород (\(H\)). В левой части 8 атомов водорода, значит, перед \(H_2O\) ставим коэффициент 4 (так как \(4 \cdot 2 = 8\)):
\[C_4H_8 + O_2 = 4CO_2 + 4H_2O\]
3. Считаем кислород (\(O\)) в правой части: в \(4CO_2\) содержится \(4 \cdot 2 = 8\) атомов, в \(4H_2O\) содержится \(4 \cdot 1 = 4\) атома. Всего \(8 + 4 = 12\) атомов кислорода.
Чтобы в левой части тоже было 12 атомов, перед \(O_2\) нужно поставить коэффициент 6 (так как \(6 \cdot 2 = 12\)).
Итоговое уравнение:
\[C_4H_8 + 6O_2 = 4CO_2 + 4H_2O\]
Согласно условию задачи (коэффициент «1» не записывать):
Перед \(C_4H_8\) — (пусто)
Перед \(O_2\) — 6
Перед \(CO_2\) — 4
Перед \(H_2O\) — 4