schoolМатематика
verifiedРешено AI
Решение задачи: расчет массы SO2 при горении серы
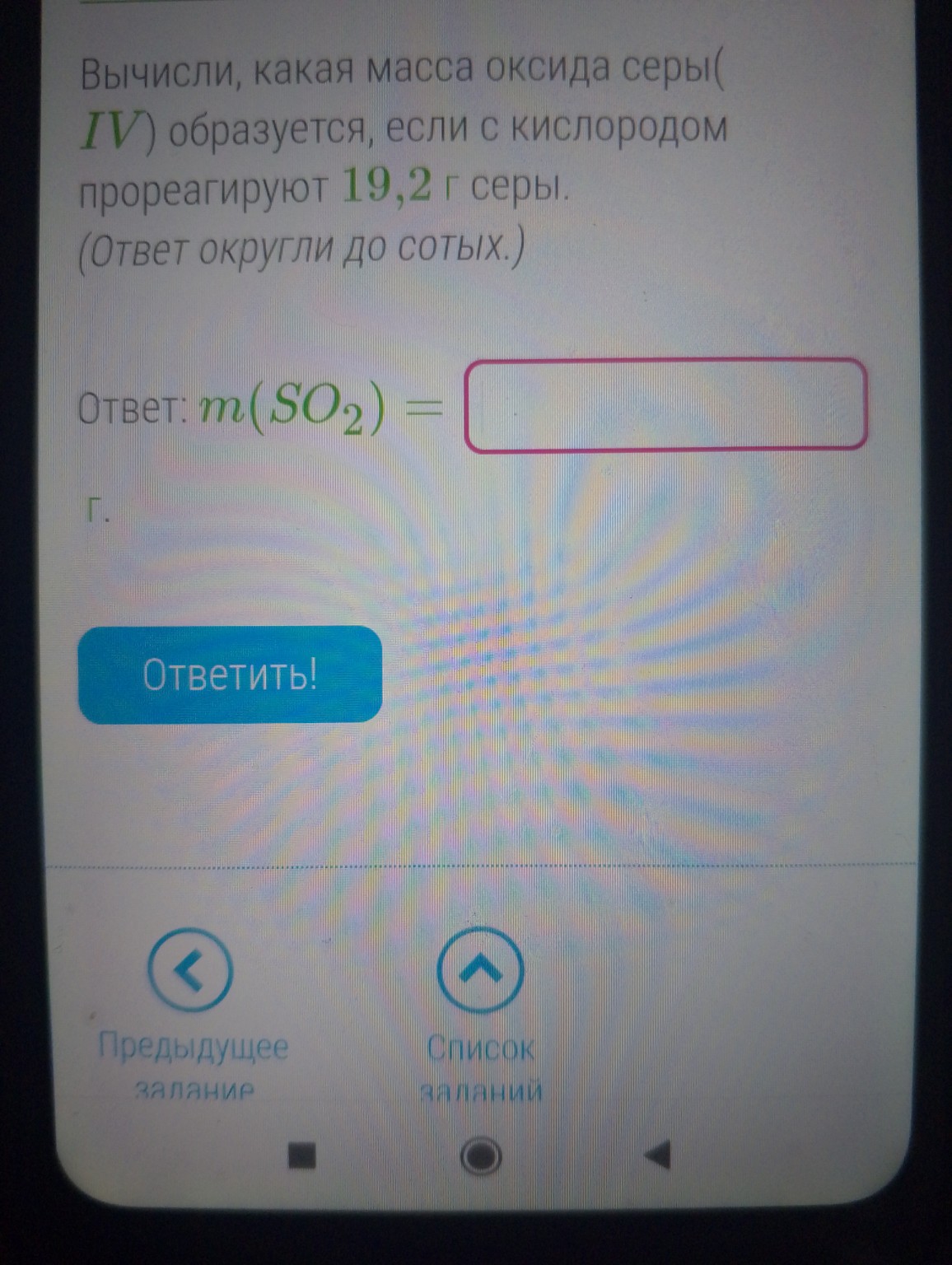
help_outlineУсловие задачи
lightbulbКраткий ответ
При горении 19,2 г серы образуется 38,40 г оксида серы(IV) (SO2). Решение включает расчет количества вещества и массы SO2 по уравнению реакции.
Подробное решение
Для решения этой задачи составим уравнение химической реакции горения серы и проведем расчеты по нему.
1. Запишем уравнение реакции:
\[S + O_2 = SO_2\]
2. Найдем количество вещества серы (\(n\)), вступившей в реакцию. Молярная масса серы \(M(S) = 32\) г/моль.
\[n(S) = \frac{m(S)}{M(S)} = \frac{19,2}{32} = 0,6 \text{ моль}\]
3. По уравнению реакции видно, что из 1 моль серы образуется 1 моль оксида серы(IV). Следовательно:
\[n(SO_2) = n(S) = 0,6 \text{ моль}\]
4. Вычислим массу оксида серы(IV). Молярная масса \(M(SO_2) = 32 + 16 \cdot 2 = 64\) г/моль.
\[m(SO_2) = n(SO_2) \cdot M(SO_2) = 0,6 \cdot 64 = 38,4 \text{ г}\]
Так как в условии просят округлить до сотых, запишем результат с двумя знаками после запятой.
Ответ:
\(m(SO_2) = 38,40\) г.