schoolМатематика
verifiedРешено AI
Решение задачи: Взаимодействие цинка с серной кислотой
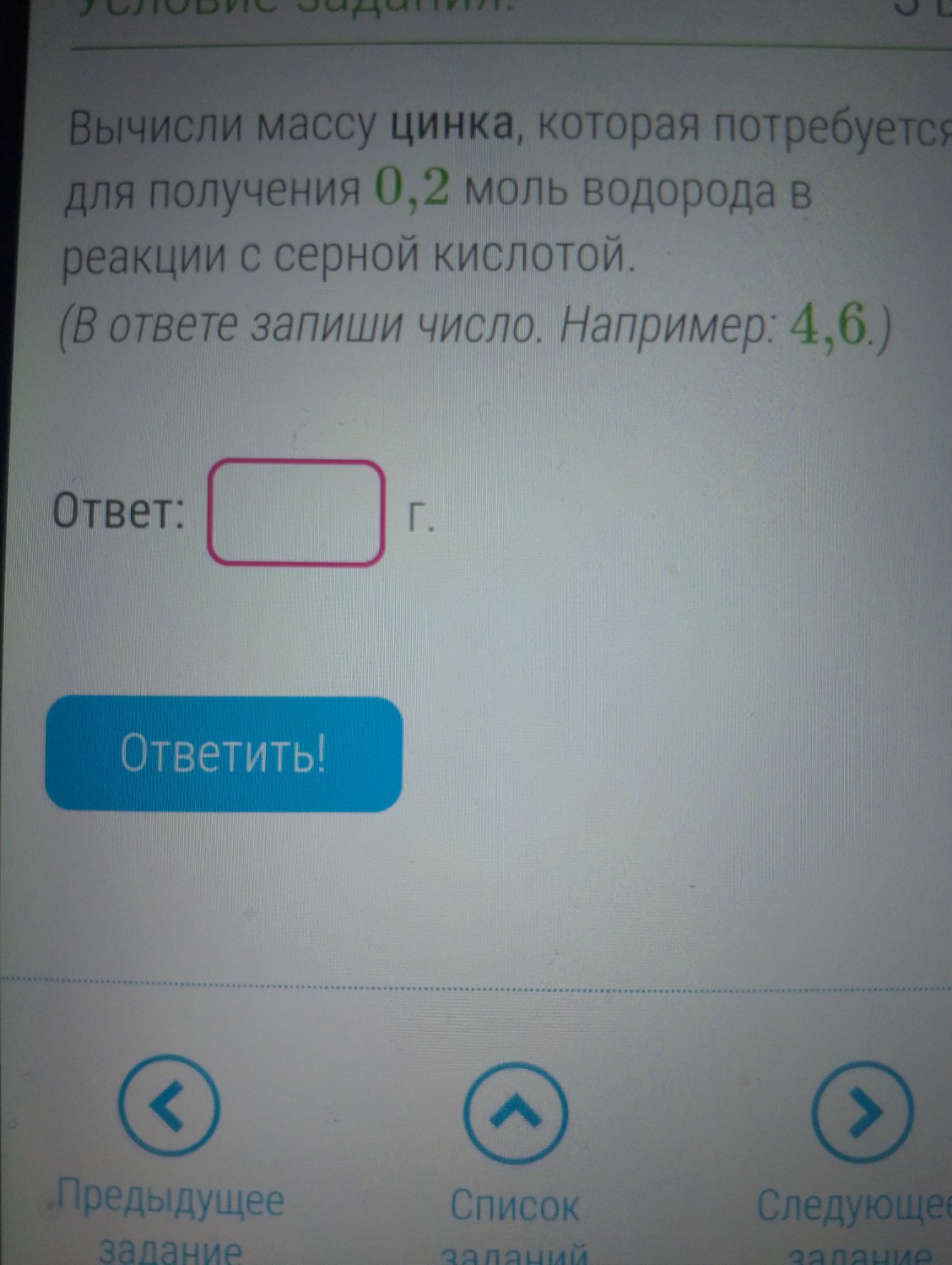
help_outlineУсловие задачи
lightbulbКраткий ответ
Для реакции цинка с серной кислотой, зная количество выделившегося водорода (0,2 моль), рассчитываем массу цинка, вступившего в реакцию. Ответ: 13 г.
Подробное решение
Для решения этой задачи составим уравнение химической реакции и проведем расчеты по нему.
Дано:
\( n(H_2) = 0,2 \) моль
Найти: \( m(Zn) \) — ?
Решение:
1. Запишем уравнение реакции взаимодействия цинка с серной кислотой:
\[ Zn + H_2SO_4 \rightarrow ZnSO_4 + H_2 \uparrow \]
2. По уравнению реакции видно, что количества вещества цинка и выделившегося водорода относятся как \( 1:1 \). Следовательно:
\[ n(Zn) = n(H_2) = 0,2 \text{ моль} \]
3. Найдем молярную массу цинка по таблице Менделеева:
\[ M(Zn) = 65 \text{ г/моль} \]
4. Вычислим массу цинка по формуле \( m = n \cdot M \):
\[ m(Zn) = 0,2 \text{ моль} \cdot 65 \text{ г/моль} = 13 \text{ г} \]
Ответ: 13