schoolМатематика
verifiedРешено AI
Решение задачи: Восстановление оксида железа(II) водородом
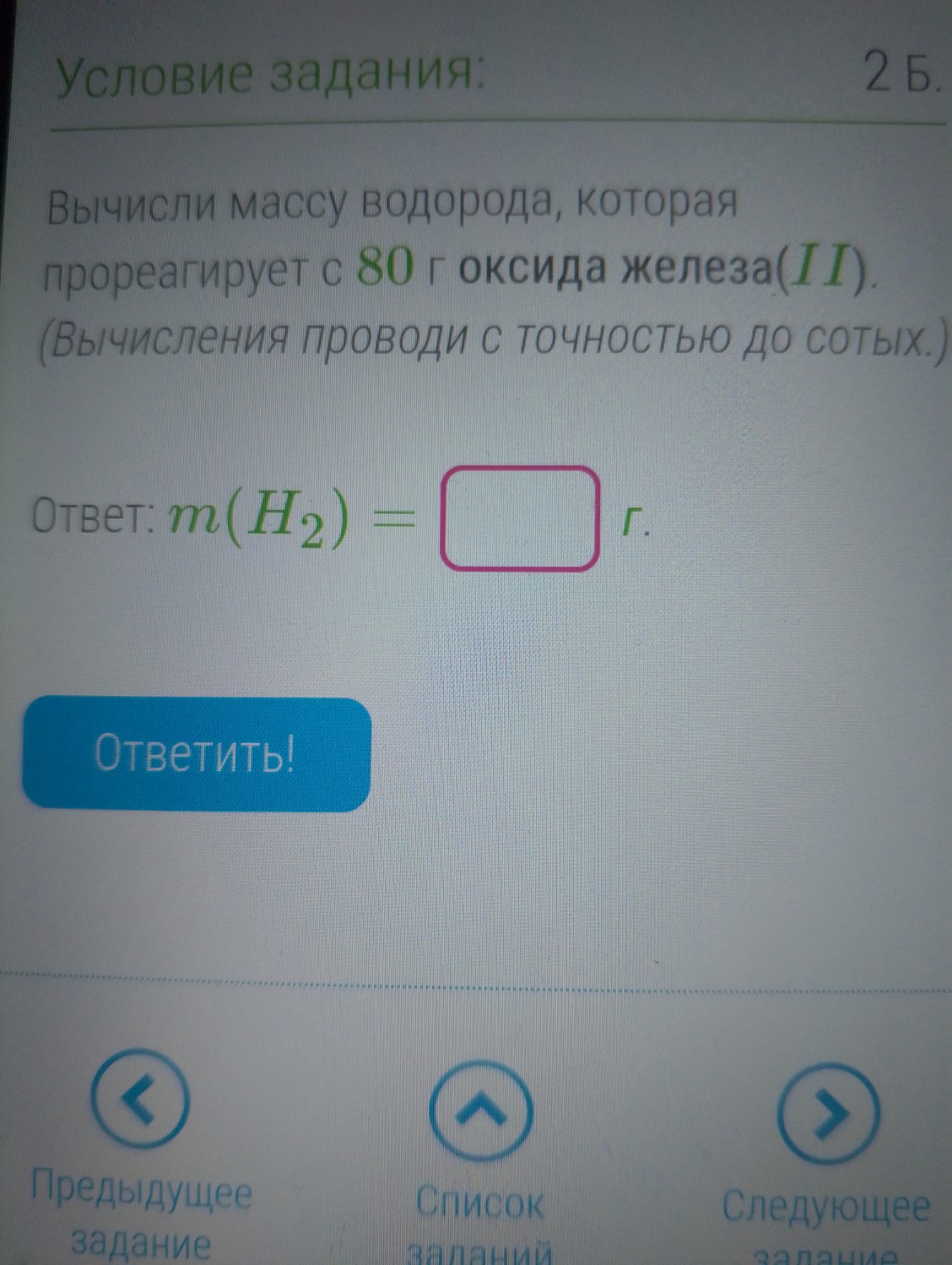
help_outlineУсловие задачи
lightbulbКраткий ответ
Для восстановления 80 г оксида железа(II) потребуется примерно 2.22 г водорода. Решение включает уравнение реакции и подробные расчеты.
Подробное решение
Для решения этой задачи составим уравнение химической реакции восстановления железа из его оксида водородом и выполним расчеты.
Дано:
\( m(FeO) = 80 \) г
Найти: \( m(H_2) \) — ?
Решение:
1. Запишем уравнение реакции:
\[ FeO + H_2 \xrightarrow{t} Fe + H_2O \]
2. Рассчитаем молярные массы веществ:
\[ M(FeO) = 56 + 16 = 72 \text{ г/моль} \]
\[ M(H_2) = 2 \cdot 1 = 2 \text{ г/моль} \]
3. Найдем количество вещества оксида железа(II):
\[ n(FeO) = \frac{m(FeO)}{M(FeO)} = \frac{80 \text{ г}}{72 \text{ г/моль}} \approx 1,1111 \text{ моль} \]
4. По уравнению реакции коэффициенты перед \( FeO \) и \( H_2 \) равны \( 1 \), значит:
\[ n(H_2) = n(FeO) = 1,1111 \text{ моль} \]
5. Вычислим массу водорода:
\[ m(H_2) = n(H_2) \cdot M(H_2) = 1,1111 \text{ моль} \cdot 2 \text{ г/моль} \approx 2,2222 \text{ г} \]
Округляем результат до сотых, как того требует условие задачи.
Ответ: 2,22