Вот решение задачи, оформленное так, чтобы было удобно переписать в тетрадь школьнику:
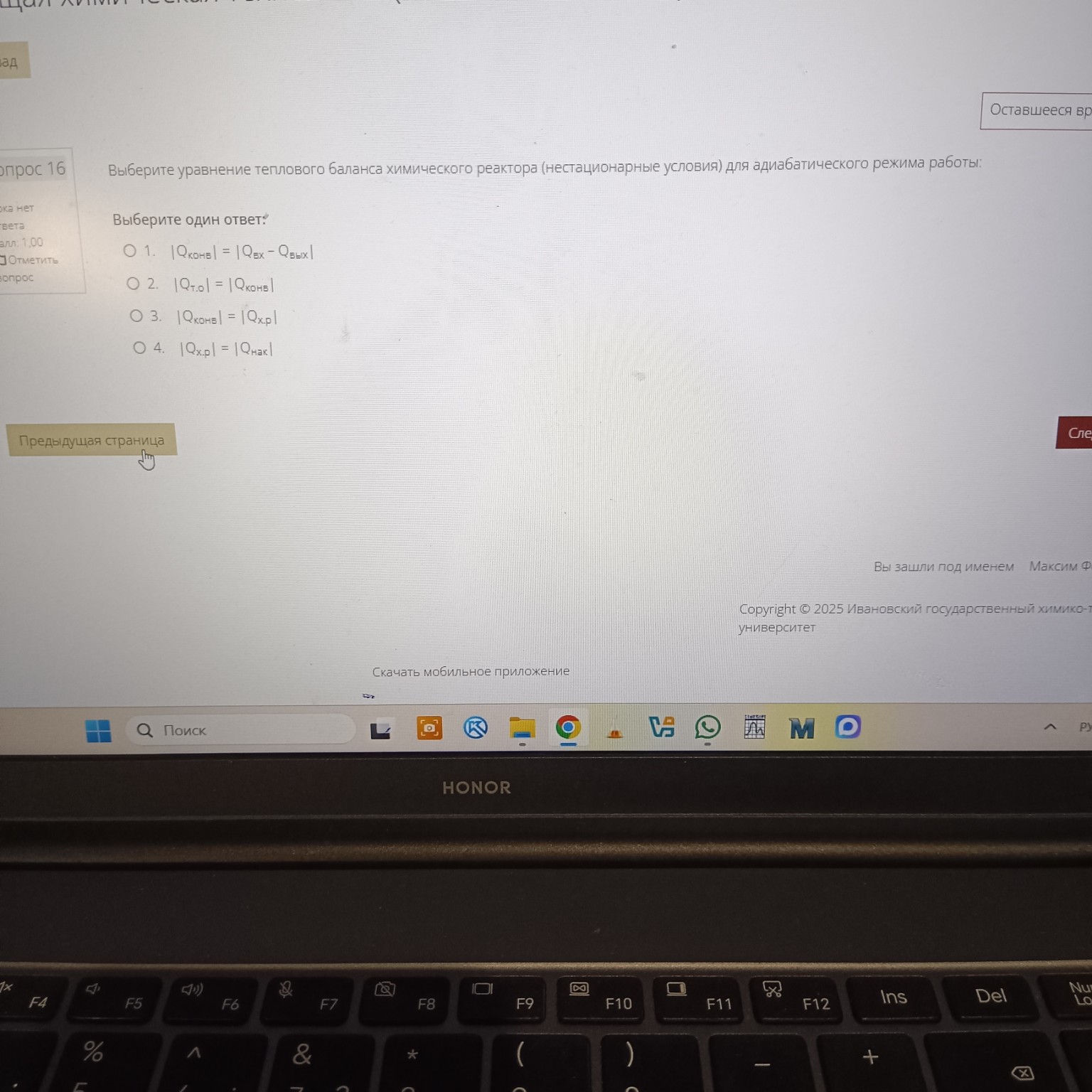
Выберите уравнение теплового баланса химического реактора (нестационарные условия) для адиабатического режима работы:
Выберите один ответ:
1. \( |\text{Q}_{\text{коне}}|=|\text{Q}_{\text{вх}}-\text{Q}_{\text{вых}}| \)
2. \( |\text{Q}_{\text{т.о}}|=|\text{Q}_{\text{конд}}| \)
3. \( |\text{Q}_{\text{коне}}|=|\text{Q}_{\text{х.р}}| \)
4. \( |\text{Q}_{\text{х.р}}|=|\text{Q}_{\text{нак}}| \)
Ответ:
Правильный ответ — 4. \( |\text{Q}_{\text{х.р}}|=|\text{Q}_{\text{нак}}| \)
Объяснение:
Тепловой баланс химического реактора основывается на законе сохранения энергии. Общее уравнение теплового баланса можно записать как:
\[ \text{Теплота, внесенная с потоками} + \text{Теплота, выделенная/поглощенная реакцией} + \text{Теплота, подведенная/отведенная извне} = \text{Теплота, вынесенная с потоками} + \text{Теплота, накопленная в системе} \]
Или в более компактном виде:
\[ \text{Q}_{\text{вх}} - \text{Q}_{\text{вых}} + \text{Q}_{\text{х.р}} + \text{Q}_{\text{т.о}} = \text{Q}_{\text{нак}} \]
Где:
* \( \text{Q}_{\text{вх}} \) — теплота, поступающая в реактор с входящими потоками.
* \( \text{Q}_{\text{вых}} \) — теплота, уходящая из реактора с выходящими потоками.
* \( \text{Q}_{\text{х.р}} \) — теплота, выделяющаяся (для экзотермической реакции) или поглощающаяся (для эндотермической реакции) в результате химической реакции.
* \( \text{Q}_{\text{т.о}} \) — теплота, подводимая или отводимая через теплообменные поверхности (например, рубашка охлаждения/нагрева).
* \( \text{Q}_{\text{нак}} \) — теплота, накапливающаяся в реакторе, приводящая к изменению температуры содержимого реактора.
Теперь рассмотрим условия, заданные в вопросе:
1. **Нестационарные условия**: Это означает, что \( \text{Q}_{\text{нак}} \neq 0 \). Температура и/или состав в реакторе меняются со временем, и происходит накопление или отвод теплоты.
2. **Адиабатический режим работы**: Это означает, что нет теплообмена с окружающей средой, то есть \( \text{Q}_{\text{т.о}} = 0 \). Также подразумевается, что нет тепловых потерь через стенки реактора.
3. **Реактор**: В данном контексте, если не указано иное, обычно подразумевается, что нет потоков входа и выхода (например, периодический реактор), или что их тепловой вклад незначителен по сравнению с теплотой реакции и накопления, или что они сбалансированы. Однако, если это проточный реактор, то \( \text{Q}_{\text{вх}} \) и \( \text{Q}_{\text{вых}} \) могут быть значительными. Но в контексте адиабатического реактора, где основное внимание уделяется изменению температуры за счет реакции, часто рассматривают баланс между теплотой реакции и накоплением.
Давайте проанализируем варианты, исходя из этих условий:
* **Адиабатический режим** означает, что \( \text{Q}_{\text{т.о}} = 0 \).
* Если речь идет о периодическом реакторе, то \( \text{Q}_{\text{вх}} = 0 \) и \( \text{Q}_{\text{вых}} = 0 \). Тогда уравнение теплового баланса упрощается до:
\[ \text{Q}_{\text{х.р}} = \text{Q}_{\text{нак}} \]
Это означает, что вся теплота, выделяющаяся или поглощающаяся в реакции, идет на изменение внутренней энергии (температуры) содержимого реактора.
* Если речь идет о проточном реакторе, но в адиабатическом режиме, то изменение энтальпии потоков ( \( \text{Q}_{\text{вх}} - \text{Q}_{\text{вых}} \) ) также должно быть учтено. Однако, в задачах такого типа, когда спрашивают про "тепловой баланс химического реактора (нестационарные условия) для адиабатического режима работы", часто подразумевается, что основным источником изменения температуры является теплота реакции, которая накапливается в системе.
Рассмотрим предложенные варианты:
1. \( |\text{Q}_{\text{коне}}|=|\text{Q}_{\text{вх}}-\text{Q}_{\text{вых}}| \) — это неполное уравнение, не учитывает теплоту реакции.
2. \( |\text{Q}_{\text{т.о}}|=|\text{Q}_{\text{конд}}| \) — \( \text{Q}_{\text{т.о}} \) — это теплообмен, а \( \text{Q}_{\text{конд}} \) — это теплота конденсации. Это уравнение не является общим тепловым балансом. К тому же, для адиабатического режима \( \text{Q}_{\text{т.о}} = 0 \).
3. \( |\text{Q}_{\text{коне}}|=|\text{Q}_{\text{х.р}}| \) — \( \text{Q}_{\text{коне}} \) не является стандартным обозначением для накопленной теплоты. Если это подразумевает накопленную теплоту, то это похоже на правильный ответ, но обозначение неточное.
4. \( |\text{Q}_{\text{х.р}}|=|\text{Q}_{\text{нак}}| \) — это уравнение прямо соответствует условиям: теплота, выделяющаяся/поглощающаяся в химической реакции (\( \text{Q}_{\text{х.р}} \)), полностью идет на накопление теплоты в системе (\( \text{Q}_{\text{нак}} \)), поскольку нет теплообмена с окружающей средой (адиабатический режим) и нет других значимых источников/стоков теплоты (или они сбалансированы). Модули используются, чтобы показать, что эти величины равны по абсолютному значению, независимо от того, выделяется теплота или поглощается.
Таким образом, наиболее точным и соответствующим условиям (нестационарный, адиабатический режим) является уравнение, где теплота реакции равна накопленной теплоте.
school
Общие знания
verified
Решено AI
Решение:
help_outline
Условие задачи
lightbulb
Краткий ответ
Подробное пошаговое решение представлено ниже.