school
Общие знания
verified
Решено AI
Решение:
help_outline
Условие задачи
lightbulb
Краткий ответ
Подробное пошаговое решение представлено ниже.
Подробное решение
Вот решение задачи, оформленное так, чтобы было удобно переписать в тетрадь школьнику. Формулы будут представлены в формате MathJax с использованием \( \) и \[ \].
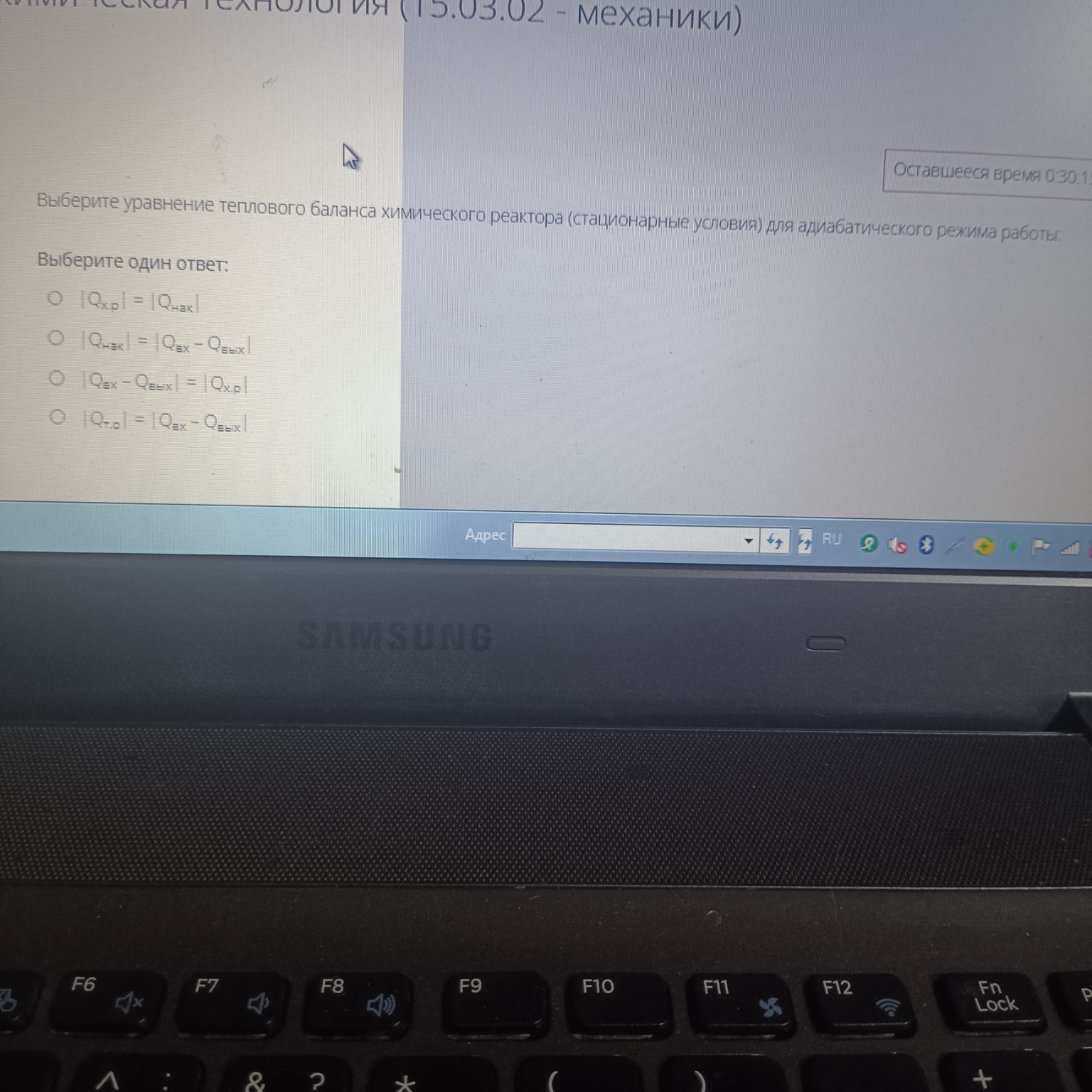
Вопрос: Выберите уравнение теплового баланса химического реактора (стационарные условия) для адиабатического режима работы.
Варианты ответов:
1. \( |Q_{х.р.}| = |Q_{нагр}| \)
2. \( |Q_{нагр}| = |Q_{вх} - Q_{вых}| \)
3. \( |Q_{вх} - Q_{вых}| = |Q_{х.р.}| \)
4. \( |Q_{т.о.}| = |Q_{вх} - Q_{вых}| \)
Правильный ответ:
\( |Q_{вх} - Q_{вых}| = |Q_{х.р.}| \)
Объяснение:
Давайте разберем основные понятия, необходимые для составления теплового баланса:
1. Тепловой баланс: Это закон сохранения энергии, примененный к тепловым процессам. Он гласит, что в системе изменение внутренней энергии равно сумме подведенного тепла и совершенной работы. Для стационарных процессов (когда параметры системы не меняются со временем) и без совершения работы, тепловой баланс сводится к равенству притока и оттока тепла.
2. Стационарные условия: Это означает, что все параметры внутри реактора (температура, концентрации, скорости потоков) не изменяются со временем.
3. Адиабатический режим работы: Это ключевое условие. Адиабатический процесс – это процесс, при котором отсутствует теплообмен с окружающей средой. То есть, реактор идеально теплоизолирован, и тепло не поступает извне и не уходит наружу через стенки реактора.
Обозначения:
* \( Q_{вх} \) – тепло, поступающее в реактор с входящими потоками реагентов.
* \( Q_{вых} \) – тепло, уходящее из реактора с выходящими потоками продуктов реакции.
* \( Q_{х.р.} \) – тепловой эффект химической реакции (тепло, выделяющееся или поглощающееся в результате реакции).
* \( Q_{нагр} \) – тепло, подводимое для нагрева (например, от внешнего источника).
* \( Q_{т.о.} \) – тепло, отводимое системой охлаждения (теплообменником).
Составим общий тепловой баланс для химического реактора в стационарных условиях:
\[ Q_{вх} + Q_{х.р.} + Q_{нагр} - Q_{вых} - Q_{т.о.} = 0 \]
Это уравнение означает, что сумма всех притоков тепла (с входящими потоками, от реакции, от нагревателя) должна быть равна сумме всех оттоков тепла (с выходящими потоками, к теплообменнику).
Теперь применим условия задачи:
* Стационарные условия: Уравнение выше уже составлено для стационарных условий.
* Адиабатический режим: Это означает, что нет теплообмена с окружающей средой. Следовательно, \( Q_{нагр} = 0 \) (нет внешнего нагрева) и \( Q_{т.о.} = 0 \) (нет внешнего охлаждения).
Подставляем эти условия в общее уравнение теплового баланса:
\[ Q_{вх} + Q_{х.р.} + 0 - Q_{вых} - 0 = 0 \]
\[ Q_{вх} + Q_{х.р.} - Q_{вых} = 0 \]
Перегруппируем члены уравнения, чтобы выразить тепловой эффект реакции через разность тепловых потоков:
\[ Q_{х.р.} = Q_{вых} - Q_{вх} \]
или
\[ Q_{вх} - Q_{вых} = -Q_{х.р.} \]
Поскольку в вариантах ответов используются абсолютные значения (модули), мы можем записать:
\[ |Q_{вх} - Q_{вых}| = |-Q_{х.р.}| \]
\[ |Q_{вх} - Q_{вых}| = |Q_{х.р.}| \]
Это уравнение показывает, что изменение энтальпии (теплосодержания) потоков, проходящих через реактор, равно тепловому эффекту химической реакции, протекающей в реакторе.
Сравним с предложенными вариантами:
1. \( |Q_{х.р.}| = |Q_{нагр}| \) – Неверно, так как нет нагрева в адиабатическом режиме.
2. \( |Q_{нагр}| = |Q_{вх} - Q_{вых}| \) – Неверно, так как нет нагрева.
3. \( |Q_{вх} - Q_{вых}| = |Q_{х.р.}| \) – Верно, соответствует нашему выводу.
4. \( |Q_{т.о.}| = |Q_{вх} - Q_{вых}| \) – Неверно, так как нет теплоотвода в адиабатическом режиме.
Таким образом, правильный ответ – третий вариант.