Получение инсулина биотехнологическим методом
1. Первое получение инсулина биотехнологическим методом
Первое получение человеческого инсулина с использованием методов генной инженерии стало одним из важнейших достижений биотехнологии. Это произошло в 1978 году, когда американская компания Genentech успешно клонировала ген человеческого инсулина и заставила бактерии производить этот белок. Коммерческое производство началось в 1982 году компанией Eli Lilly под торговой маркой "Хумулин".
До этого момента инсулин для лечения диабета получали из поджелудочных желез животных (свиней и крупного рогатого скота). Такой инсулин имел некоторые отличия от человеческого, что могло вызывать аллергические реакции и другие побочные эффекты у пациентов.
2. Впервые предложенный путь получения инсулина (на основе схемы)
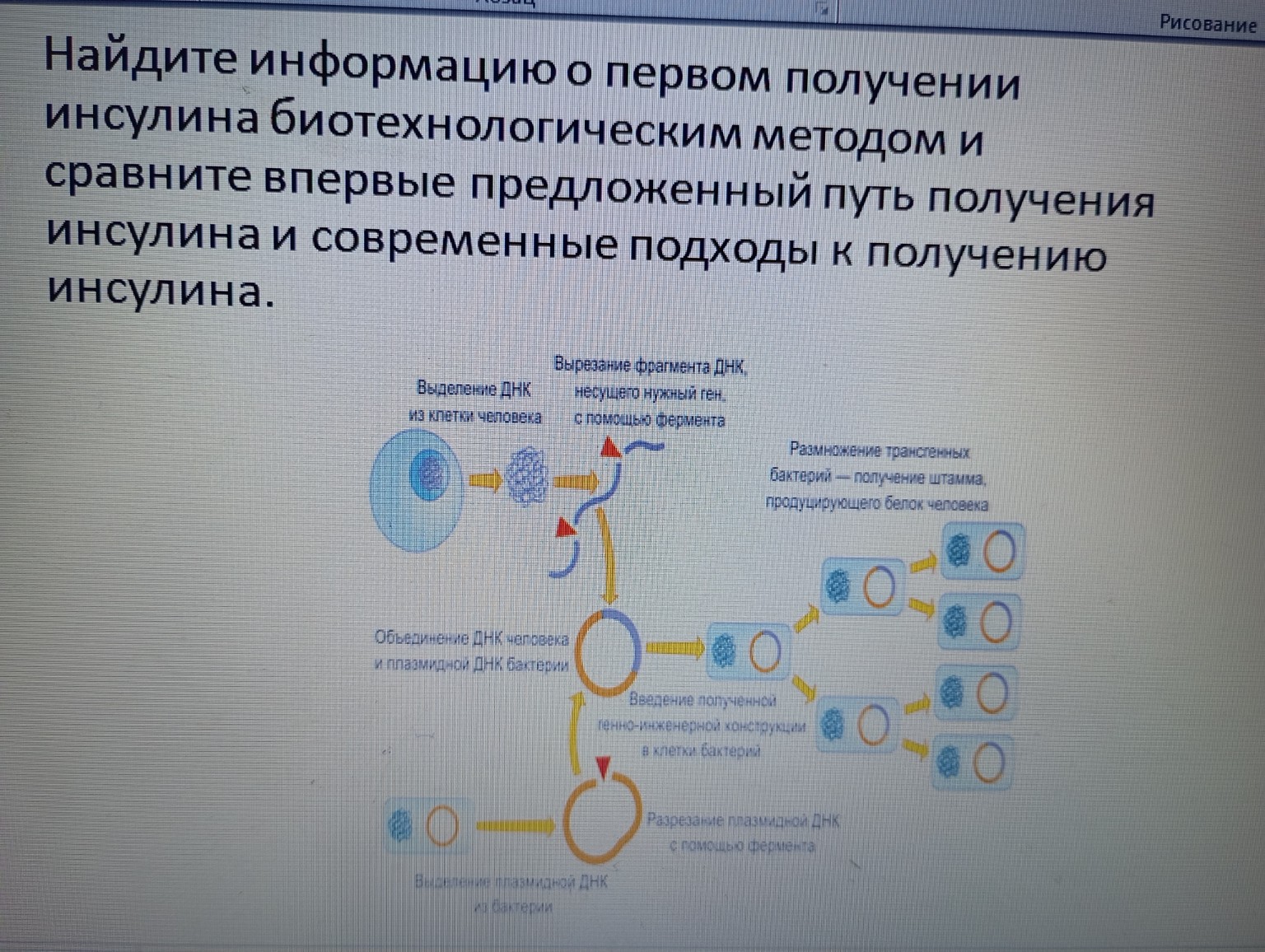
Схема, представленная на изображении, иллюстрирует классический подход к получению рекомбинантного белка, в данном случае инсулина. Давайте разберем его по шагам:
Выделение ДНК из клетки человека:
Из клеток человека (например, из клеток поджелудочной железы или других клеток, содержащих полный геном) выделяется общая ДНК.
Вырезание фрагмента ДНК, несущего нужный ген, с помощью фермента:
С помощью специальных ферментов, называемых рестриктазами, из человеческой ДНК вырезается ген, кодирующий инсулин. Эти ферменты разрезают ДНК в определенных местах, позволяя выделить нужный фрагмент.
Выделение плазмидной ДНК из бактерии:
Из бактериальной клетки (чаще всего используют кишечную палочку, Escherichia coli) выделяется плазмида – небольшая кольцевая молекула ДНК, которая существует отдельно от основного бактериального хромосомного ДНК и способна к автономной репликации.
Разрезание плазмидной ДНК с помощью фермента:
Ту же рестриктазу, которая использовалась для вырезания гена инсулина, применяют для разрезания плазмиды. Это создает "липкие концы" – одноцепочечные участки, которые комплементарны "липким концам" гена инсулина.
Объединение ДНК человека и плазмидной ДНК бактерии:
Ген инсулина человека встраивается в разрезанную плазмиду. Этот процесс катализируется ферментом ДНК-лигазой, которая "сшивает" фрагменты ДНК, образуя рекомбинантную плазмиду.
Введение полученной генно-инженерной конструкции в клетки бактерий:
Рекомбинантные плазмиды вводятся обратно в бактериальные клетки. Этот процесс называется трансформацией. Бактерии, поглотившие плазмиды, становятся трансгенными.
Размножение трансгенных бактерий – получение штамма, продуцирующего белок человека:
Трансгенные бактерии размножаются в больших количествах. Поскольку плазмида реплицируется вместе с бактериальной ДНК, каждая новая бактериальная клетка будет содержать рекомбинантную плазмиду с геном инсулина. Подходящие условия культивирования стимулируют бактерии к экспрессии гена инсулина, то есть к синтезу человеческого инсулина.
Выделение и очистка инсулина:
После культивирования бактерий инсулин выделяется из культуральной среды или из самих бактериальных клеток и подвергается многоступенчатой очистке для получения чистого лекарственного препарата.
3. Современные подходы к получению инсулина
Современные подходы к получению инсулина в целом следуют той же базовой схеме, что и описанный выше метод, но с рядом значительных усовершенствований и модификаций, направленных на повышение эффективности, безопасности и снижение стоимости производства:
Использование различных продуцентов:
Хотя Escherichia coli остается основным продуцентом, для производства инсулина также используются другие микроорганизмы, такие как дрожжи (например, Saccharomyces cerevisiae или Pichia pastoris). Дрожжи имеют преимущество в том, что они являются эукариотами и способны к посттрансляционным модификациям белков, что может быть важно для правильного сворачивания и активности инсулина. Кроме того, дрожжи часто секретируют белки в культуральную среду, что упрощает их выделение и очистку.
Оптимизация генных конструкций:
Современные генные конструкции (плазмиды) содержат оптимизированные промоторы (участки ДНК, регулирующие экспрессию гена), энхансеры и другие регуляторные элементы, которые обеспечивают максимально эффективную и стабильную экспрессию гена инсулина. Также используются синтетические гены, последовательность которых оптимизирована для экспрессии в конкретном организме-продуценте (например, с учетом предпочтений в использовании кодонов).
Производство проинсулина и его последующая модификация:
Человеческий инсулин синтезируется в виде проинсулина, который затем подвергается ферментативному расщеплению для удаления С-пептида и образования активного двухцепочечного инсулина. В современных методах часто производят проинсулин в бактериях или дрожжах, а затем проводят его ферментативную обработку in vitro для получения зрелого инсулина. Это позволяет избежать проблем с правильным сворачиванием и образованием дисульфидных связей, которые могут возникнуть при прямой экспрессии двух отдельных цепей инсулина.
Разработка аналогов инсулина:
Современная биотехнология позволяет не только производить человеческий инсулин, но и создавать его аналоги с измененными фармакокинетическими свойствами (например, быстродействующие или пролонгированные инсулины). Это достигается путем точечных мутаций в гене инсулина, которые изменяют аминокислотную последовательность белка, влияя на его абсорбцию, распределение и метаболизм в организме человека. Примеры таких аналогов – инсулин лизпро, аспарт, гларгин.
Усовершенствованные методы культивирования и очистки:
Используются биореакторы большого объема с точным контролем параметров культивирования (температура, pH, аэрация, подача питательных веществ) для максимизации выхода продукта. Методы очистки стали более эффективными и автоматизированными, включая различные виды хроматографии (ионообменная, гель-фильтрационная, аффинная) и ультрафильтрацию, что позволяет получать инсулин высокой степени чистоты, соответствующий фармацевтическим стандартам.
Контроль качества:
Строгий многоступенчатый контроль качества на всех этапах производства, от проверки исходных материалов до анализа конечного продукта, является неотъемлемой частью современных биотехнологических процессов. Это включает молекулярно-биологические, биохимические, иммунологические и физико-химические методы анализа.
Сравнение впервые предложенного пути и современных подходов
Хотя фундаментальные принципы генной инженерии остаются неизменными, современные подходы значительно усовершенствовали каждый этап процесса:
Эффективность:
Современные методы позволяют получать гораздо больший выход инсулина с единицы объема культуральной среды благодаря оптимизации продуцентов, генных конструкций и условий культивирования.
Качество и безопасность:
Усовершенствованные методы очистки и строгий контроль качества обеспечивают получение инсулина с минимальным содержанием примесей, что снижает риск побочных реакций у пациентов. Производство проинсулина и его последующая обработка также способствуют получению более нативного и активного белка.
Разнообразие продуктов:
Современные подходы позволяют не только производить человеческий инсулин, но и разрабатывать его аналоги с улучшенными фармакологическими свойствами, что расширяет возможности лечения диабета и позволяет индивидуализировать терапию.
Стоимость:
Несмотря на сложность технологий, масштабирование производства и оптимизация процессов в конечном итоге способствуют снижению себестоимости инсулина, делая его более доступным для пациентов по всему миру.
Технологии:
Использование более совершенных ферментов, векторов, систем экспрессии и аналитического оборудования делает процесс более точным и контролируемым.
Таким образом, впервые предложенный путь заложил основу, а современные подходы развили эту технологию до высокоэффективного, безопасного и гибкого метода производства жизненно важного лекарства.