schoolХимия
verifiedРешено AI
Решение задачи: 2H+ + CO32- = H2O + CO2↑
help_outlineУсловие задачи
lightbulbКраткий ответ
Для реакции 2H+ + CO32- = H2O + CO2↑ необходимы кислота (источник H+) и карбонат (источник CO32-). Подходящие реагенты: HNO3 и Na2CO3.
Подробное решение
Вот решение задачи, оформленное так, чтобы было удобно переписать в тетрадь школьнику:
Условие задания:
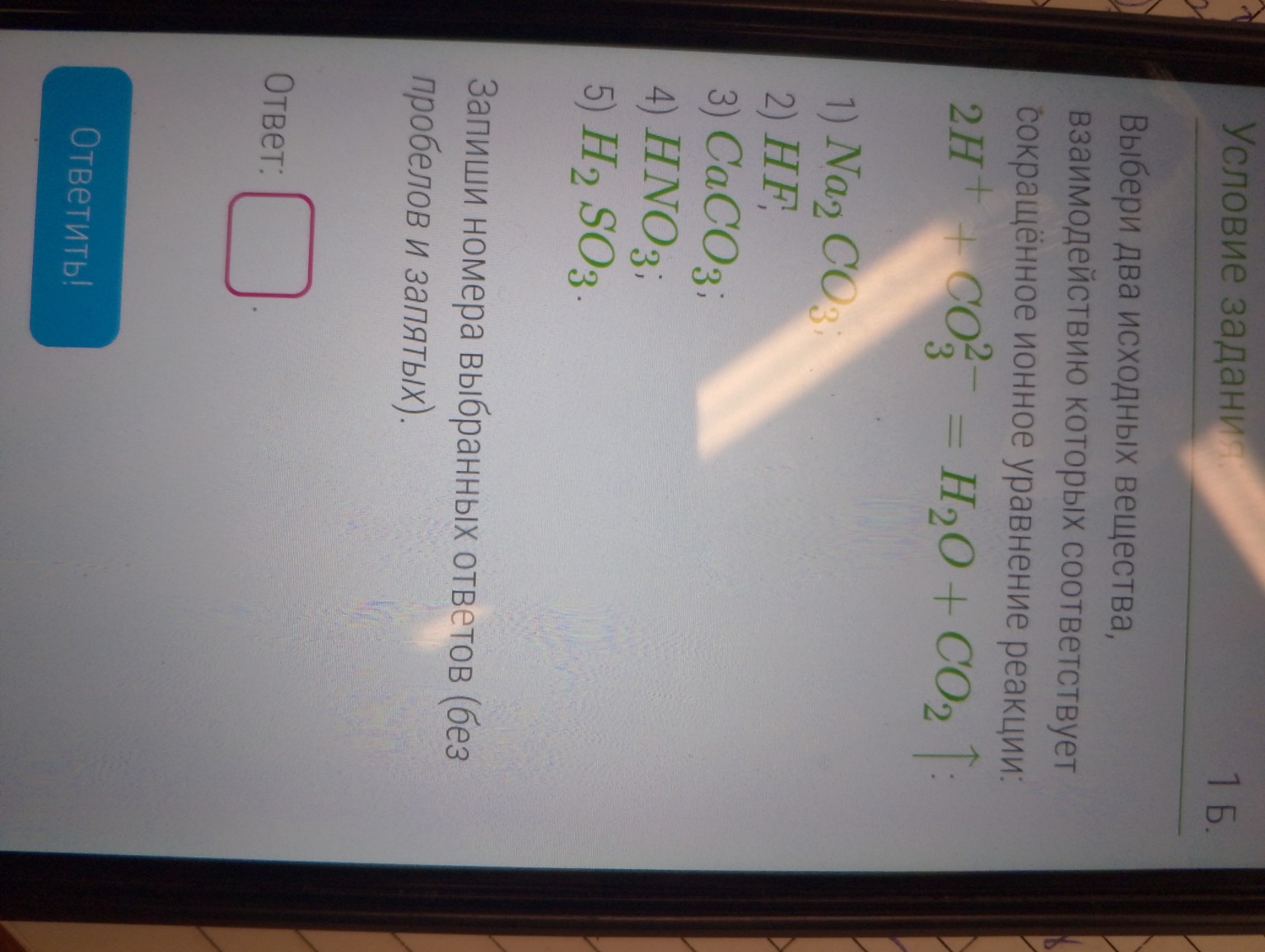
Выбери два исходных вещества, взаимодействие которых соответствует сокращённое ионное уравнение реакции:
\[2H^{+} + CO_{3}^{2-} = H_{2}O + CO_{2} \uparrow\]
Предложенные вещества:
1) \(Na_{2}CO_{3}\)
2) \(HF\)
3) \(CaCO_{3}\)
4) \(HNO_{3}\)
5) \(H_{2}SO_{3}\)
Решение:
Для того чтобы реакция соответствовала сокращённому ионному уравнению \[2H^{+} + CO_{3}^{2-} = H_{2}O + CO_{2} \uparrow\], нам нужны два исходных вещества:
1. Вещество, которое является источником ионов \(H^{+}\) (то есть кислота).
2. Вещество, которое является источником ионов \(CO_{3}^{2-}\) (то есть карбонат).
Рассмотрим предложенные варианты:
1) \(Na_{2}CO_{3}\) (карбонат натрия) – это растворимая соль, которая диссоциирует в воде на ионы \(2Na^{+}\) и \(CO_{3}^{2-}\). Это хороший источник ионов \(CO_{3}^{2-}\).
2) \(HF\) (фтороводородная кислота) – это слабая кислота. Она диссоциирует на ионы \(H^{+}\) и \(F^{-}\), но является слабой, поэтому не полностью.
3) \(CaCO_{3}\) (карбонат кальция) – это нерастворимая соль. Хотя она содержит ионы \(CO_{3}^{2-}\), она не диссоциирует в растворе в значительной степени, поэтому не является хорошим источником ионов \(CO_{3}^{2-}\) для реакции в растворе.
4) \(HNO_{3}\) (азотная кислота) – это сильная кислота. Она полностью диссоциирует в воде на ионы \(H^{+}\) и \(NO_{3}^{-}\). Это отличный источник ионов \(H^{+}\).
5) \(H_{2}SO_{3}\) (сернистая кислота) – это слабая кислота. Она диссоциирует на ионы \(H^{+}\) и \(SO_{3}^{2-}\), но является слабой.
Теперь выберем два вещества, которые дадут нам необходимые ионы:
* Для ионов \(H^{+}\) нам нужна сильная кислота. Подходит \(HNO_{3}\) (вариант 4).
* Для ионов \(CO_{3}^{2-}\) нам нужен растворимый карбонат. Подходит \(Na_{2}CO_{3}\) (вариант 1).
Проверим реакцию между \(Na_{2}CO_{3}\) и \(HNO_{3}\):
Молекулярное уравнение:
\[Na_{2}CO_{3} + 2HNO_{3} = 2NaNO_{3} + H_{2}O + CO_{2} \uparrow\]
Полное ионное уравнение:
\[2Na^{+} + CO_{3}^{2-} + 2H^{+} + 2NO_{3}^{-} = 2Na^{+} + 2NO_{3}^{-} + H_{2}O + CO_{2} \uparrow\]
Сокращённое ионное уравнение (после сокращения одинаковых ионов с обеих сторон):
\[2H^{+} + CO_{3}^{2-} = H_{2}O + CO_{2} \uparrow\]
Это соответствует заданному сокращённому ионному уравнению.
Таким образом, правильные исходные вещества – это \(Na_{2}CO_{3}\) и \(HNO_{3}\), что соответствует номерам 1 и 4.
Запиши номера выбранных ответов (без пробелов и запятых).
Ответ: 14