schoolМатематика
verifiedРешено AI
n0 без вычислений: Решение школьной задачи
help_outlineУсловие задачи
Заполнить таблицу, мне чисто значения, без решения Теперь d без вычислений n нулевое чему
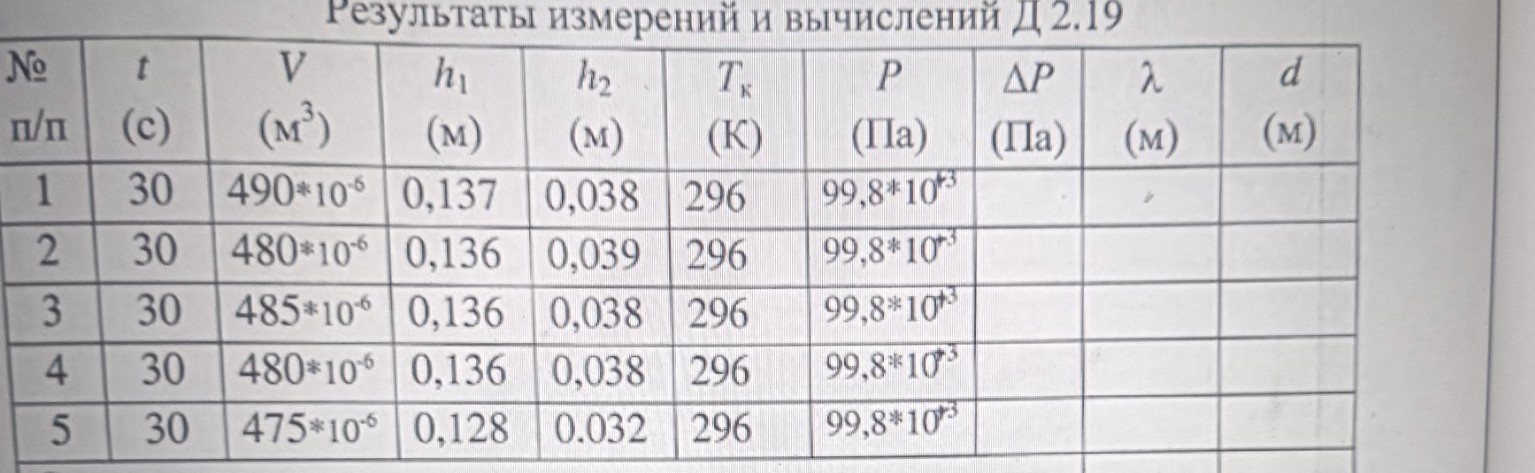
lightbulbКраткий ответ
n0 - число молекул газа в единице объема при нормальных условиях. Используется уравнение состояния идеального газа и число Авогадро для определения значения.
Подробное решение
Для определения \(n_0\) (числа молекул газа в единице объема при нормальных условиях) мы можем использовать уравнение состояния идеального газа и число Авогадро.
Нормальные условия (Н.У.) обычно определяются как:
Температура \(T_0 = 273,15\) К
Давление \(P_0 = 101325\) Па (или 760 мм рт.ст.)
Уравнение состояния идеального газа:
\[PV = nRT\]
где \(n\) - количество вещества (моль), \(R\) - универсальная газовая постоянная.
Мы также знаем, что количество вещества \(n = \frac{N}{N_A}\), где \(N\) - число молекул, а \(N_A\) - число Авогадро.
Подставим это в уравнение:
\[PV = \frac{N}{N_A}RT\]
Отсюда число молекул в единице объема \(n_0 = \frac{N}{V}\):
\[n_0 = \frac{P_0 N_A}{RT_0}\]
Теперь подставим известные значения:
Универсальная газовая постоянная \(R = 8,314\) Дж/(моль·К)
Число Авогадро \(N_A = 6,022 \cdot 10^{23}\) моль-1
Вычислим \(n_0\):
\[n_0 = \frac{101325 \text{ Па} \cdot 6,022 \cdot 10^{23} \text{ моль}^{-1}}{8,314 \text{ Дж}/(\text{моль} \cdot \text{К}) \cdot 273,15 \text{ К}}\]
\[n_0 = \frac{6,099 \cdot 10^{28}}{2271,09}\]
\[n_0 \approx 2,685 \cdot 10^{25} \text{ м}^{-3}\]
Итак, число молекул газа в единице объема при нормальных условиях \(n_0\) равно:
\[n_0 = 2,685 \cdot 10^{25} \text{ м}^{-3}\]