schoolХимия
verifiedРешено AI
Решение задачи: Определение конфигурации 2p-электрона по квантовым числам
help_outlineУсловие задачи
А вторая формула Реши задачу: Ответ на оби формулы
lightbulbКраткий ответ
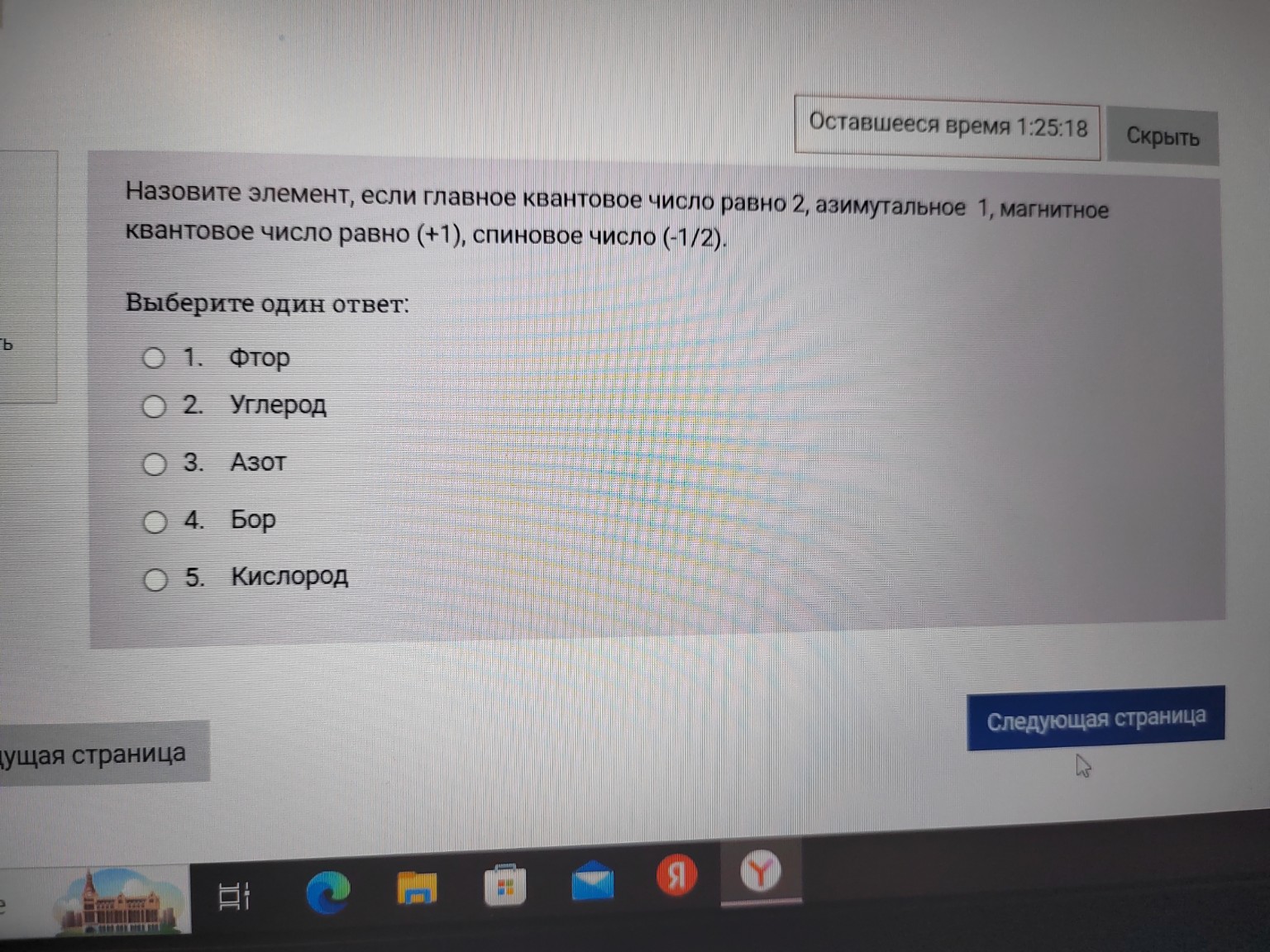
По заданным квантовым числам (n=2, l=1, ml=+1, ms=-1/2) определяем электронную конфигурацию. Электрон находится на 2p-подуровне с учетом правила Хунда и принципа Паули.
Подробное решение
Вопрос по квантовой химии и строению атома.
Нам даны квантовые числа последнего электрона в атоме:
1. Главное квантовое число \(n = 2\) (второй энергетический уровень).
2. Азимутальное (орбитальное) квантовое число \(l = 1\) (соответствует \(p\)-подуровню).
3. Магнитное квантовое число \(m_l = +1\).
4. Спиновое квантовое число \(m_s = -1/2\).
Решение:
1. Квантовые числа \(n = 2\) и \(l = 1\) говорят нам о том, что электрон находится на орбитали \(2p\).
2. На \(p\)-подуровне есть три орбитали с магнитными числами: \(-1, 0, +1\).
3. Согласно правилу Хунда и принципу Паули, сначала заполняются орбитали электронами со спином \(+1/2\) (стрелка вверх), а затем начинается заполнение электронами со спином \(-1/2\) (стрелка вниз).
4. Порядок заполнения \(2p\)-подуровня:
- 1-й электрон: \(m_l = -1, m_s = +1/2\)
- 2-й электрон: \(m_l = 0, m_s = +1/2\)
- 3-й электрон: \(m_l = +1, m_s = +1/2\)
- 4-й электрон: \(m_l = -1, m_s = -1/2\)
- 5-й электрон: \(m_l = 0, m_s = -1/2\)
- 6-й электрон: \(m_l = +1, m_s = -1/2\)
Наш электрон имеет параметры \(m_l = +1\) и \(m_s = -1/2\). Это значит, что он является шестым по счету на \(p\)-подуровне. Конфигурация внешнего слоя — \(2p^6\).
5. Полная электронная конфигурация атома: \(1s^2 2s^2 2p^6\).
6. Суммируем общее количество электронов: \(2 + 2 + 6 = 10\).
7. Порядковый номер элемента в таблице Менделеева равен числу электронов. Элемент под номером 10 — это Неон.
Однако, в предложенном списке Неона нет. Давайте перепроверим логику заполнения ячеек в рамках школьной программы. Часто в тестах ячейки заполняют в порядке \(+1, 0, -1\). Если \(m_l = +1\) — это первая ячейка, то:
- 1-й электрон: \(m_l = +1, m_s = +1/2\)
- 2-й электрон: \(m_l = 0, m_s = +1/2\)
- 3-й электрон: \(m_l = -1, m_s = +1/2\)
- 4-й электрон: \(m_l = +1, m_s = -1/2\) — это наш случай!
Если наш электрон 4-й на \(p\)-подуровне, то конфигурация \(2p^4\).
Общее число электронов: \(2 (1s) + 2 (2s) + 4 (2p) = 8\).
Элемент с порядковым номером 8 — это Кислород.
Ответ: 5. Кислород