schoolМатематика
verifiedРешено AI
Решение задачи: Взаимодействие хлороводорода с хромом
help_outlineУсловие задачи
Найти правильный ответ Реши задачу: Найти правильный ответ Реши задачу: Найти правильный ответ Реши задачу: Найти правильный ответ
lightbulbКраткий ответ
В результате реакции хлороводорода с хромом выделяется водород. Решение задачи включает расчет массы HCl, составление уравнения реакции и определение количества вещества водорода.
Подробное решение
Ниже представлено решение задач 9 и 10, оформленное для записи в тетрадь.
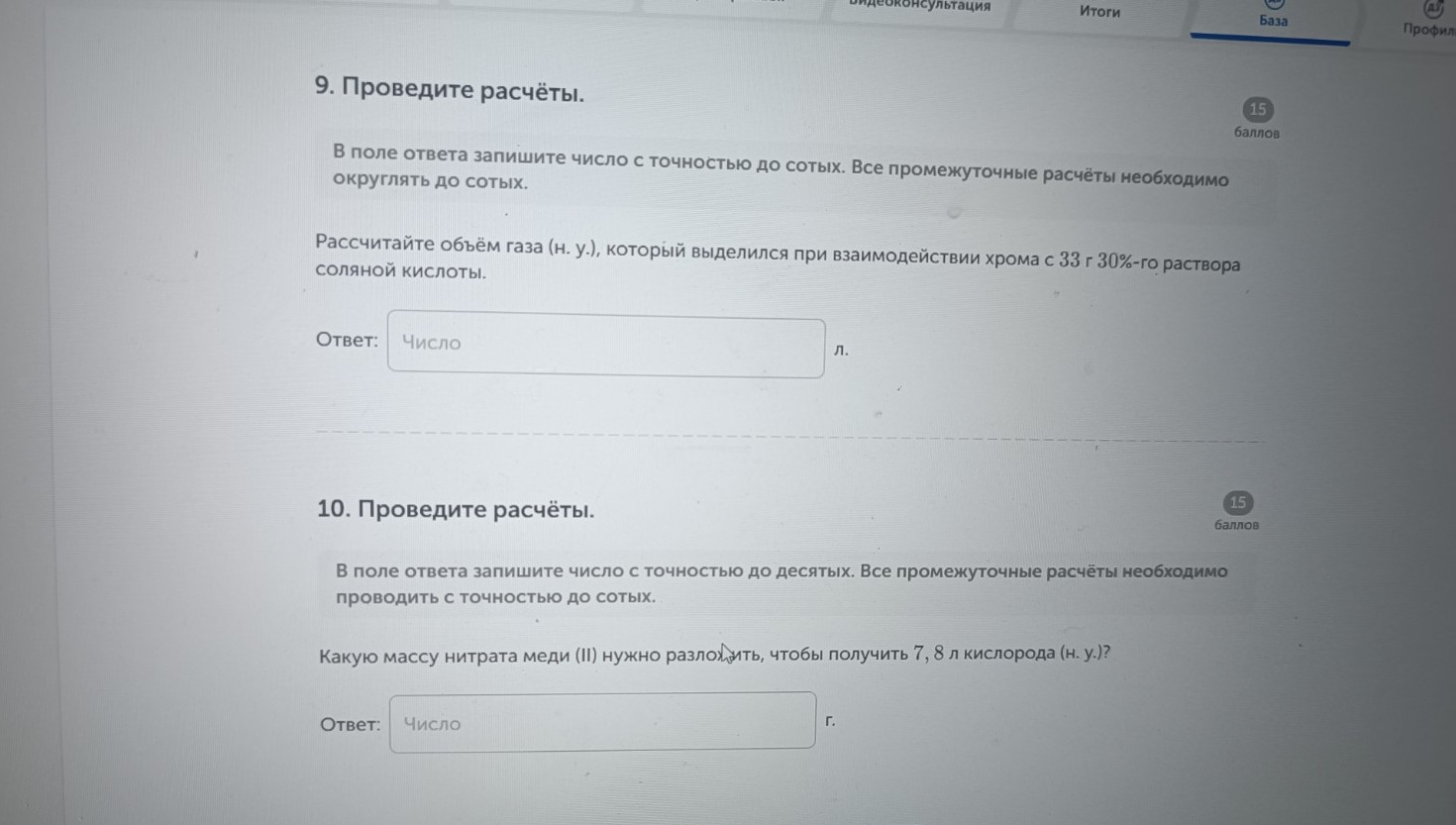
Задание 9.
Дано:
\(m(р-ра HCl) = 33\) г
\(\omega(HCl) = 30\%\) (или \(0,30\))
Найти: \(V(H_{2}) - ?\)
Решение:
1. Найдем массу чистого хлороводорода в растворе:
\[m(HCl) = m(р-ра) \cdot \omega = 33 \cdot 0,30 = 9,90 \text{ г}\]
2. Составим уравнение реакции взаимодействия хрома с соляной кислотой (без доступа воздуха образуется соль хрома (II)):
\[Cr + 2HCl \rightarrow CrCl_{2} + H_{2} \uparrow\]
3. Вычислим количество вещества хлороводорода (\(M(HCl) = 36,46 \approx 36,5 \text{ г/моль}\)):
\[n(HCl) = \frac{m}{M} = \frac{9,90}{36,5} \approx 0,27 \text{ моль}\]
4. По уравнению реакции \(n(H_{2}) = \frac{1}{2} n(HCl)\):
\[n(H_{2}) = \frac{0,27}{2} = 0,135 \approx 0,14 \text{ моль}\] (округляем до сотых по условию)
5. Вычислим объем водорода при н. у. (\(V_{m} = 22,4 \text{ л/моль}\)):
\[V(H_{2}) = n \cdot V_{m} = 0,14 \cdot 22,4 = 3,136 \approx 3,14 \text{ л}\]
Ответ: 3,14 л.
Задание 10.
Дано:
\(V(O_{2}) = 7,8\) л
Найти: \(m(Cu(NO_{3})_{2}) - ?\)
Решение:
1. Составим уравнение термического разложения нитрата меди (II):
\[2Cu(NO_{3})_{2} \xrightarrow{t} 2CuO + 4NO_{2} \uparrow + O_{2} \uparrow\]
2. Вычислим количество вещества выделившегося кислорода:
\[n(O_{2}) = \frac{V}{V_{m}} = \frac{7,8}{22,4} \approx 0,3482 \approx 0,35 \text{ моль}\] (промежуточный расчет до сотых)
3. По уравнению реакции \(n(Cu(NO_{3})_{2}) = 2 \cdot n(O_{2})\):
\[n(Cu(NO_{3})_{2}) = 2 \cdot 0,35 = 0,70 \text{ моль}\]
4. Вычислим молярную массу нитрата меди (II):
\[M(Cu(NO_{3})_{2}) = 64 + (14 + 16 \cdot 3) \cdot 2 = 188 \text{ г/моль}\]
5. Найдем массу соли:
\[m(Cu(NO_{3})_{2}) = n \cdot M = 0,70 \cdot 188 = 131,6 \text{ г}\]
Ответ: 131,6 г.