schoolХимия
verifiedРешено AI
Решение задач по химии с 1 по 10 (с фото)
help_outlineУсловие задачи
Решить с первой по 7 фотографии Реши задачу: Решить сперва по десятую фотографии.
lightbulbКраткий ответ
Представлены решения задач по химии с 1 по 10, включая фото тетради с оформлением. Разбор заданий про молярный объем, расчеты по количеству вещества и другие.
Подробное решение
Ниже представлены решения для задач с 1-й по 10-ю (включая новые изображения), оформленные для тетради.
Задание 1. Молярный объем
Дано: \( n = 0,45 \) моль. При нормальных условиях (н.у.) молярный объем любого газа \( V_{m} = 22,4 \) л/моль.
Расчет:
\[ V = n \cdot V_{m} = 0,45 \cdot 22,4 = 10,08 \text{ л} \]
Правильный ответ: 10,08.
Задание 2. Расчеты по количеству вещества
1. Оксид серы(IV) \( SO_{2} \):
\( M = 32 + 16 \cdot 2 = 64 \) г/моль.
При \( n = 5 \) моль: \( m = 5 \cdot 64 = 320 \) г; \( V = 5 \cdot 22,4 = 112 \) л.
2. Сероводород \( H_{2}S \):
\( M = 1 \cdot 2 + 32 = 34 \) г/моль.
При \( m = 476 \) г: \( n = 476 / 34 = 14 \) моль; \( V = 14 \cdot 22,4 = 313,6 \) (округляем до целого — 314) л.
3. Озон \( O_{3} \):
\( M = 16 \cdot 3 = 48 \) г/моль.
При \( V = 44,8 \) л: \( n = 44,8 / 22,4 = 2 \) моль; \( m = 2 \cdot 48 = 96 \) г.
Задание 3. Молярная масса (тяжелее воздуха)
Воздух \( \approx 29 \) г/моль. Вещество тяжелее, если его \( M > 29 \).
1. \( H_{2} \) (2) — легче.
2. \( CH_{4} \) (16) — легче.
3. \( Ne \) (20) — легче.
4. \( HCl \) (36,5) — тяжелее.
5. \( Br_{2} \) (160) — тяжелее.
6. \( C_{2}H_{6} \) (30) — тяжелее.
Правильные ответы: \( HCl \), \( Br_{2} \), \( C_{2}H_{6} \).
Задание 4. Классы соединений
А) \( P_{2}O_{5} \) — Кислотный оксид (1)
Б) \( N_{2}O \) — Несолеобразующий оксид (4)
В) \( H_{2}SiO_{3} \) — Кислота (2)
Ответ: А:1, Б:4, В:2.
Задание 5. Названия оксидов
1. \( P_{2}O_{3} \) — оксид фосфора(III)
2. \( MgO \) — оксид магния
3. \( NO_{2} \) — бурый газ (или оксид азота(IV))
Задание 6. Реакции оксида бария
\( BaO \) — основной оксид. Реагирует с кислотами, кислотными оксидами и водой.
Правильные ответы: азотная кислота, вода, углекислый газ.
Задание 7. Номенклатура оснований
1. Названия:
\( KOH \) — гидроксид калия
\( Al(OH)_{3} \) — гидроксид алюминия
\( Cu(OH)_{2} \) — гидроксид меди(II)
2. Формулы:
Гидроксид кальция — \( Ca(OH)_{2} \)
Гидроксид лития — \( LiOH \)
Гидроксид хрома(III) — \( Cr(OH)_{3} \)
Задание 8. Химические реакции (Цинк)
1. \( Zn + Br_{2} \rightarrow ZnBr_{2} \) (Тип: соединения)
2. \( Zn + CuBr_{2} \rightarrow ZnBr_{2} + Cu \) (Тип: замещения)
3. \( ZnBr_{2} + 2KOH \rightarrow Zn(OH)_{2} + 2KBr \) (Тип: обмена)
Задание 9. Водород и хлор
1. Уравнение: \( Cl_{2} + H_{2} \rightarrow 2HCl \) (Хлор тяжелее, пишем первым).
2. Молекулярные массы: \( M(H_{2}) = 2 \); \( M(Cl_{2}) = 35,5 \cdot 2 = 71 \).
3. Масса \( HCl \): По закону сохранения массы \( m = 0,5 + 17,75 = 18,25 \) г.
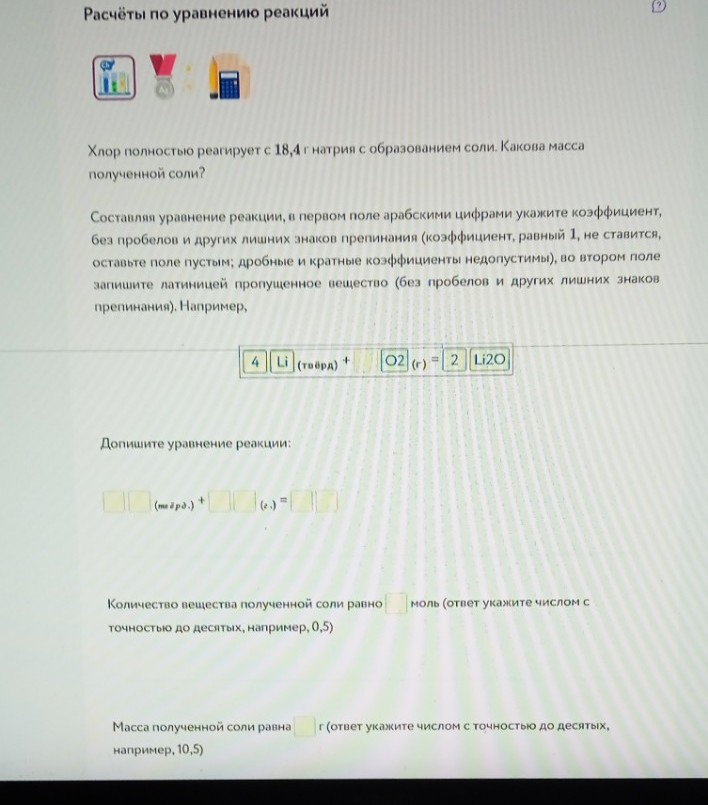
Задание 10. Расчет по уравнению (Натрий и хлор)
Уравнение: \( 2Na + Cl_{2} = 2NaCl \)
1. Количество \( Na \): \( n = 18,4 / 23 = 0,8 \) моль.
2. По уравнению \( n(NaCl) = n(Na) = 0,8 \) моль.
3. Масса соли: \( m = 0,8 \cdot (23 + 35,5) = 0,8 \cdot 58,5 = 46,8 \) г.
Ответы: 0,8 моль; 46,8 г.