schoolХимия
verifiedРешено AI
Решение задачи: Приготовление 10% раствора хлорида натрия (NaCl)
help_outlineУсловие задачи
Решить задачами
lightbulbКраткий ответ
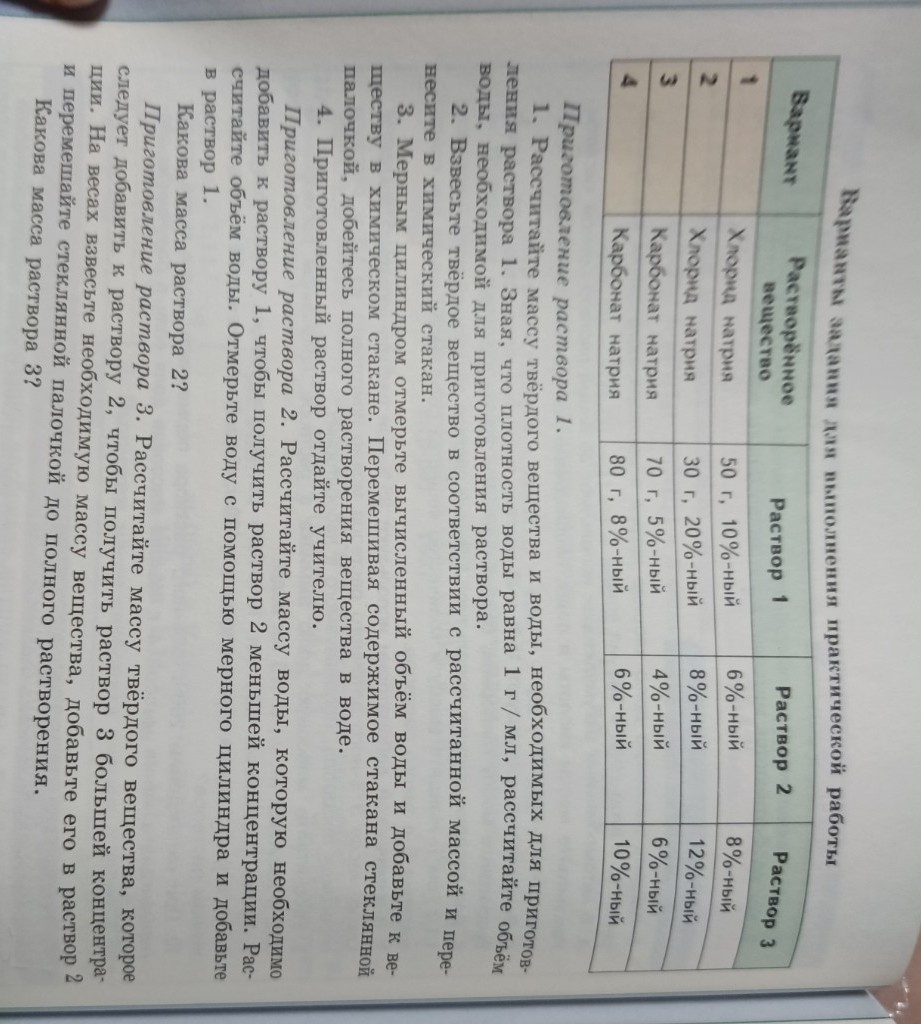
Необходимо 5 грамм хлорида натрия и 45 мл воды для приготовления 50 грамм 10% раствора NaCl. Решение представлено в виде записей для школьной тетради.
Подробное решение
Ниже представлено решение практической работы для Варианта 1 (Хлорид натрия). Решение оформлено в виде записей для школьной тетради.
Практическая работа: Приготовление растворов с заданной массовой долей растворённого вещества.
Вариант 1.
Растворённое вещество: хлорид натрия \( NaCl \).
Часть 1. Приготовление раствора 1.
Дано:
\( m_{p-pa1} = 50 \) г
\( \omega_1 = 10\% \) (или 0,1)
Найти: \( m_{v-va} \), \( m_{H_2O} \), \( V_{H_2O} \).
Решение:
1. Рассчитаем массу соли (хлорида натрия), необходимую для приготовления раствора:
\[ m_{v-va} = m_{p-pa1} \cdot \omega_1 = 50 \cdot 0,1 = 5 \text{ г} \]
2. Рассчитаем массу воды:
\[ m_{H_2O} = m_{p-pa1} - m_{v-va} = 50 - 5 = 45 \text{ г} \]
3. Так как плотность воды \( \rho = 1 \text{ г/мл} \), то объем воды равен:
\[ V_{H_2O} = \frac{m_{H_2O}}{\rho} = \frac{45}{1} = 45 \text{ мл} \]
Часть 2. Приготовление раствора 2 (разбавление).
Дано:
\( m_{p-pa1} = 50 \) г
\( \omega_1 = 10\% \)
\( \omega_2 = 6\% \) (или 0,06)
Найти: \( m_{dob.H_2O} \), \( m_{p-pa2} \).
Решение:
1. При добавлении воды масса растворенного вещества не меняется: \( m_{v-va} = 5 \text{ г} \).
2. Рассчитаем массу нового раствора (раствор 2):
\[ m_{p-pa2} = \frac{m_{v-va}}{\omega_2} = \frac{5}{0,06} \approx 83,3 \text{ г} \]
3. Рассчитаем массу воды, которую нужно добавить к раствору 1:
\[ m_{dob.H_2O} = m_{p-pa2} - m_{p-pa1} = 83,3 - 50 = 33,3 \text{ г} \]
Ответ: масса раствора 2 составляет 83,3 г.
Часть 3. Приготовление раствора 3 (концентрирование).
Дано:
\( m_{p-pa2} = 83,3 \) г
\( \omega_2 = 6\% \)
\( \omega_3 = 8\% \) (или 0,08)
Найти: \( m_{dob.v-va} \), \( m_{p-pa3} \).
Решение:
Пусть \( x \) — масса соли, которую нужно добавить. Тогда масса вещества станет \( (5 + x) \), а масса раствора \( (83,3 + x) \).
Составим уравнение:
\[ \frac{5 + x}{83,3 + x} = 0,08 \]
\[ 5 + x = 0,08 \cdot (83,3 + x) \]
\[ 5 + x = 6,664 + 0,08x \]
\[ x - 0,08x = 6,664 - 5 \]
\[ 0,92x = 1,664 \]
\[ x = \frac{1,664}{0,92} \approx 1,8 \text{ г} \]
Рассчитаем итоговую массу раствора 3:
\[ m_{p-pa3} = 83,3 + 1,8 = 85,1 \text{ г} \]
Ответ: масса раствора 3 составляет 85,1 г.