schoolМатематика
verifiedРешено AI
Решение задачи: Описание процесса на графике P-V
help_outlineУсловие задачи
Решите график, описывая процесс
lightbulbКраткий ответ
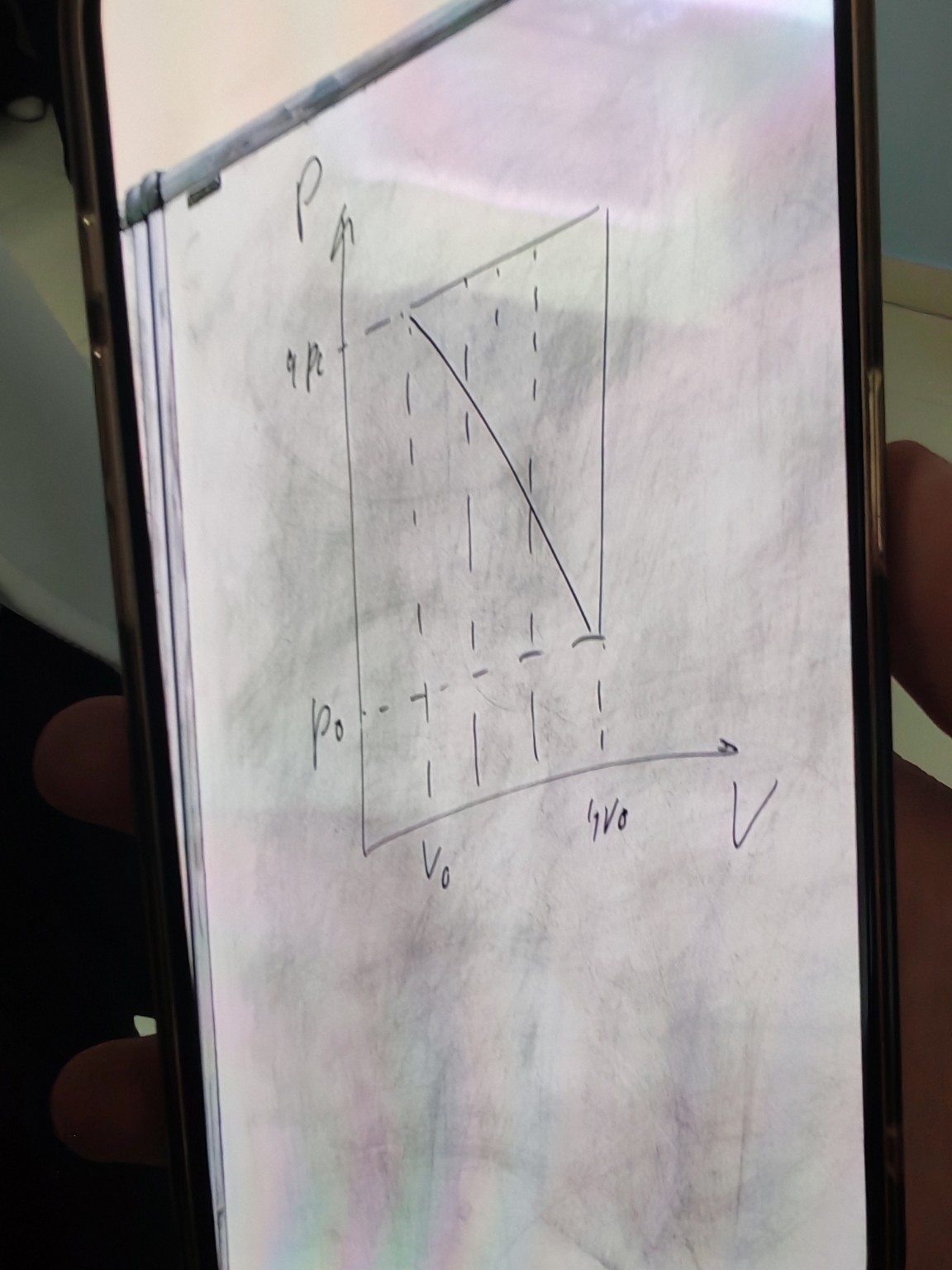
На графике представлен линейный процесс изменения состояния идеального газа. Уравнение процесса: P(V) = -P₀/V₀ * V + 5P₀.
Подробное решение
На графике представлен процесс изменения состояния идеального газа в осях \(P\) (давление) и \(V\) (объем). Процесс изображен в виде прямой линии, соединяющей две точки.
Дано:
Начальное состояние (точка 1): \(V_1 = V_0\), \(P_1 = 4P_0\).
Конечное состояние (точка 2): \(V_2 = 4V_0\), \(P_2 = P_0\).
1. Описание процесса:
Данный процесс является линейным. Уравнение прямой в осях \(P-V\) можно записать в виде:
\[ P(V) = kV + b \]
Подставим значения координат точек, чтобы найти коэффициенты:
Для точки 1: \(4P_0 = k \cdot V_0 + b\)
Для точки 2: \(P_0 = k \cdot 4V_0 + b\)
Вычтем из первого уравнения второе:
\[ 3P_0 = -3kV_0 \implies k = -\frac{P_0}{V_0} \]
Теперь найдем \(b\):
\[ 4P_0 = -\frac{P_0}{V_0} \cdot V_0 + b \implies b = 5P_0 \]
Таким образом, уравнение процесса имеет вид:
\[ P(V) = -\frac{P_0}{V_0}V + 5P_0 \]
2. Работа газа (\(A\)):
Работа газа в термодинамике численно равна площади фигуры под графиком процесса в осях \(P-V\). В данном случае это прямоугольная трапеция.
\[ A = \frac{P_1 + P_2}{2} \cdot (V_2 - V_1) \]
Подставим значения:
\[ A = \frac{4P_0 + P_0}{2} \cdot (4V_0 - V_0) = \frac{5P_0}{2} \cdot 3V_0 = 7,5 P_0 V_0 \]
3. Изменение температуры:
Используя уравнение Менделеева-Клапейрона \(PV = \nu RT\), определим температуру в начале и в конце:
\[ T_1 = \frac{P_1 V_1}{\nu R} = \frac{4P_0 V_0}{\nu R} \]
\[ T_2 = \frac{P_2 V_2}{\nu R} = \frac{P_0 \cdot 4V_0}{\nu R} = \frac{4P_0 V_0}{\nu R} \]
Так как \(T_1 = T_2\), то изменение внутренней энергии газа в этом полном процессе равно нулю (\(\Delta U = 0\)). Однако это не изотермический процесс, так как график — прямая, а не гипербола. В середине процесса температура сначала увеличивается, а затем уменьшается до исходного значения.
4. Максимальная температура:
Температура \(T \sim PV\). Найдем максимум функции \(f(V) = P(V) \cdot V\):
\[ f(V) = \left(-\frac{P_0}{V_0}V + 5P_0\right)V = -\frac{P_0}{V_0}V^2 + 5P_0 V \]
Производная по \(V\):
\[ f'(V) = -2\frac{P_0}{V_0}V + 5P_0 = 0 \implies V_{max} = 2,5 V_0 \]
Максимальная температура достигается при объеме \(2,5 V_0\).
Ответ: Процесс представляет собой линейное расширение газа с уменьшением давления. Работа, совершенная газом, составляет \(7,5 P_0 V_0\). Начальная и конечная температуры газа равны.