schoolФизика
verifiedРешено AI
Решение задачи: График расширения идеального газа
help_outlineУсловие задачи
Решите график по физике
lightbulbКраткий ответ
Найдена работа газа A и изменение внутренней энергии ΔU для процесса расширения идеального газа, представленного графиком в координатах P-V. Работа газа равна площади под графиком, а изменение внутренней энергии вычисляется на основе начального и конечного состояний.
Подробное решение
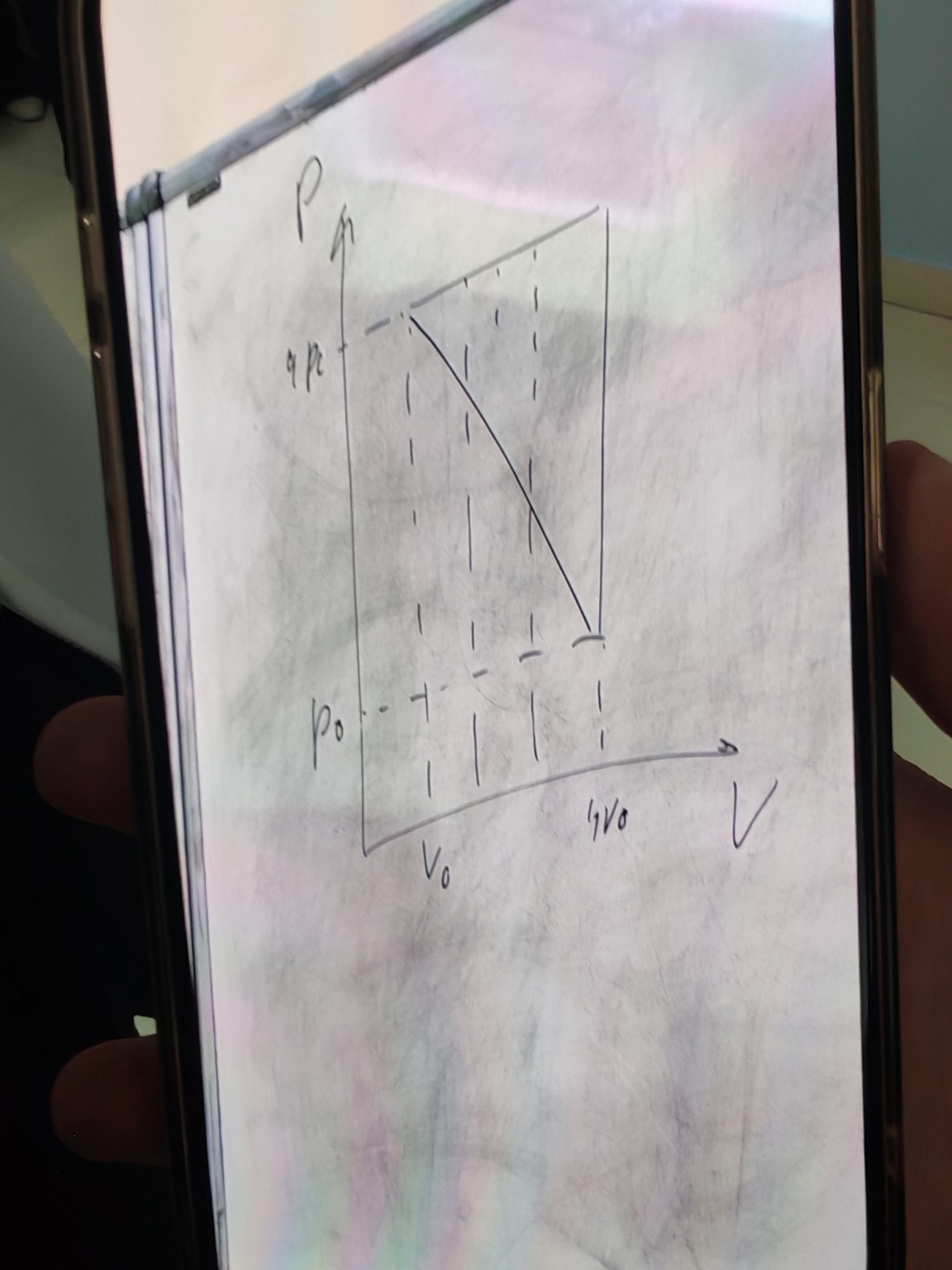
На графике представлен процесс расширения идеального газа, изображенный прямой линией в координатах \(P\) (давление) и \(V\) (объем).
Дано:
Начальное состояние (точка 1): \(P_1 = 4P_0\), \(V_1 = V_0\).
Конечное состояние (точка 2): \(P_2 = P_0\), \(V_2 = 4V_0\).
Обычно в таких задачах требуется найти работу газа \(A\), изменение внутренней энергии \(\Delta U\) или количество теплоты \(Q\). Решим задачу в общем виде для этих величин.
1. Работа газа \(A\):
Работа газа численно равна площади фигуры под графиком процесса в осях \(P-V\). В данном случае это прямоугольная трапеция.
\[A = \frac{P_1 + P_2}{2} \cdot (V_2 - V_1)\]
Подставим значения:
\[A = \frac{4P_0 + P_0}{2} \cdot (4V_0 - V_0) = \frac{5P_0}{2} \cdot 3V_0 = 7,5 P_0 V_0\]
2. Изменение внутренней энергии \(\Delta U\):
Для одноатомного идеального газа формула имеет вид:
\[\Delta U = \frac{3}{2} (P_2 V_2 - P_1 V_1)\]
Подставим значения:
\[\Delta U = \frac{3}{2} (P_0 \cdot 4V_0 - 4P_0 \cdot V_0) = \frac{3}{2} (4P_0 V_0 - 4P_0 V_0) = 0\]
Так как произведение давления на объем в начале и в конце одинаково (\(4P_0 V_0\)), то начальная и конечная температуры равны (\(T_1 = T_2\)), и внутренняя энергия не изменилась.
3. Количество теплоты \(Q\):
По первому закону термодинамики:
\[Q = \Delta U + A\]
\[Q = 0 + 7,5 P_0 V_0 = 7,5 P_0 V_0\]
Ответ: Работа газа составляет \(7,5 P_0 V_0\), изменение внутренней энергии равно \(0\), полученное количество теплоты равно \(7,5 P_0 V_0\).