schoolМатематика
verifiedРешено AI
Решение задачи по химии: Fe2O3 + H2 → Fe + H2O
help_outlineУсловие задачи
Решите задачу по химии 8 класс
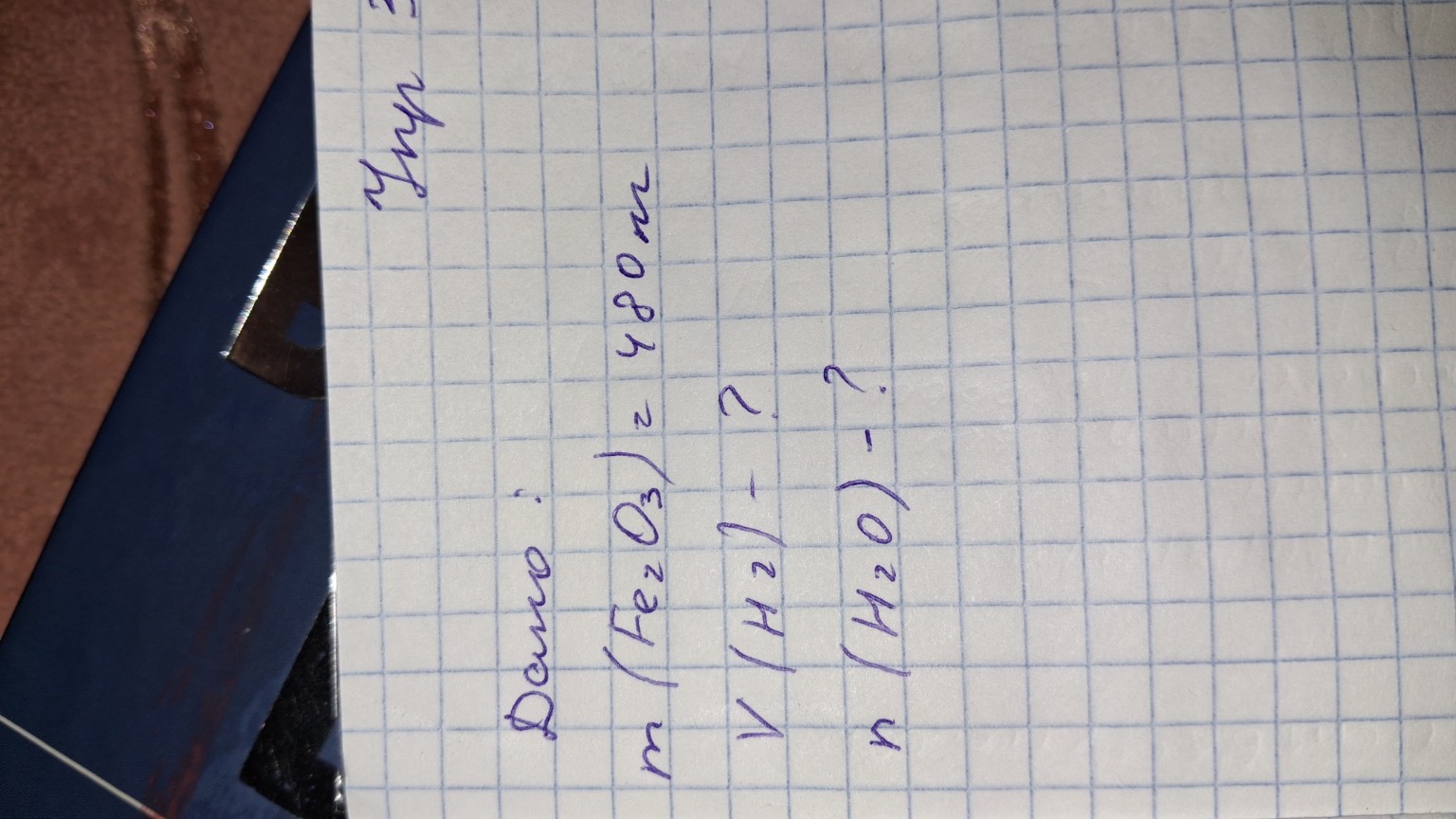
lightbulbКраткий ответ
В результате реакции оксида железа (III) с водородом образуется железо и вода. Для восстановления 0.48 г Fe2O3 требуется определенный объем водорода, который рассчитывается по уравнению реакции.
Подробное решение
Дано:
\(m(Fe_{2}O_{3}) = 480\) мг
Найти:
\(V(H_{2}) - ?\)
\(n(H_{2}O) - ?\)
Решение:
1. Переведем массу оксида железа (III) из миллиграммов в граммы:
\[m(Fe_{2}O_{3}) = 480 \text{ мг} = 0,48 \text{ г}\]
2. Запишем уравнение реакции восстановления железа водородом:
\[Fe_{2}O_{3} + 3H_{2} \rightarrow 2Fe + 3H_{2}O\]
3. Вычислим молярную массу оксида железа (III):
\[M(Fe_{2}O_{3}) = 2 \cdot 56 + 3 \cdot 16 = 112 + 48 = 160 \text{ г/моль}\]
4. Найдем количество вещества оксида железа (III):
\[n(Fe_{2}O_{3}) = \frac{m}{M} = \frac{0,48 \text{ г}}{160 \text{ г/моль}} = 0,003 \text{ моль}\]
5. По уравнению реакции определим количество вещества водорода и воды:
Согласно уравнению, на 1 моль \(Fe_{2}O_{3}\) требуется 3 моля \(H_{2}\) и образуется 3 моля \(H_{2}O\).
\[n(H_{2}) = 3 \cdot n(Fe_{2}O_{3}) = 3 \cdot 0,003 = 0,009 \text{ моль}\]
\[n(H_{2}O) = 3 \cdot n(Fe_{2}O_{3}) = 3 \cdot 0,003 = 0,009 \text{ моль}\]
6. Вычислим объем водорода (при н.у.), используя молярный объем \(V_{m} = 22,4 \text{ л/моль}\):
\[V(H_{2}) = n(H_{2}) \cdot V_{m} = 0,009 \text{ моль} \cdot 22,4 \text{ л/моль} = 0,2016 \text{ л}\]
(или 201,6 мл)
Ответ: \(V(H_{2}) = 0,2016 \text{ л}\); \(n(H_{2}O) = 0,009 \text{ моль}\).