schoolМатематика
verifiedРешено AI
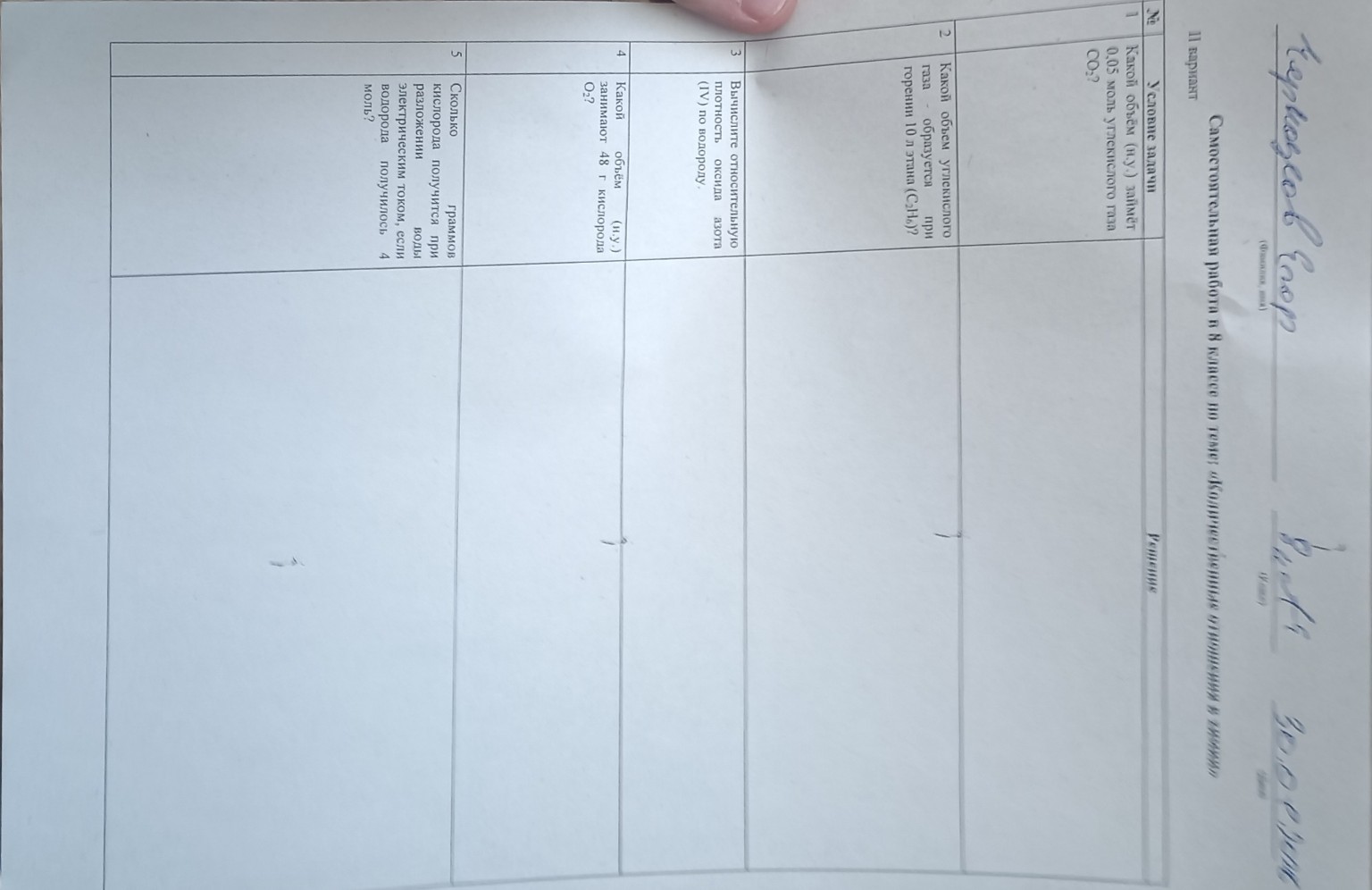
Решение задач по химии 8 класс (Вариант II)
help_outlineУсловие задачи
Выполни задания с дано и решением полным
lightbulbКраткий ответ
Представлено решение задач по химии для 8 класса. Рассчитан объем углекислого газа при нормальных условиях и при горении этана.
Подробное решение
Ниже представлено решение задач из самостоятельной работы по химии для 8 класса (Вариант II).
Задача №1
Дано:
\(n(CO_2) = 0,05\) моль
\(V_m = 22,4\) л/моль
Найти:
\(V(CO_2) - ?\)
Решение:
Объем газа при нормальных условиях (н.у.) рассчитывается по формуле:
\[V = n \cdot V_m\]
Подставим значения:
\[V(CO_2) = 0,05 \text{ моль} \cdot 22,4 \text{ л/моль} = 1,12 \text{ л}\]
Ответ: \(V(CO_2) = 1,12\) л.
Задача №2
Дано:
\(V(C_2H_6) = 10\) л
Найти:
\(V(CO_2) - ?\)
Решение:
1. Запишем уравнение реакции горения этана:
\[2C_2H_6 + 7O_2 \rightarrow 4CO_2 + 6H_2O\]
2. Согласно закону объемных отношений газов, объемы реагирующих и образующихся газов относятся как их стехиометрические коэффициенты:
\[\frac{V(C_2H_6)}{V(CO_2)} = \frac{2}{4} = \frac{1}{2}\]
3. Отсюда объем углекислого газа:
\[V(CO_2) = 2 \cdot V(C_2H_6) = 2 \cdot 10 \text{ л} = 20 \text{ л}\]
Ответ: \(V(CO_2) = 20\) л.
Задача №3
Дано:
Газ: \(NO_2\) (оксид азота IV)
Найти:
\(D_{H_2}(NO_2) - ?\)
Решение:
1. Рассчитаем молярные массы газов:
\[M(NO_2) = 14 + 16 \cdot 2 = 46 \text{ г/моль}\]
\[M(H_2) = 2 \cdot 1 = 2 \text{ г/моль}\]
2. Относительная плотность газа по водороду находится по формуле:
\[D_{H_2}(NO_2) = \frac{M(NO_2)}{M(H_2)}\]
\[D_{H_2}(NO_2) = \frac{46}{2} = 23\]
Ответ: \(D_{H_2} = 23\).
Задача №4
Дано:
\(m(O_2) = 48\) г
\(V_m = 22,4\) л/моль
Найти:
\(V(O_2) - ?\)
Решение:
1. Найдем количество вещества кислорода:
\[M(O_2) = 16 \cdot 2 = 32 \text{ г/моль}\]
\[n(O_2) = \frac{m(O_2)}{M(O_2)} = \frac{48 \text{ г}}{32 \text{ г/моль}} = 1,5 \text{ моль}\]
2. Найдем объем:
\[V(O_2) = n(O_2) \cdot V_m = 1,5 \text{ моль} \cdot 22,4 \text{ л/моль} = 33,6 \text{ л}\]
Ответ: \(V(O_2) = 33,6\) л.
Задача №5
Дано:
\(n(H_2) = 4\) моль
Найти:
\(m(O_2) - ?\)
Решение:
1. Запишем уравнение разложения воды электрическим током:
\[2H_2O \xrightarrow{эл. ток} 2H_2 \uparrow + O_2 \uparrow\]
2. По уравнению реакции видно, что из 2 моль водорода получается 1 моль кислорода. Составим пропорцию:
\[\frac{n(H_2)}{2} = \frac{n(O_2)}{1} \Rightarrow n(O_2) = \frac{n(H_2)}{2}\]
\[n(O_2) = \frac{4 \text{ моль}}{2} = 2 \text{ моль}\]
3. Вычислим массу кислорода:
\[M(O_2) = 32 \text{ г/моль}\]
\[m(O_2) = n(O_2) \cdot M(O_2) = 2 \text{ моль} \cdot 32 \text{ г/моль} = 64 \text{ г}\]
Ответ: \(m(O_2) = 64\) г.