schoolХимия
verifiedРешено AI
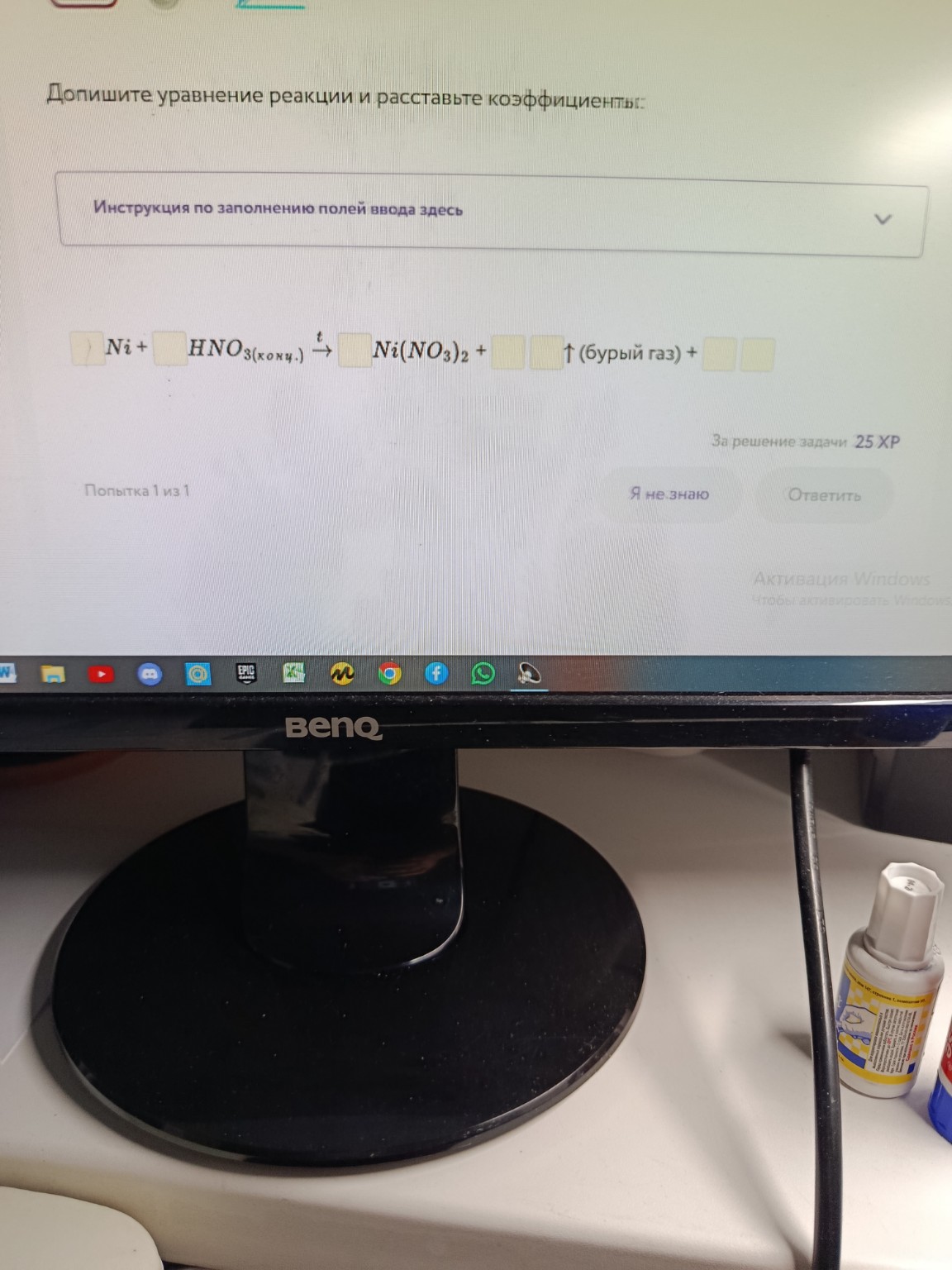
Решение задачи: Ni + HNO3 (конц.)
help_outlineУсловие задачи
lightbulbКраткий ответ
Взаимодействие никеля с концентрированной азотной кислотой приводит к образованию нитрата никеля(II), диоксида азота и воды. Уравнение реакции: Ni + 4HNO3(конц.) → Ni(NO3)2 + 2NO2 + 2H2O.
Подробное решение
Для решения этой задачи нужно составить уравнение реакции взаимодействия никеля с концентрированной азотной кислотой.
1. Определение продуктов:
При взаимодействии металлов средней активности (никель \( Ni \)) с концентрированной азотной кислотой при нагревании выделяется оксид азота (IV) — бурый газ \( NO_2 \) и образуется вода \( H_2O \).
2. Составление электронного баланса:
\[ Ni^0 - 2e \rightarrow Ni^{+2} \text{ (окисление)} \mid \times 1 \]
\[ N^{+5} + 1e \rightarrow N^{+4} \text{ (восстановление)} \mid \times 2 \]
3. Расстановка коэффициентов:
Перед \( NO_2 \) ставим коэффициент 2.
Чтобы уравнять азот (2 атома в соли и 2 в газе), перед \( HNO_3 \) ставим 4.
Чтобы уравнять водород, перед \( H_2O \) ставим 2.
Итоговое уравнение:
\[ Ni + 4HNO_3(конц.) \xrightarrow{t} Ni(NO_3)_2 + 2NO_2 \uparrow + 2H_2O \]
Заполнение полей ввода на сайте:
Первое поле (перед \( Ni \)): (пусто или 1)
Второе поле (перед \( HNO_3 \)): 4
Третье поле (перед \( Ni(NO_3)_2 \)): (пусто или 1)
Четвертое поле (коэффициент перед бурым газом): 2
Пятое поле (формула бурого газа): \( NO_2 \)
Шестое поле (коэффициент перед водой): 2
Седьмое поле (формула воды): \( H_2O \)
Для записи в тетрадь:
\[ Ni + 4HNO_3(конц.) = Ni(NO_3)_2 + 2NO_2 + 2H_2O \]