schoolХимия
verifiedРешено AI
Определение Окислителя и Восстановителя для Фосфора в Реакциях
help_outlineУсловие задачи
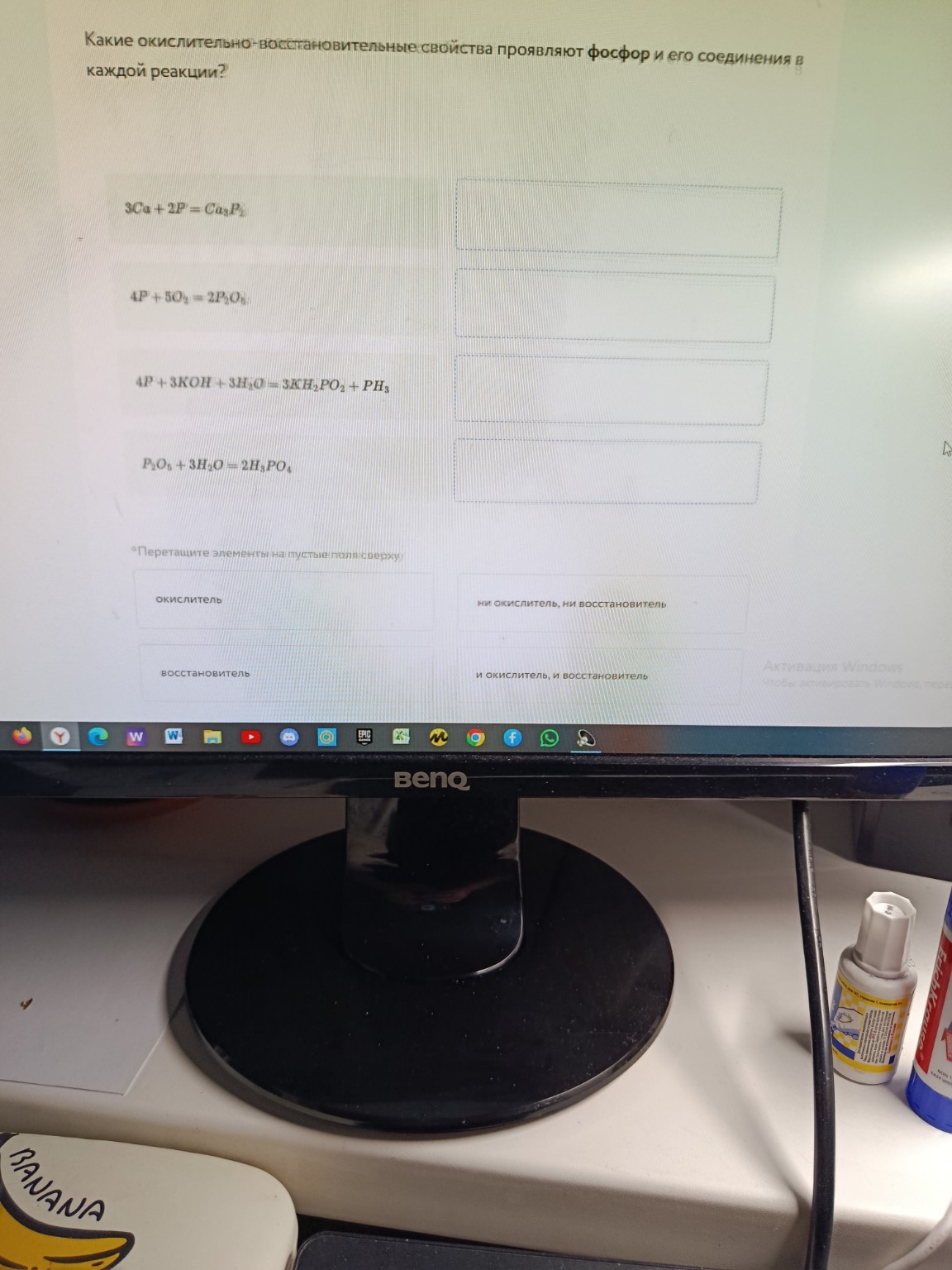
lightbulbКраткий ответ
Для определения окислителя и восстановителя нужно проследить за изменением степени окисления фосфора. Понижение степени окисления указывает на окислитель, повышение - на восстановитель.
Подробное решение
Для решения этой задачи нужно проследить за изменением степени окисления фосфора в каждой реакции. Если степень окисления понижается — вещество является окислителем, если повышается — восстановителем. Если одновременно и повышается, и понижается — и окислителем, и восстановителем. Если не меняется — ни тем, ни другим.
Разберем каждую реакцию:
1. \(3Ca + 2P = Ca_{3}P_{2}\)
Фосфор был простым веществом (степень окисления \(0\)), а стал фосфидом (\(-3\)). Степень окисления понизилась.
Ответ: окислитель
2. \(4P + 5O_{2} = 2P_{2}O_{5}\)
Фосфор был простым веществом (\(0\)), а стал оксидом (\(+5\)). Степень окисления повысилась.
Ответ: восстановитель
3. \(4P + 3KOH + 3H_{2}O = 3KH_{2}PO_{2} + PH_{3}\)
Это реакция диспропорционирования. Фосфор из степени окисления \(0\) переходит в \(+1\) (в составе \(KH_{2}PO_{2}\)) и в \(-3\) (в составе \(PH_{3}\)). Он одновременно и повышает, и понижает степень окисления.
Ответ: и окислитель, и восстановитель
4. \(P_{2}O_{5} + 3H_{2}O = 2H_{3}PO_{4}\)
В оксиде \(P_{2}O_{5}\) у фосфора степень окисления \(+5\). В ортофосфорной кислоте \(H_{3}PO_{4}\) у фосфора также степень окисления \(+5\). Степень окисления не изменилась.
Ответ: ни окислитель, ни восстановитель
Соответствие для перетаскивания:
1-я строка — окислитель
2-я строка — восстановитель
3-я строка — и окислитель, и восстановитель
4-я строка — ни окислитель, ни восстановитель