schoolХимия
verifiedРешено AI
Решение задачи: Взаимодействие LiOH, Li и Cu2O с серной кислотой
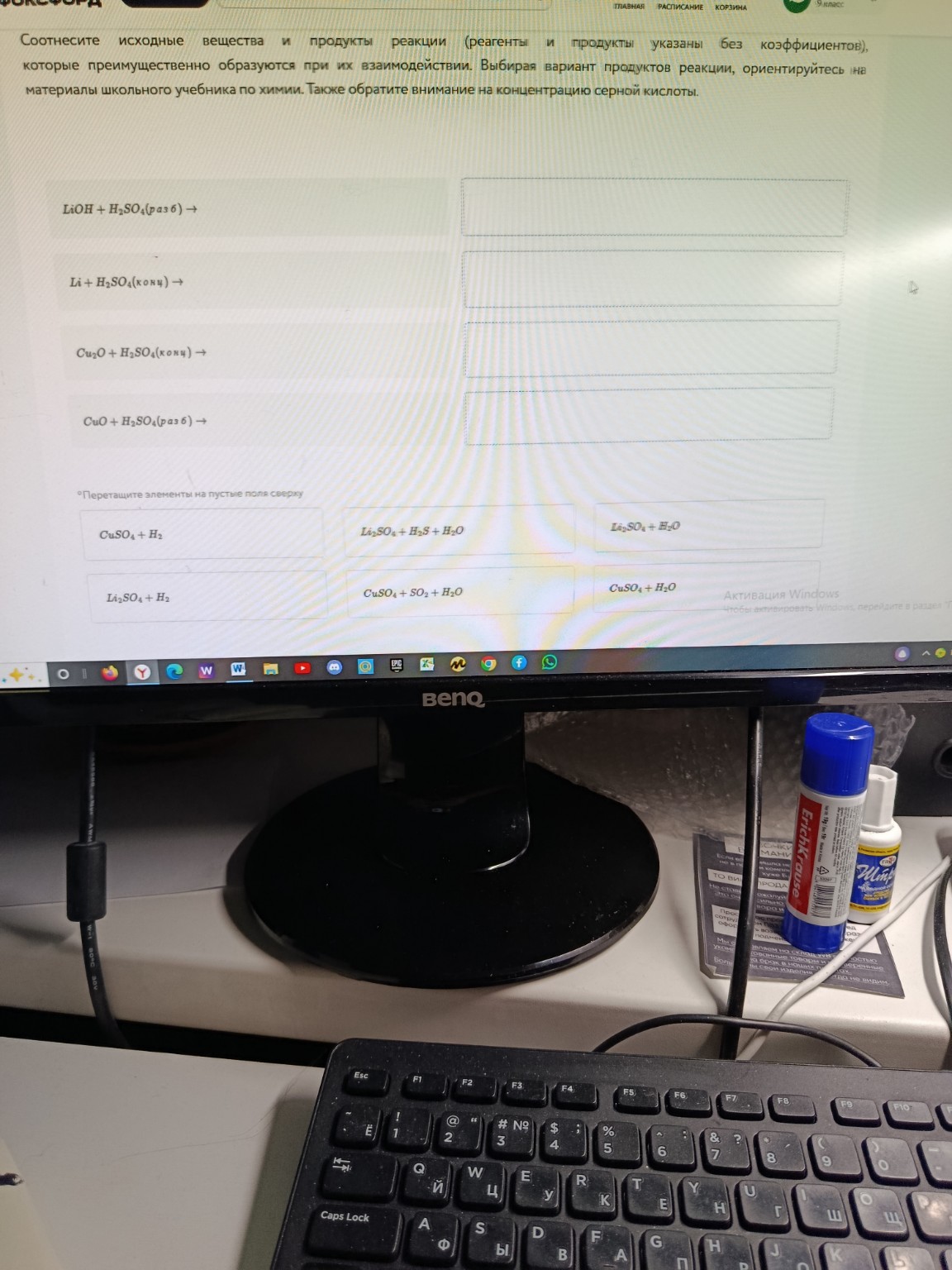
help_outlineУсловие задачи
lightbulbКраткий ответ
Правильные уравнения реакций: LiOH + H2SO4(разб) → Li2SO4 + H2O, Li + H2SO4(конц) → Li2SO4 + H2S + H2O, Cu2O + H2SO4(конц) → CuSO4 + SO2 + H2O. Объясняется механизм каждой реакции и роль концентрации кислоты.
Подробное решение
Для того чтобы правильно соотнести реагенты и продукты, нужно учитывать тип химической реакции и концентрацию кислоты. Ниже приведены правильные пары для записи в тетрадь:
1. \(LiOH + H_2SO_4(разб) \rightarrow Li_2SO_4 + H_2O\)
Это классическая реакция нейтрализации между щелочью и кислотой, в результате которой образуются соль и вода.
2. \(Li + H_2SO_4(конц) \rightarrow Li_2SO_4 + H_2S + H_2O\)
Литий — активный щелочной металл. При взаимодействии с концентрированной серной кислотой она восстанавливается максимально глубоко — до сероводорода \(H_2S\).
3. \(Cu_2O + H_2SO_4(конц) \rightarrow CuSO_4 + SO_2 + H_2O\)
В этой реакции медь в оксиде меди(I) имеет степень окисления \(+1\). Концентрированная серная кислота выступает как окислитель, окисляя медь до \(+2\) (сульфат меди(II)), а сама восстанавливается до сернистого газа \(SO_2\).
4. \(CuO + H_2SO_4(разб) \rightarrow CuSO_4 + H_2O\)
Это реакция основного оксида с разбавленной кислотой. Происходит обычный обмен, образуются соль и вода.
Итоговое соответствие для переноса в таблицу:
\[LiOH + H_2SO_4(разб) \longrightarrow Li_2SO_4 + H_2O\]
\[Li + H_2SO_4(конц) \longrightarrow Li_2SO_4 + H_2S + H_2O\]
\[Cu_2O + H_2SO_4(конц) \longrightarrow CuSO_4 + SO_2 + H_2O\]
\[CuO + H_2SO_4(разб) \longrightarrow CuSO_4 + H_2O\]