schoolХимия
verifiedРешено AI
Решение задачи: Оксиды, соответствующие гидроксидам
help_outlineУсловие задачи
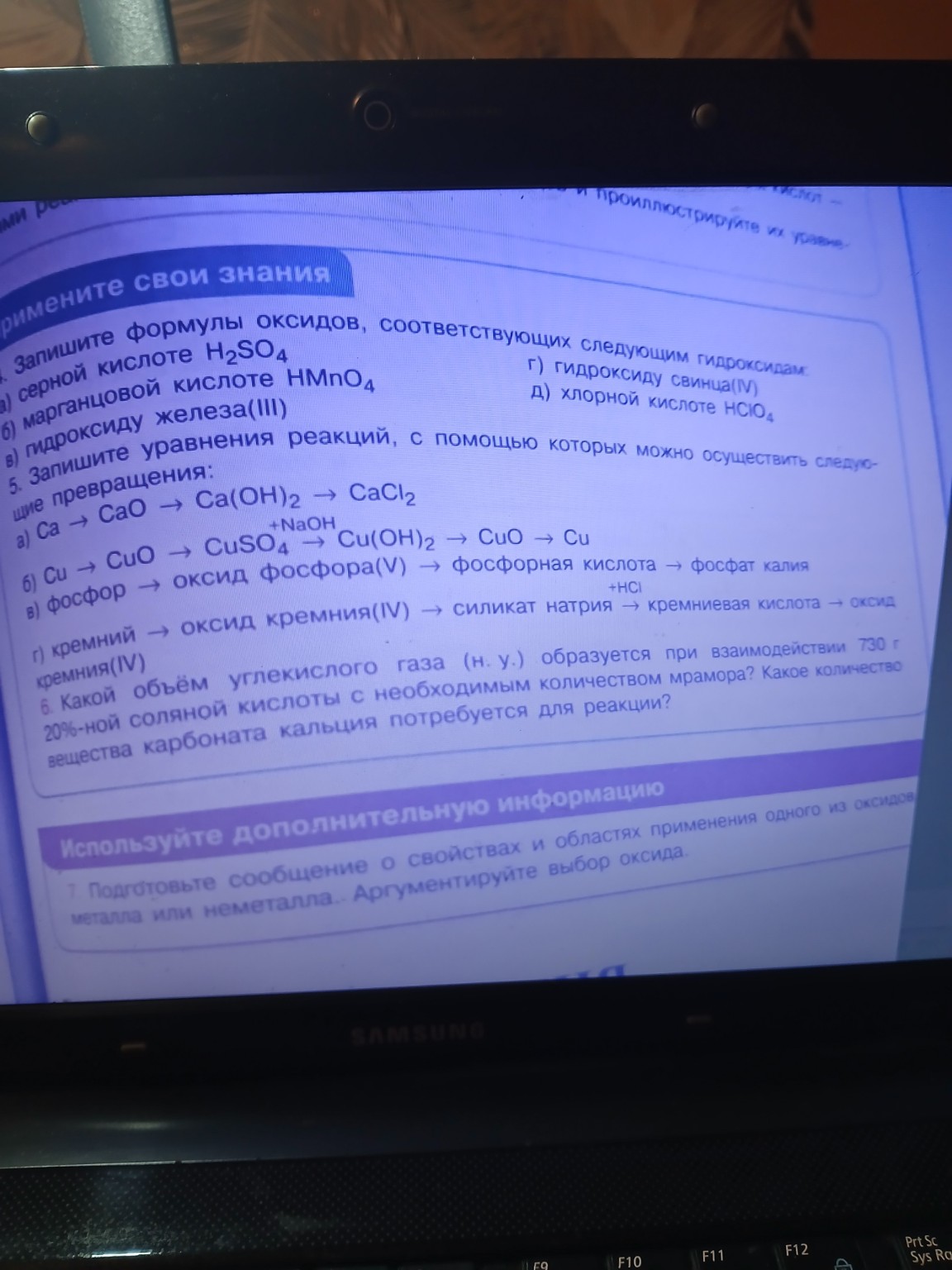
lightbulbКраткий ответ
Чтобы найти оксид, соответствующий гидроксиду, определите степень окисления центрального элемента в гидроксиде и составьте формулу оксида с той же степенью окисления. Например, для серной кислоты (H₂SO₄) это оксид серы (VI) - SO₃.
Подробное решение
Ниже представлены решения заданий с фотографии, оформленные для записи в школьную тетрадь.
Задание 4. Формулы оксидов, соответствующих гидроксидам.
Чтобы найти оксид, нужно определить степень окисления центрального элемента в гидроксиде и составить формулу оксида с такой же степенью окисления.
а) Серная кислота \( H_{2}SO_{4} \) (S имеет степень окисления +6) — оксид серы (VI) \( SO_{3} \).
б) Марганцовая кислота \( HMnO_{4} \) (Mn имеет степень окисления +7) — оксид марганца (VII) \( Mn_{2}O_{7} \).
в) Гидроксид железа (III) \( Fe(OH)_{3} \) (Fe имеет степень окисления +3) — оксид железа (III) \( Fe_{2}O_{3} \).
г) Гидроксид свинца (IV) \( Pb(OH)_{4} \) (Pb имеет степень окисления +4) — оксид свинца (IV) \( PbO_{2} \).
д) Хлорная кислота \( HClO_{4} \) (Cl имеет степень окисления +7) — оксид хлора (VII) \( Cl_{2}O_{7} \).
Задание 5. Уравнения реакций для превращений.
а) \( Ca \rightarrow CaO \rightarrow Ca(OH)_{2} \rightarrow CaCl_{2} \)
1) \( 2Ca + O_{2} = 2CaO \)
2) \( CaO + H_{2}O = Ca(OH)_{2} \)
3) \( Ca(OH)_{2} + 2HCl = CaCl_{2} + 2H_{2}O \)
б) \( Cu \rightarrow CuO \rightarrow CuSO_{4} \xrightarrow{+NaOH} Cu(OH)_{2} \rightarrow CuO \rightarrow Cu \)
1) \( 2Cu + O_{2} \xrightarrow{t} 2CuO \)
2) \( CuO + H_{2}SO_{4} = CuSO_{4} + H_{2}O \)
3) \( CuSO_{4} + 2NaOH = Cu(OH)_{2} \downarrow + Na_{2}SO_{4} \)
4) \( Cu(OH)_{2} \xrightarrow{t} CuO + H_{2}O \)
5) \( CuO + H_{2} \xrightarrow{t} Cu + H_{2}O \)
в) Фосфор \( \rightarrow \) оксид фосфора (V) \( \rightarrow \) фосфорная кислота \( \rightarrow \) фосфат калия
1) \( 4P + 5O_{2} = 2P_{2}O_{5} \)
2) \( P_{2}O_{5} + 3H_{2}O = 2H_{3}PO_{4} \)
3) \( H_{3}PO_{4} + 3KOH = K_{3}PO_{4} + 3H_{2}O \)
г) Кремний \( \rightarrow \) оксид кремния (IV) \( \rightarrow \) силикат натрия \( \xrightarrow{+HCl} \) кремниевая кислота \( \rightarrow \) оксид кремния (IV)
1) \( Si + O_{2} \xrightarrow{t} SiO_{2} \)
2) \( SiO_{2} + 2NaOH \xrightarrow{t} Na_{2}SiO_{3} + H_{2}O \)
3) \( Na_{2}SiO_{3} + 2HCl = H_{2}SiO_{3} \downarrow + 2NaCl \)
4) \( H_{2}SiO_{3} \xrightarrow{t} SiO_{2} + H_{2}O \)
Задание 6. Расчетная задача.
Дано:
\( m_{р-ра}(HCl) = 730 \) г
\( \omega(HCl) = 20\% = 0,2 \)
Найти: \( V(CO_{2}) \), \( n(CaCO_{3}) \)
Решение:
1) Уравнение реакции взаимодействия мрамора (карбоната кальция) с соляной кислотой:
\[ CaCO_{3} + 2HCl = CaCl_{2} + CO_{2} \uparrow + H_{2}O \]
2) Найдем массу чистого хлороводорода в растворе:
\[ m(HCl) = m_{р-ра} \cdot \omega = 730 \cdot 0,2 = 146 \text{ г} \]
3) Найдем количество вещества \( HCl \):
\[ n(HCl) = \frac{m}{M} = \frac{146}{36,5} = 4 \text{ моль} \]
4) По уравнению реакции:
\( n(CaCO_{3}) = \frac{1}{2} n(HCl) = \frac{4}{2} = 2 \text{ моль} \)
\( n(CO_{2}) = \frac{1}{2} n(HCl) = \frac{4}{2} = 2 \text{ моль} \)
5) Вычислим объем углекислого газа (н. у.):
\[ V(CO_{2}) = n \cdot V_{m} = 2 \cdot 22,4 = 44,8 \text{ л} \]
Ответ: \( V(CO_{2}) = 44,8 \) л; \( n(CaCO_{3}) = 2 \) моль.