schoolХимия
verifiedРешено AI
Решение задачи по химии: расчет объема раствора H2SO4 (pH=2)
help_outlineУсловие задачи
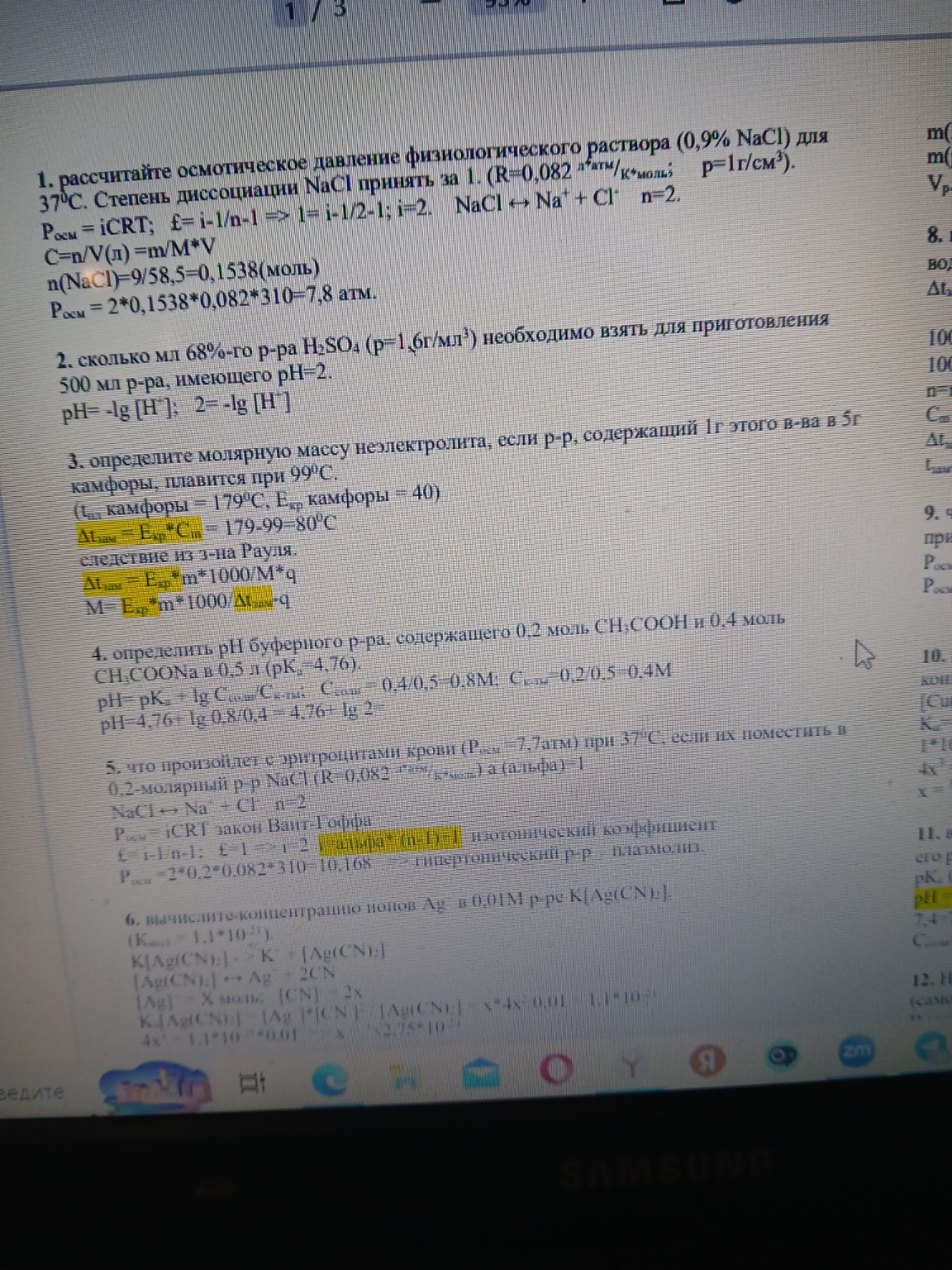
lightbulbКраткий ответ
Для получения 500 мл раствора с pH=2 потребуется определенное количество 68% раствора серной кислоты. Ниже представлено подробное решение с необходимыми расчетами.
Подробное решение
Ниже представлено решение задач №2 и №3 с изображения в удобном для переписывания виде.
Задача №2
Дано:
\(\omega(H_2SO_4) = 68\%\) (или 0,68)
\(\rho_{р-ра} = 1,6 \, г/мл\)
\(V_{конечный} = 500 \, мл = 0,5 \, л\)
\(pH = 2\)
Найти: \(V(68\% \, р-ра) - ?\)
Решение:
1. Находим концентрацию ионов водорода через pH:
\[pH = -\lg[H^+] \Rightarrow [H^+] = 10^{-pH} = 10^{-2} = 0,01 \, моль/л\]
2. Серная кислота — сильный электролит, диссоциирует по уравнению:
\(H_2SO_4 \rightarrow 2H^+ + SO_4^{2-}\)
Следовательно, молярная концентрация кислоты \(C_M\) в 2 раза меньше концентрации ионов водорода:
\[C_M(H_2SO_4) = \frac{[H^+]}{2} = \frac{0,01}{2} = 0,005 \, моль/л\]
3. Находим количество вещества кислоты в 500 мл раствора:
\[n(H_2SO_4) = C_M \cdot V = 0,005 \cdot 0,5 = 0,0025 \, моль\]
4. Находим массу чистой кислоты:
\(M(H_2SO_4) = 98 \, г/моль\)
\[m(H_2SO_4) = n \cdot M = 0,0025 \cdot 98 = 0,245 \, г\]
5. Находим массу и объем исходного 68%-го раствора:
\[m_{р-ра} = \frac{m(H_2SO_4)}{\omega} = \frac{0,245}{0,68} \approx 0,36 \, г\]
\[V_{р-ра} = \frac{m_{р-ра}}{\rho} = \frac{0,36}{1,6} = 0,225 \, мл\]
Ответ: 0,225 мл.
---
Задача №3
Дано:
\(m_{в-ва} = 1 \, г\)
\(m_{камфоры} = 5 \, г\)
\(T_{пл. камфоры} = 179^\circ C\)
\(T_{пл. р-ра} = 99^\circ C\)
\(E_{кр} = 40\)
Найти: \(M_{неэлектролита} - ?\)
Решение:
1. Находим понижение температуры плавления:
\[\Delta T_{зам} = T_{пл. камфоры} - T_{пл. р-ра} = 179 - 99 = 80^\circ C\]
2. Используем следствие из закона Рауля для определения молярной массы:
\[\Delta T_{зам} = E_{кр} \cdot C_m = E_{кр} \cdot \frac{m_{в-ва} \cdot 1000}{M \cdot m_{камфоры}}\]
3. Выражаем и рассчитываем молярную массу \(M\):
\[M = \frac{E_{кр} \cdot m_{в-ва} \cdot 1000}{\Delta T_{зам} \cdot m_{камфоры}}\]
\[M = \frac{40 \cdot 1 \cdot 1000}{80 \cdot 5} = \frac{40000}{400} = 100 \, г/моль\]
Ответ: 100 г/моль.