schoolХимия
verifiedРешено AI
Решение Варианта 3 школьной задачи по химии
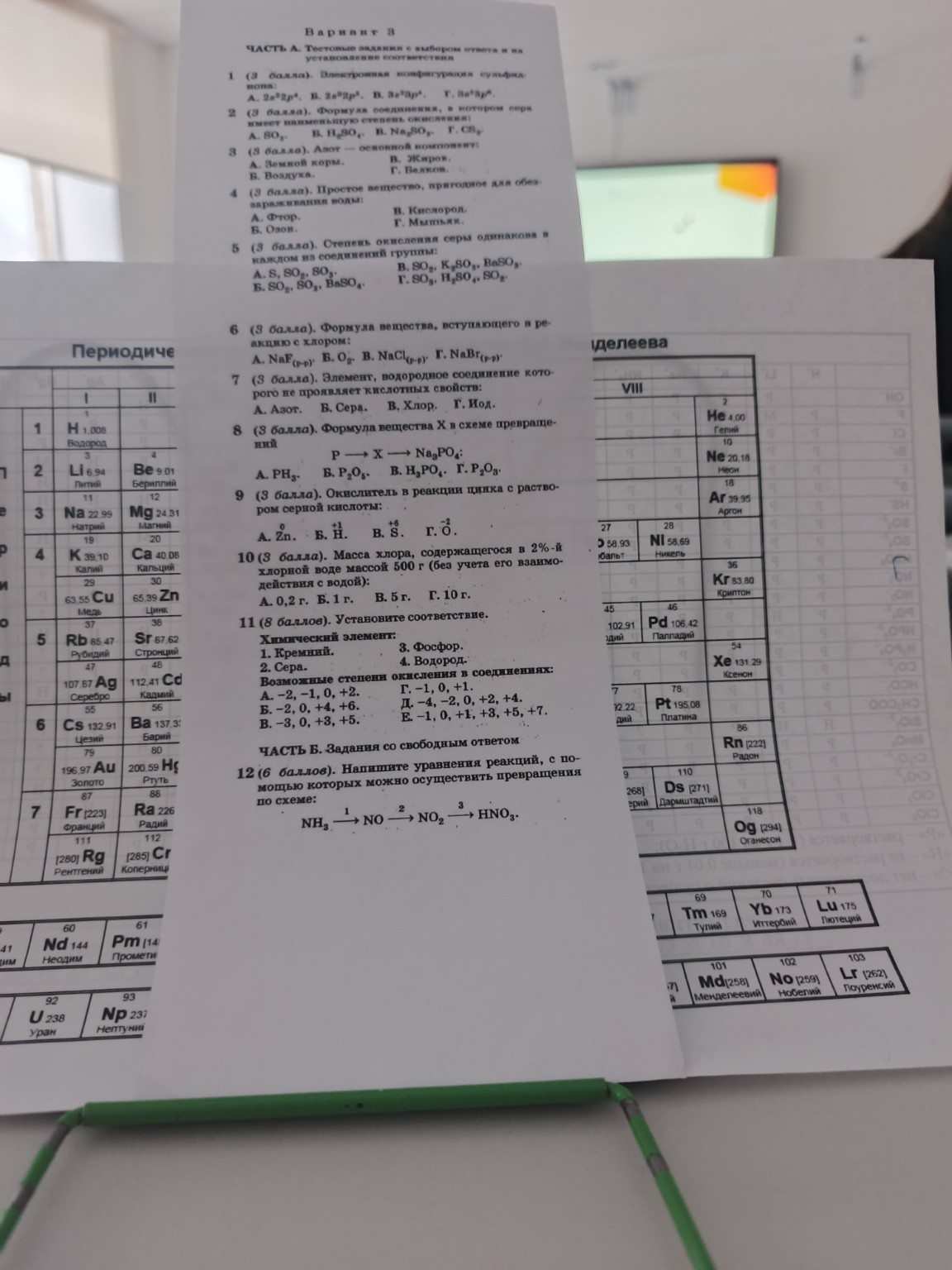
help_outlineУсловие задачи
lightbulbКраткий ответ
Представлено подробное решение задач варианта 3 по химии. Включает определение электронной конфигурации сульфид-иона, степени окисления серы и роль азота в воздухе.
Подробное решение
Ниже представлены решения заданий Варианта 3, оформленные для записи в тетрадь.
ЧАСТЬ А
1. Электронная конфигурация сульфид-иона \(S^{2-}\). Сера находится в 3 периоде, VI группе. Атом серы имеет конфигурацию \(1s^2 2s^2 2p^6 3s^2 3p^4\). Принимая 2 электрона, ион получает конфигурацию благородного газа аргона.
Ответ: Г. \(2s^2 2p^6 3s^2 3p^6\).
2. Формула соединения, в котором сера имеет наименьшую степень окисления. Минимальная степень окисления серы равна \(-2\). В соединении \(CS_2\) (сероуглерод) у серы \(-2\).
Ответ: Г. \(CS_2\).
3. Азот — основной компонент:
Ответ: Б. Воздуха (составляет около 78% по объему).
4. Простое вещество, пригодное для обеззараживания воды:
Ответ: Б. Озон (процесс озонирования).
5. Степень окисления серы одинакова в каждом из соединений группы:
В группе Г: \(SO_3\) (\(+6\)), \(H_2SO_4\) (\(+6\)), \(SO_4^{2-}\) (\(+6\)).
Ответ: Г. \(SO_3, H_2SO_4, SO_4^{2-}\).
6. Формула вещества, вступающего в реакцию с хлором:
Хлор как более активный галоген вытесняет бром из его солей.
Ответ: Г. \(NaBr_{(р-р)}\).
7. Элемент, водородное соединение которого не проявляет кислотных свойств:
Аммиак (\(NH_3\)) проявляет основные свойства.
Ответ: А. Азот.
8. Формула вещества X в схеме превращений \(P \rightarrow X \rightarrow Na_3PO_4\):
При сгорании фосфора образуется оксид фосфора (V).
Ответ: Б. \(P_2O_5\).
9. Окислитель в реакции цинка с раствором серной кислоты:
\[Zn + H_2SO_4 \rightarrow ZnSO_4 + H_2 \uparrow\]
Цинк \(Zn^0\) отдает электроны (восстановитель), а ионы водорода \(H^+\) принимают их.
Ответ: Б. \(H^+\).
10. Масса хлора в 500 г 2%-й хлорной воды:
\[m(Cl_2) = m(р-ра) \cdot \omega = 500 \cdot 0,02 = 10 \text{ г}\]
Ответ: Г. 10 г.
11. Соответствие химического элемента и степеней окисления:
1. Кремний (Si): Д. \(-4, -2, 0, +2, +4\).
2. Сера (S): Б. \(-2, 0, +4, +6\).
3. Фосфор (P): В. \(-3, 0, +3, +5\).
4. Водород (H): Г. \(-1, 0, +1\).
ЧАСТЬ Б
12. Уравнения реакций для схемы превращений:
1) Каталитическое окисление аммиака:
\[4NH_3 + 5O_2 \xrightarrow{kat, t} 4NO + 6H_2O\]
2) Окисление оксида азота (II) кислородом воздуха:
\[2NO + O_2 \rightarrow 2NO_2\]
3) Растворение диоксида азота в воде в присутствии избытка кислорода:
\[4NO_2 + O_2 + 2H_2O \rightarrow 4HNO_3\]