schoolМатематика
verifiedРешено AI
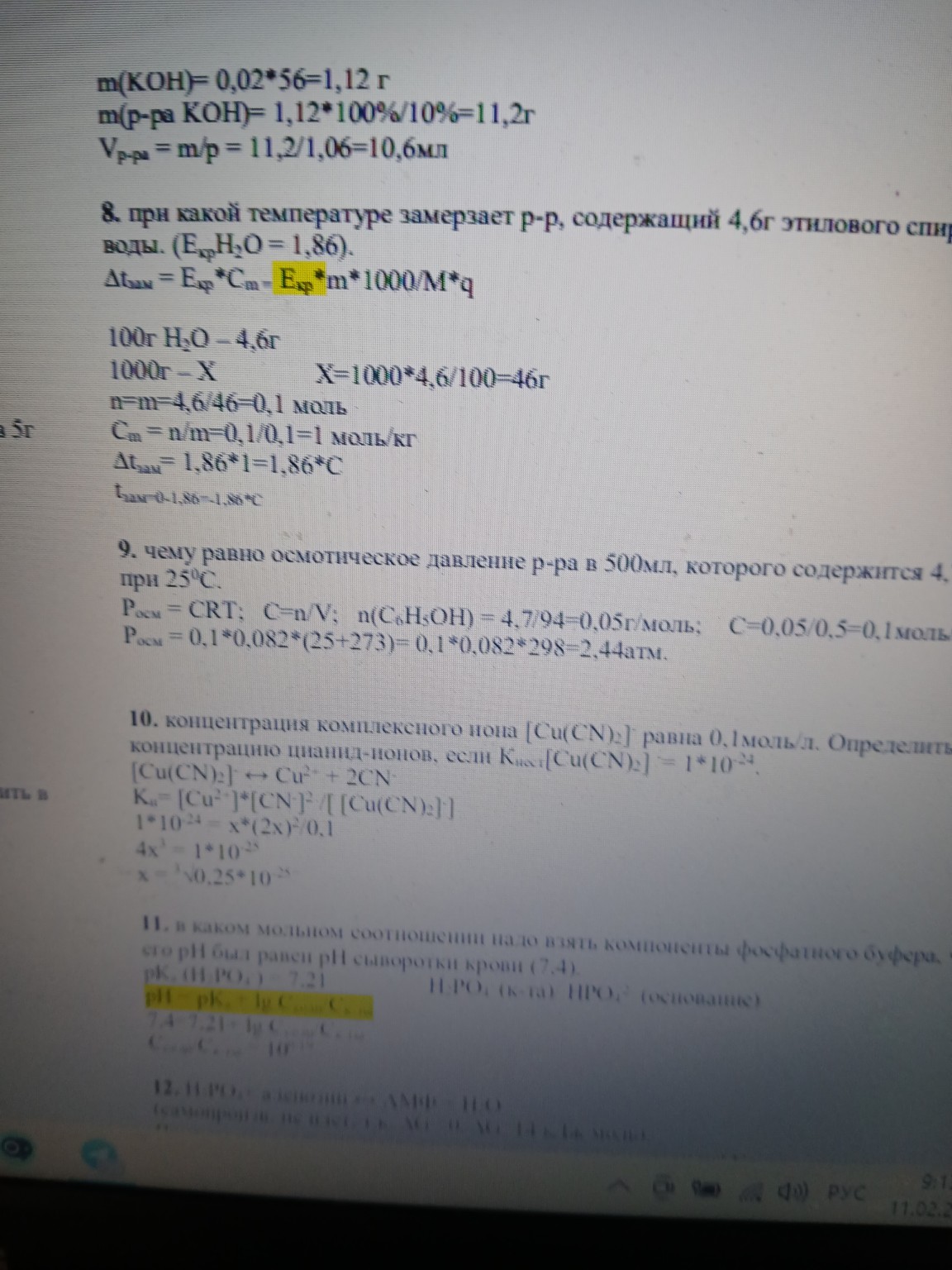
Решение задач №8, 9, 10, 11 по химии
help_outlineУсловие задачи
lightbulbКраткий ответ
Представлено подробное решение задач по химии для школьной тетради. Включает вычисления, формулы и ответы к задачам №8, 9, 10 и 11.
Подробное решение
Ниже представлено решение задач №8, №9, №10 и №11, оформленное для записи в школьную тетрадь.
Задача №8
Дано:
\(m(C_2H_5OH) = 4,6 \, г\)
\(m(H_2O) = 100 \, г = 0,1 \, кг\)
\(K_{кр}(H_2O) = 1,86\)
\(M(C_2H_5OH) = 46 \, г/моль\)
Найти:
\(t_{зам} - ?\)
Решение:
1. Находим количество вещества спирта:
\[n = \frac{m}{M} = \frac{4,6}{46} = 0,1 \, моль\]
2. Находим моляльную концентрацию раствора (\(C_m\)):
\[C_m = \frac{n(вещества)}{m(растворителя, кг)} = \frac{0,1}{0,1} = 1 \, моль/кг\]
3. Вычисляем понижение температуры замерзания:
\[\Delta t_{зам} = K_{кр} \cdot C_m = 1,86 \cdot 1 = 1,86^{\circ}C\]
4. Температура замерзания чистого растворителя (воды) \(0^{\circ}C\), значит:
\[t_{зам} = 0 - 1,86 = -1,86^{\circ}C\]
Ответ: \(-1,86^{\circ}C\).
Задача №9
Дано:
\(V = 500 \, мл = 0,5 \, л\)
\(m(C_6H_5OH) = 4,7 \, г\)
\(t = 25^{\circ}C \Rightarrow T = 298 \, К\)
\(M(C_6H_5OH) = 94 \, г/моль\)
\(R = 0,082 \, \frac{л \cdot атм}{моль \cdot К}\)
Найти:
\(P_{осм} - ?\)
Решение:
1. Находим количество вещества фенола:
\[n = \frac{m}{M} = \frac{4,7}{94} = 0,05 \, моль\]
2. Находим молярную концентрацию:
\[C = \frac{n}{V} = \frac{0,05}{0,5} = 0,1 \, моль/л\]
3. Вычисляем осмотическое давление:
\[P_{осм} = C \cdot R \cdot T = 0,1 \cdot 0,082 \cdot 298 \approx 2,44 \, атм\]
Ответ: \(2,44 \, атм\).
Задача №10
Дано:
\([[Cu(CN)_2]^-] = 0,1 \, моль/л\)
\(K_{нест} = 1 \cdot 10^{-24}\)
Найти:
\([CN^-] - ?\)
Решение:
1. Уравнение диссоциации комплекса:
\[[Cu(CN)_2]^- \rightleftharpoons Cu^+ + 2CN^-\]
2. Пусть \([Cu^+] = x\), тогда \([CN^-] = 2x\).
3. Выражение константы нестойкости:
\[K_{нест} = \frac{[Cu^+] \cdot [CN^-]^2}{[[Cu(CN)_2]^-]}\]
\[1 \cdot 10^{-24} = \frac{x \cdot (2x)^2}{0,1} \Rightarrow 1 \cdot 10^{-24} = \frac{4x^3}{0,1}\]
\[4x^3 = 1 \cdot 10^{-25} \Rightarrow x^3 = 0,25 \cdot 10^{-25} = 25 \cdot 10^{-27}\]
\[x = \sqrt[3]{25 \cdot 10^{-27}} \approx 2,92 \cdot 10^{-9} \, моль/л\]
4. Концентрация цианид-ионов:
\[[CN^-] = 2x = 2 \cdot 2,92 \cdot 10^{-9} = 5,84 \cdot 10^{-9} \, моль/л\]
Ответ: \(5,84 \cdot 10^{-9} \, моль/л\).
Задача №11
Дано:
\(pH = 7,4\)
\(pK_a(H_2PO_4^-) = 7,21\)
Найти:
\(\frac{C_{соли}}{C_{кислоты}} - ?\)
Решение:
1. Для фосфатного буфера (состоящего из \(H_2PO_4^-\) как кислоты и \(HPO_4^{2-}\) как соли/основания) используем уравнение Гендерсона-Хассельбаха:
\[pH = pK_a + \lg \frac{C_{соли}}{C_{кислоты}}\]
2. Подставим значения:
\[7,4 = 7,21 + \lg \frac{C_{соли}}{C_{кислоты}}\]
\[\lg \frac{C_{соли}}{C_{кислоты}} = 7,4 - 7,21 = 0,19\]
3. Находим соотношение:
\[\frac{C_{соли}}{C_{кислоты}} = 10^{0,19} \approx 1,55\]
Ответ: соотношение соли к кислоте составляет \(1,55 : 1\).