schoolХимия
verifiedРешено AI
Решение цепочки превращений: H2S → SO2 → SO3 → K2SO4
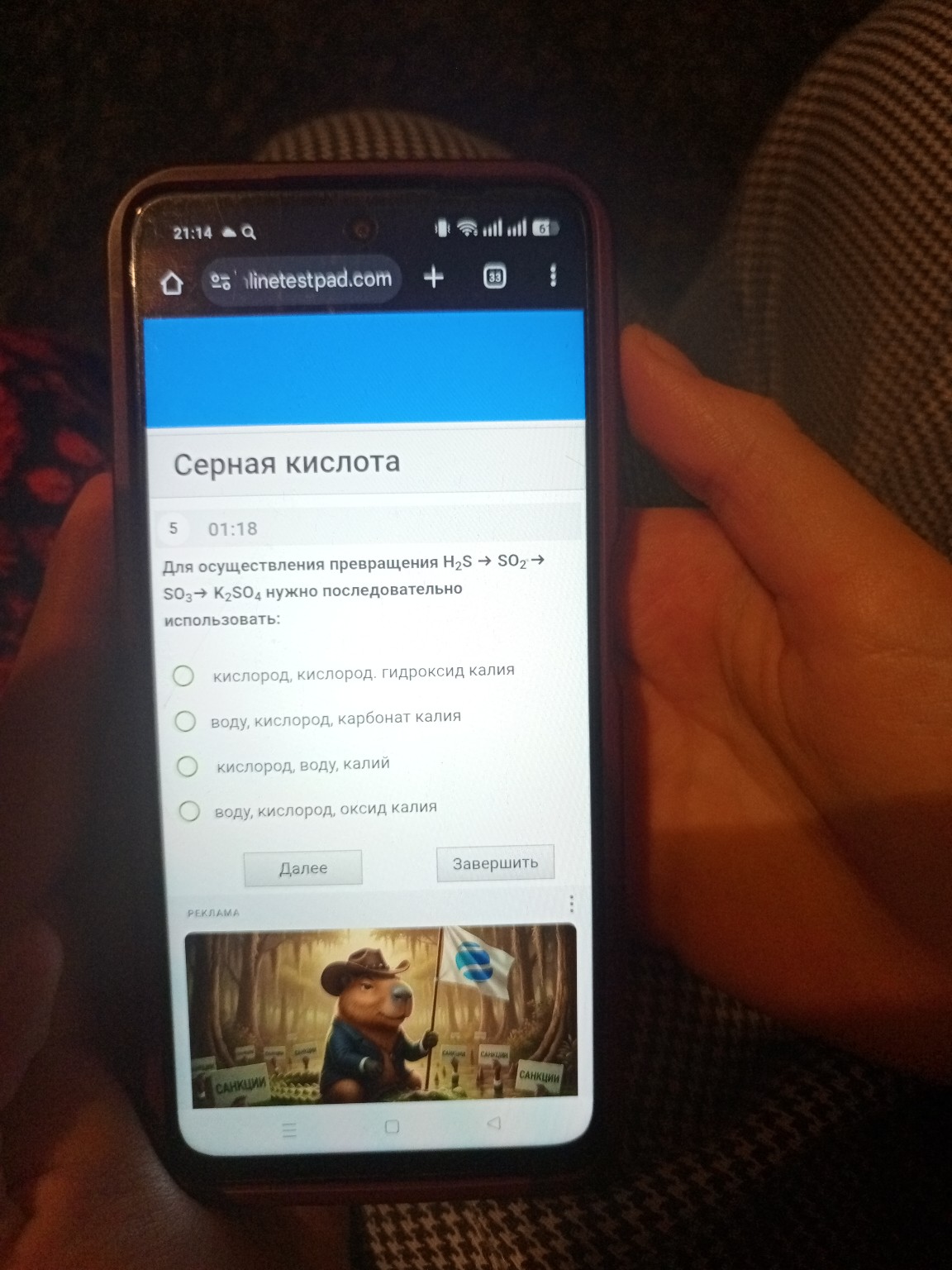
help_outlineУсловие задачи
lightbulbКраткий ответ
Для превращения H2S в K2SO4 требуется последовательно провести реакции с кислородом и гидроксидом калия. Сначала H2S сжигается до SO2, затем SO2 окисляется до SO3, который реагирует с KOH, образуя K2SO4.
Подробное решение
Для решения этой цепочки превращений разберем каждую стадию реакции:
1. \( H_{2}S \rightarrow SO_{2} \)
Чтобы из сероводорода получить оксид серы(IV), его нужно сжечь в избытке кислорода:
\[ 2H_{2}S + 3O_{2} = 2SO_{2} + 2H_{2}O \]
Используемое вещество: кислород.
2. \( SO_{2} \rightarrow SO_{3} \)
Для дальнейшего окисления оксида серы(IV) до оксида серы(VI) также требуется кислород (реакция идет в присутствии катализатора):
\[ 2SO_{2} + O_{2} \rightleftarrows 2SO_{3} \]
Используемое вещество: кислород.
3. \( SO_{3} \rightarrow K_{2}SO_{4} \)
Оксид серы(VI) — это кислотный оксид. Чтобы получить соль (сульфат калия), нужно провести реакцию со щелочью — гидроксидом калия:
\[ SO_{3} + 2KOH = K_{2}SO_{4} + H_{2}O \]
Используемое вещество: гидроксид калия.
Таким образом, последовательность необходимых веществ: кислород, кислород, гидроксид калия.
Правильный ответ: кислород, кислород, гидроксид калия.